Генетика людини: методичка
2.3. Прикладна генетика
У другій половині XX сторіччя на межі генетики та молекулярної біології сформувалася нова потужна галузь науки – біотехнологія. Її значення ілюструється тим фактом, що в США саме на біотехнологію витрачається майже половина коштів, виділених для академічних наукових досліджень. Біотехнологія сьогодні все більше використовується в промисловості, медицині, сільському господарстві та багатьох інших сферах людської діяльності. Її досягнення можуть бути спрямовані на благо людей, але можуть завдати людству і значну шкоду. За такої ситуації слід пам’ятати, що, чим ширшою інформацією ми володіємо, виробляючи власну точку зору, і чим більше людей готові обговорювати ці проблеми, тим з більшою вірогідністю ухвалені нами рішення виявляться правильними.
2.3.1. Генна інженерія
Генна інженерія – це найпотужніший метод прикладної генетики та біотехнології. Вона дає змогу вивчати і змінювати генетичний код живих організмів. Людина дістала можливість змінювати інші організми для своїх потреб, а в недалекому майбутньому й лікувати спадкові хвороби.
Бактерії. Основні методи генної інженерії були розроблені в другій половині ХХ століття на бактеріях. Вони полягали у введення в організм нового гена. Такий ген може бути синтезований наново, а може бути перенесений з іншого організму. Якщо в геном бактерії вбудувати ген, що кодує якийнебудь білок, бактерійна клітина перетворюється на живу фабрику по продокуванню цього білка.
Одержати будь-яку кількість копій гена всього з одного його зразка сьогодні неважко. Цей процес дістав назву клонування Для клонування гена користуються так званим вектором, у ролі якого виступає звичайно плазміда або бактеріофаг . Плазміда являє собою невеликий кільцевий фрагмент ДНК, виявлений в деяких бактеріях. Вона відокремлена від основної ДНК і реплікується незалежно від неї. Бактеріофаги (або, скорочено, фаги) – це віруси, які можуть вводити свою ДНК в бактеріальну клітину, де ця ДНК реплікується.
Фрагменти ДНК, тобто гени, які необхідно клонувати, за допомогою спеціального ферменту вилучають із генома організма-донора , а потім за допомогою іншого ферменту сполучають з плазмідною чи фаговою ДНК. Якщо таку гібридну ДНК ввести в бактеріальну клітину, то в процесі розмноження бактерії збільшується і кількість копій цієї ДНК. Модифіковані таким чином бактерії здатні продукувати необхідні людині речовини, чого в нормі вони робити не здатні, наприклад інсулін, гормон росту людини, коров’ячий соматотропін тощо..
Інсулін – це гормон білкової природи, який утворюється в підшлунковій залозі і грає життєво важливу роль в регуляції вмісту цукру в крові. Недолік інсуліну служить однією з причин цукрового діабету – тяжкого захворювання, через яке потерпає близько 3% населення Земної кулі. Зараз більше 2 млн. хворих на діабет у всьому світі користуються для лікування інсуліном, одержаним за допомогою модифікованих бактерій, коли в бактеріальний геном вбудовується ген інсуліну людини.
Гормон росту – це білок, який виробляється гіпофізом і діє на всі тканини організму. Нестача цього гормону в дитинстві приводить до карликовості з нормальними пропорціями тіла. Для медичних потреб гормон росту одержують за допомогою бактерій з вбудованим в їх геном людським геном, що забезпечує синтез цього білка. Регулярні ін’єкції такого гормону хворим дітям відновлюють їхній зріст майже до нормального рівня.
Коров’ячий соматотропін – це гормон, подібний до гормону росту людини. Він теж виробляється в гіпофізі та стимулює поділ клітин у тілі тварин. Ген, що кодує коров’ячий соматотропін, був вбудований в геном бактерії описаним вище способом. Ін’єкції навіть невеликих доз цього гормону коровам збільшують продукцію молока на 25%, а масу худоби, вирощуваної на м’ясо – на 10-15%. Після припинення ін’єкцій маса корів та їх удійність поверталися до початкового рівня.
За допомогою генної інженерії стало можливим створення бактерій, здатних очищати поверхню водоймищ від нафтового забруднення. Існуючий нині спосіб хімічного очищення надзвичайно шкідливий для живої природи. В даний час проводяться випробування створених штучно бактерій, які здатні руйнувати вуглеводні сполуки нафти.
Рослини і тварини. Багатоклітинні організми теж можна змінювати за допомогою генної інженерії. Організми, які генетично перебудовані з використанням методів генної інженерії, прийнято називати трансгенними.
Виведення трансгенних організмів є перспективною альтернативою традиційним методам селекції тварин та рослин. Поліпшення сортів рослин та порід тварин традиційними методами – тривалий процес, який потребує 7– 12 років. Генна інженерія дає можливість створювати нові форми рослин і тварин з потрібними людині властивостями всього за кілька років. Трансгенні рослини чи тварини, подібно до бактерій, можуть стати дешевим і простим засобом виробництва достатньої кількості різноманітних корисних продуктів, і не тільки харчових.
2.3.2. Трансгенні організми
Трансгенні рослини. Найефективніший метод перенесення генів у рослини – використання плазміди одного з видів ґрунтової бактерії як вектора. За допомогою вектора потрібний ген вбудовується в геном клітин рослини, яку ми хочемо змінити. Для цього клітини рослини розмножують в пробірці у поживному розчині. Клітини рослин з вбудованою в їх геном зміненою плазмідою називаються трансформованими. Діючи певними гормонами, можна із трансформованої клітини виростити цілу рослину.
Ця технологія використовується для виведення поліпшених сортів томатів, картоплі, кукурудзи, рису, цукрового буряка та багатьох інших рослин.
Ці сорти більш продуктивні, дають продукцію з підвищеним вмістом певних речовин (білків, жирів, вуглеводів тощо), а головне, є стійкими проти збудників хвороб та комах-шкідників. Остання особливість дасть змогу зменшити забруднення біосфери отрутохімікатами, які сьогодні широко застосовуються в рослинництві.
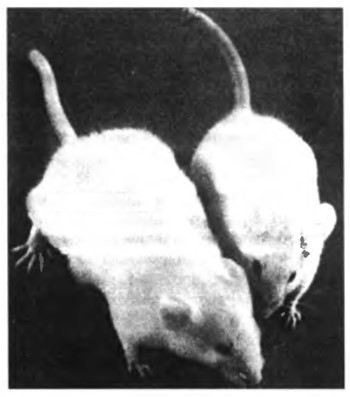
Мал. 19. Перша трансгенна тварина
Трансгенні тварини. Один із перших успішних експериментів по створенню трансгенних тварин був здійснений на мишах. В геном миші був вбудований ген, що кодує гормон росту щура. Такі трансгенні миші росли в 2-3 рази швидше, ніж їх родичі, не несучі чужого гена, і досягали приблизно в 2 рази більших розмірів. (Мал. 19). Для створення трансгенних тварин використовують різні методи введення ДНК: за допомогою вірусів; мікроін’єкції в яйцеклітини; в стовбурні клітини; способом фагоцитозу та інші
В даний час все більш популярним стає процес, який є більш контрольованим в порівнянні з іншими. Декілька клітин раннього зародка розмножують в живильному середовищі. ДНК вводять в ці клітини різними способами, у тому числі за допомогою мікроін’єкції. Перевага даного методу полягає в тому, що трансформовані клітини можна визначити до того, як вони будуть уведені в материнські організми як яйцеклітини. Таким чином забезпечується народження трансгенного організму.
Один з найперспективніших напрямків генної інженерії – продукування рідкісних і дорогих білків, вживаних у медицині, з молока трансгенних корів або овець. Прикладом може слугувати одержання білка з молока трансгенних овець, який ефективно лікує спадкову емфізему легенів людини, викликану мутацією гена. Трансгенні тварини були одержані шляхом введення в їх геном нормального алеля цього гена людини.
Вбудовування людського гена в геном вівці було використано і при отриманні одного з ферментів згортання крові, відсутність якого спричиняє один із видів гемофілії. Генетики працюють над одержанням таким же шляхом фібриногену – головного білка системи згортання крові. Його передбачають використовувати як клей для з’єднання тканин після хірургічних операцій.
2.3.3. Клонування тварин
Клонуванням називають створення численних генетичних копій одного індивідуума за допомогою безстатевого розмноження. У хребетних тварин цей процес природним шляхом не відбувається. Проте, пересадивши ядро, узяте з клітини кишечника або шкіри жаби, в яйцеклітину, власне ядро якої було зруйновано ультрафіолетовими променями, в 60-х роках ХХ ст. в Оксфордському університеті вдалося виростити пуголовка, що перетворився потім в жабу, ідентичну тій батьківській особині, від якої було узято ядро.
Подальші подібні експерименти довели, що диференційовані клітини (клітини різноманітних специфічних тканин тіла) містять всю інформацію, необхідну для розвитку повноцінного організму. А наприкінці минулого століття в Шотландії біло здійснено успішне клонування високоорганізованої хребетної тварини – вівці (Доллі) з клітини материнського вимені.
Клонування тварин представляється вельми перспективним. Можна, наприклад, використовувати зародки тварин на стадії декількох клітин і, розділивши такий зародок на окремі клітини, одержати певну кількість генетично ідентичних (однакових) організмів. Цей процес можна повторювати багато разів, тому що на цій стадії клітини ще не досягають необоротної спеціалізації. Таким чином можна створити безліч ідентичних копій однієї тварини, що має цінні ознаки. Потім одержані зародки можна пересадити в матку замінних матерів для виношування плоду та наступного народження тварин з бажаними ознаками. Подібне клонування зародків починає грати все більш важливу роль у тваринництві, наприклад при розведенні великої рогатої худоби, овець та кіз. Воно прискорює отримання будь-якої кількості тварин від бажаних материнських особин.
Клонування людини було вперше здійснено в США в 1993 р., проте клоновані зародки були доведені лише до стадії декількох клітин, щоб показати, що в принципі це можливо.
2.3.4. Етичні та соціальні проблеми генної інженерії
З перших же кроків генної інженерії учені повністю усвідомлювали, як важливо мати на увазі потенційну небезпеку та етичні проблеми, пов’язані з цією новою галуззю біології.
Безпека людини та біосфери. Першим дозволеним до продажу харчовим продуктом були трансгенні томати. На цьому прикладі ми розглянемо питання, що стосуються безпечності трансгенних харчових продуктів. Одна з головних проблем безпеки пов’язана з наявністю в геномі модифікованих томатів гена стійкості до антибіотика канаміцину, який відіграє роль маркера для виявлення трансформованих клітин. Внаслідок споживання плодів таких томатів ген стійкості проти антибіотика може потрапити в геном бактерії Escherichia coli, що живе в кишечнику людини. Оскільки бактерії виводяться з організму разом з фекаліями, ген може розповсюдитися в навколишньому середовищі та передатися іншим хвороботворним бактеріям, які, потрапивши в організм людини, виявляться стійкими до антибіотиків. Однак насправді ген томату разом зі всією іншою ДНК звичайно буде розщеплений в травному каналі людини. Навіть якщо цього не трапиться, вірогідність того, що ген пройде через серію організмів, надзвичайно мала. Крім того, гени стійкості до деяких антибіотиків, на жаль, вже поширені в навколишньому середовищі.
Ще одним прикладом подібно модифікованих рослин є впроваджена у виробництво кукурудза, яка містить бактеріальний ген, що підвищує її стійкість до шкідників та хвороб, а також маркерний ген стійкості до антибіотика ампіциліну.
У зв’язку з протестами громадськості дослідники шукають способи видалення небажаних маркерних генів після здійснення трансформації.
Існує теоретична вірогідність, що трансгенні рослини можуть передавати спорідненим бур’янам, шляхом схрещування з ними, стійкість до гербіцидів, хвороб, засухи та інших несприятливих чинників. Внаслідок цього можуть утворитися так звані супер-бур’яни, з якими буде дуже важко боротися і які заполонять сільськогосподарські угіддя.
Всупереч існуючим побоюванням, вирощування та використання генетично модифікованих організмів у багатьох країнах зростає. Варто зауважити, що поки-що ніякого помітного шкідливого впливу на здоров’я людини, свійських тварин та взагалі на біосферу зафіксовано не було.
Етичні проблеми. Люди часто вважають, що через свій розум мають право переробляти інші організми заради власної користі. Проте останнім часом така антропоцентрична точка зору зазнає все більшої критики. Крім того, невідомо, чим може обернутися введення генів людини в геноми лабораторних тварин – така методика широко використовується нині для вивчення молекулярних механізмів багатьох хвороб людини.
Всупереч таким побоюванням, виведення генетично модифікованих тварин для потреб сільського господарства, фармакології та медицини – реалії нашого життя, і подальші зусилля генетиків мають бути спрямовані на гарантування безпечності трансгенних організмів для людини та біосфери.
Клонування вівці Доллі було неминучим наслідком прогресу, досягнутого в генетиці та біотехнології. Тепер з’явилася можливість створення безлічі ідентичних копій тварин з потрібними ознаками. Метод клонування може бути здійснений і стосовно людини, але тут з’являється значна етична проблема через непередбачувані біологічні та соціальні наслідки. Поки-що наукові дослідження в цьому напрямку заборонені.