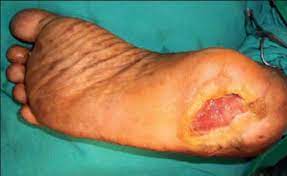
Профілактика хірургічної інфекції
Мета:
- вивчити основні положення асептики і антисептики (мал. 2);
- оволодіти методами оброблення рук і операційного поля.
Аж до XIX ст. хірурги не знали про існування мікробів і їх роль у розвитку гнійних процесів.
Операції виконувались нестерильними інструментами. Майже всі рани нагноювалися, у деяких хворих розвивався сепсис.
Створення і наукове обґрунтування асептики належить англійському хірургу Дж. Лістеру (1827— 1912 рр.). Ґрунтуючись на відкриттях Л. Пастера про причини розвитку бродіння і гниття, Лістер дійшов висновку, що причиною нагноєння ран є мікроби, які потрапили в них з повітря або занесені під час операції руками хірургів.
Під терміном «інфекція» розуміють реакцію організму люд ини на мікроорганізми, найчастіше мікроби. Під терміном «хірургічна інфекція» мають на увазі гнійно-запальні процеси в організмі людини, спричинені попаданням хвороботворних (гноєтворних) мікробів; такі процеси вимагають хірургічного лікування (фурункули, карбункули, флегмони тощо).
При вивченні хірургічної інфекції необхідно знати такі поняття, як:
- первинна інфекція — процес, що розвивається при первинному забрудненні рани;
- реінфекція — повторне забруднення на місці ліквідації первинної інфекції; суперінфекція —
- повторне зараження в умовах незавершеного інфекційного процесу, яке зазвичай перебігає агресивно.
Для попадання мікробів в організм потрібні «вхідні ворота», тобто порушення цілості покриву (шкіри, слизових оболонок).
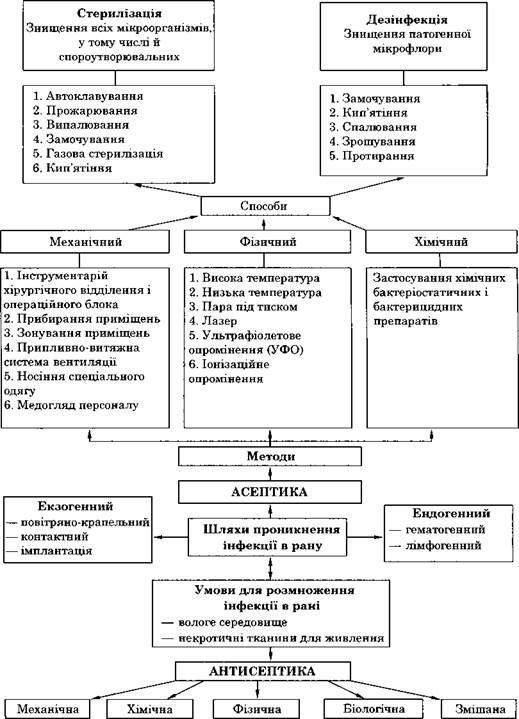
Мал. 2. Структурна схема теми «Профілактика хірургічної інфекції»
Хірургічна інфекція залежить від двох чинників:
від дози і вірулентності мікробів, що проникли в організм;
від захисних сил організму.
Що більш виражений перший чинник і менший другий, то сильніше розвивається інфекція.
В основі профілактики хірургічної інфекції лежить посилення захисних сил організму, зменшення забруднення шкіри і слизових оболонок мікрофлорою, а також попередження і своєчасне хірургічне оброблення ушкоджень.
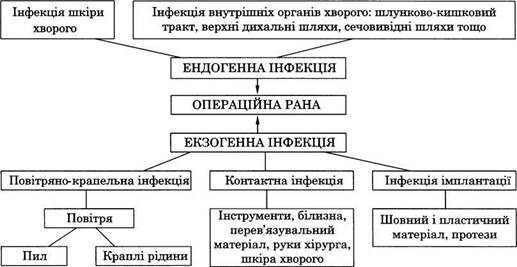
Для того щоб попередити попадання інфекції в рану, необхідно знати її основні джерела і шляхи поширення (мал. 3). Інфекція може потрапити двома шляхами: екзогенним і ендогенним.
Основні джерела екзогенної інфекції:
- повітря з часточками пилу, на яких осідають мікроорганізми;
- виділення з носової частини глотки (носоглотки) і верхніх дихальних шляхів
- хворих, відвідувачів і медперсоналу;
- виділення з гнійних ран;
- побутові забруднення.
У рану екзогенна інфекція може проникнути трьома основними шляхами: повітряно-крапельним; контактним; імплатаційним.
Джерело ендогенної інфекції знаходиться в організмі хворого (гноячкові захворювання шкіри, каріозні зуби, запалення мигдаликів, слизової оболонки дихальних шляхів тощо).
Збудники інфекції можуть бути занесені в рану як під час операції, так і в післяопераційний період кровоносними судинами (гематогенний шлях) і лімфатичними судинами (лімфогенний шлях).
У хірургії вироблена чітка система заходів, яка дає змогу зменшити небезпеку попадання мікробів у рану. Це досягається дотриманням методів асептики і антисептики, що є основою сучасної хірургії.
Внутрішньо лікарняна інфекція (госпітальна) — захворювання або ускладнення, розвиток яких пов’язаний з інфікуванням хворого під час знаходження в хірургічному стаціонарі.
Госпітальна інфекція має такі характерні особливості:
Її збудники стійкі до основних антибіотиків і антисептичних засобів. Це пов’язано з пасивуванням мікрофлори в умовах хірургічного стаціонару, де в повітрі, на поверхнях, в організмі хворих наявні низькі концентрації антимікробних засобів.
Збудниками є звичайні умовно-патогенні мікроорганізми, найчастіше стафілокок, клебсієла, кишкова паличка, протей тощо.
Виникає у ослаблених в результаті хвороби або операції пацієнтів, часто є суперінфекцією.
Часто виникають масові ураження одним штамом мікроорганізму, що виявляються схожою клінічною картиною захворювання (ускладнення).
ПРОФІЛАКТИКА ГОСПІТАЛЬНОЇ ІНФЕКЦІЇ
1. Скорочення передопераційного періоду.
2. Урахування при госпіталізації особливостей заповнення палат (в одній палаті повинні знаходитись хворі приблизно з однаковою тривалістю перебування в стаціонарі).
3. Раннє виписування з наглядом вдома.
4. Зміна антисептичних засобів і антибіотиків, використовуваних у відділенні.
5. Раціональне призначення антибіотиків.
6. За можливості — закриття хірургічних стаціонарів на провітрювання (1 міс на рік). Цей захід обов’язковий для гнійних відділень, а також при спалаху госпітальної інфекції.
Асептика (а — без, septicus — гниття) — метод роботи із запобіганням гниттю.
Асептика — це сукупність методів і прийомів роботи, спрямованих на попередження попадання інфекції в рану, організм хворого; створення безмікробних стерильних умов шляхом використання організаційних заходів, активних знезаражувальних хімічних речовин, а також технічних засобів і фізичних чинників.
У сучасній асептиці зберегли своє значення два основні принципи: усе, що стикається з раною, має бути стерильне;
хірургічні хворі мають бути поділені на два потоки: «чисті» і «гнійні».
Профілактика повітряно-крапельної інфекції
При повітряно-крапельному шляху поширення інфекції мікроорганізми потрапляють у рану з навколишнього повітря, де вони знаходяться на часточках пилу або в краплях виділень з верхніх дихальних шляхів чи ранового ексудату.
ОСОБЛИВОСТІ ОРГАНІЗАЦІЇ І ОБЛАШТУВАННЯ ХІРУРГІЧНОГО СТАЦІОНАРУ
Принцип дотримання правил асептики і антисептики лежить в основі організації хірургічного стаціонару. Це необхідно для профілактики ранової інфекції, створення необхідних умов для виконання операцій, обстеження і післяопераційного догляду за хворими.
ОСНОВНІ СТРУКТУРНІ ПІДРОЗДІЛИ ХІРУРГІЧНОГО СТАЦІОНАРУ
Приймальне відділення. Призначене для прийому, реєстрації, огляду, санітарно-гігієнічної обробки і транспортування хворих до лікувальних відділень.
Лікувально-діагностичні відділення. Особливості облаштування лікувально-діагностичних відділень хірургічного профілю підпорядковані правилам асептики і антисептики. При плануванні багатопрофільних лікарень враховують особливості контингенту хворих, устаткування хірургічних відділень, призначених для обстеження і лікування пацієнтів з певними захворюваннями. Виділяють спеціалізовані відділення (кардіохірургічні, урологічні, травматологічні, нейрохірургічні тощо) — це робить лікування ефективнішим і дає змогу запобігти можливим ускладненням.
Операційний блок. Найбільш чисте місце хірургічного стаціонару. Саме в операційному блоці необхідне найбільш суворе дотримання правил асептики. Операційний блок має розташовуватись окремо, у разі можливості виноситись у спеціальні прибудови, сполучені переходом з основним лікарняним комплексом. Для того щоб запобігти забрудненню повітря і приміщень у безпосередній близькості від операційної рани, при організації операційного блока дотримуються принципу зональності.
Існує 4 зони стерильності.
1. Зона абсолютної стерильності: операційна, стерилізаційна.
2. Зона відносної стерильності (суворого режиму): передопераційна, наркозна.
3. Зона обмеженого режиму: приміщення для зберігання крові, переносної апаратури, приміщення для чистої білизни.
4. Зона спільного режиму: кабінет завідувача, старшої операційної сестри, приміщення для брудної білизни.
Виділяють різні види операційних: планові і екстрені, чисті і гнійні.
Види прибирання:
1. Поточне — проводиться в ході операції.
2. Після кожної операції — виносяться всі відпрацьовані матеріали, протирається операційний стіл.
3. Завершальне (наприкінці робочого дня) — миються підлоги, стіни.
4. Попереднє (на початку робочого дня) — протираються горизонтальні поверхні.
5. Генеральне— 1 раз на тиждень операційна миється з використанням антисептичних розчинів.
Розділення потоків хворих. Розділення «чистих» і «гнійних» хворих — основний принцип асептики. Залежно від потужності стаціонару існують різні способи вирішення цієї проблеми.
МЕТОДИ БОРОТЬБИ З ІНФЕКЦІЄЮ У ПОВІТРІ
• Носіння масок. Маски використовуються медичним персоналом для запобігання потраплянню при диханні крапель секрету з носоглотки і ротової порожнини в зовнішнє середовище. Існують два типи масок: фільтрівні і відбивні. До фільтрівних належать марлеві маски. Тришарові маски затримують 70 % мікроорганізмів, що видихаються, чотиришарові — 88 %, шестишарові — 96 %. При зволоженні марлі її фільтрівна здатність знижується. Через 3 год 100 % тришарових масок значною мірою вже засіяні мікрофлорою. Носіння масок обов’язкове в операційній, перев’язувальній.
Бактерицидні лампи. Існують спеціальні лампи, які випромінюють ультрафіолетові промені. Промені з такою довжиною хвилі мають максимальний бактерицидний ефект. Одна лампа протягом 2 год стерилізує ЗО м3 повітря і знищує мікроорганізми на відкритих поверхнях.
Вентиляція. Провітрювання і вентиляція приміщень на ЗО % знижують забрудненість повітря мікроорганізмами.
Особиста гігієна хворих і медперсоналу. При поступленні в стаціонар хворі проходять через санпропускник в приймальному відділенні. Медперсонал повинен дотримуватись правил особистої гігієни, слідкувати за відсутністю у себе застудних і гноячкових захворювань.
Профілактика контактної інфекції
Зводиться до виконання одного з головних принципів асептики: «Усе, що стикається з раною, має бути стерильне».
З раною стикаються:
— хірургічні інструменти;
— перев’язувальний матеріал і хірургічна білизна; руки хірурга;
— операційне поле (шкіра самого хворого).
СПОСОБИ ПРОФІЛАКТИКИ
Дезінфекція. Комплекс заходів, спрямованих на зменшення кількості патогенних і умовно-патогенних для людини мікроорганізмів на інструментах і предметах зовнішнього середовища.
Стерилізація. Комплекс фізичних і хімічних способів повного знезараження медичних інструментів, приладів, апаратів тощо. Для цього використовують обпалення, пастеризацію, кип’ятіння, сухожаровий метод, автоклавування.
Профілактика інфекції при імплантації
Імплантація — впровадження з лікувальною метою в організм хворого штучних або чужорідних матеріалів і пристосувань.
Профілактика вимагає абсолютної стерильності всіх предметів, що контактують з організмом хворого, оскільки при імплантації є практично 100 % контагіозність і поширення інфекції.
Таким чином, будь-яке імплантоване тіло — можливе джерело так званої інфекції, що дрімає. Усі імплантанти мають бути стерильні, спосіб стерилізації визначається тим, з якого вони матеріалу. Основним джерелом імплантаційної інфекції є шовний матеріал, дренажі.
Основою асептики є стерилізація. Методи і засоби стерилізації мають забезпечувати знищення всіх, у тому числі стійких, мікроорганізмів — як патогенних, так і непатогенних. Найбільш стійкими є спори мікроорганізмів. Використовувані в практиці методи і засоби мають бути ефективними в плані бактерицидної і спороцидної активності, безпечними для хворих і медперсоналу і не повинні погіршувати робочі властивості інструментів.
У сучасній асептиці використовують:
І. Фізичні методи.
1. Термічна стерилізація:
• стерилізація парою під тиском (автоклавування);
• стерилізація гарячим повітрям (сухожарова).
2. Променева стерилізація.
II. Хімічні методи.
1. Газовий спосіб.
2. Стерилізація розчинами хімічних препаратів.
Такі поширені колись способи термічної стерилізації інструментів, як обпалення і кип’ятіння, зараз у хірургічній практиці не використовують. їх можна застосовувати в домашніх умовах за відсутності інших можливостей. Обпалення металевих інструментів проводиться відкритим полум’ям. Від кип’ятіння, яке довгий час було основним способом стерилізації інструментів, відмовились, оскільки при цьому досягається температура лише 100 °С, а її недостатньо для знищення спороутворювальних бактерій.
АВТОКЛАВУВАННЯ
При такому способі стерилізації діючим агентом є гаряча пара.
В автоклаві можливе нагрівання води при збільшеному тиску. Це підвищує точку кипіння води і, відповідно, температуру пари до 132,9 °С (при тиску 2 атм).
Існує два режими стерилізації:
- при тиску 1,1 атм і 120 °С — 45 хв (щадний режим);
- при тиску 2 атм і 132 °С — 20 хв (загальний режим).
Після закінчення стерилізації бікси якийсь час залишаються в гарячому автоклаві для просушування при трохи відкритих дверцятах. Вийнявши бікси з автоклава, закривають отвори в стінках біксів і позначають дату стерилізації (на прикріпленому до бікса шматочку церати). Закритий бікс зберігає стерильність інструментів, що знаходяться в ньому, протягом 72 год.
СТЕРИЛІЗАЦІЯ ГАРЯЧИМ ПОВІТРЯМ
Діючим агентом при цьому способі є нагріте повітря. Стерилізація здійснюється в сухожарових шафах-стерилізаторах при закритих дверцятах протягом 1 год при температурі 180 °С (загальний режим) і протягом 2,5 год при 160 °С (щадний режим).
ПРОМЕНЕВА СТЕРИЛІЗАЦІЯ
Антимікробне оброблення може здійснюватись за допомогою іонізаційного випромінювання (гамма-промені), ультрафіолетових променів і ультразвуку. Використовують, наприклад, ізотопи 137Cs.
Інструменти та інші матеріали стерилізують у герметичних упаковках; при цілості останніх можуть зберігатися до 5 років.
ГАЗОВА СТЕРИЛІЗАЦІЯ
Здійснюється в спеціальних герметичних камерах. Діючим агентом є пари формаліну (на дно камери кладуть пігулки формальдегіду) або етилен оксиду. Інструменти вважають стерильними через 6—48 год (залежно від компонентів газової суміші і температури в камері).
СТЕРИЛІЗАЦІЯ РОЗЧИНАМИ АНТИСЕПТИКІВ
Належить до холодних способів стерилізації і не призводить до затуплення інструментів, завдяки чому застосовується для оброблення ріжучих хірургічних інструментів. Для стерилізації можуть використовуватись три різні розчини: потрійний розчин (20 г формаліну, 10 г карболової кислоти, ЗО г соди і вода до 1 л);
96 % етиловий спирт;
6 % розчин пероксиду водню.
Для холодної стерилізації інструменти в розкритому або розібраному вигляді повністю занурюють в один із розчинів.
При замочуванні в спирті або потрійному розчині інструменти вважаються стерильними через 2—3 год, у пероксиді водню — через 6 год.
Стерилізовані інструменти, білизна тощо підлягають обов’язковому контролю. Контролюють як ефективність стерилізації, так і якість передстершгізаційного оброблення.
КОНТРОЛЮВАННЯ СТЕРИЛЬНОСТІ
Стерильність може перевірятись безпосередньо (бактеріологічне дослідження, проводиться раз на 7—10 днів) або непрямими методами (за допомогою тест-ампули).
КОНТРОЛЮВАННЯ ЯКОСТІ ПЕРЕДСТЕРИЛІЗАЦІЙНОГО ОБРОБЛЕННЯ
З цією метою використовують хімічні реактиви, за допомогою яких можна виявити на інструментах сліди невідмитої крові або залишки мийних засобів. Реактиви змінюють свій колір за наявності відповідних речовин (кров, лужні мийні засоби). Така перевірка проводиться після оброблення перед стерилізацією.
Для виявлення крові використовується бензидинова проба (амідопіринова); для виявлення слідів мийних засобів — фенолфталеїнова проба. Універсальною вважається ізопіранова проба.
ОБРОБЛЕННЯ ОПЕРАЦІЙНОГО ПОЛЯ
Заздалегідь проводиться санітарно-гігієнічне оброблення хворого (миття у ванні або під душем, заміна натільної і постільної білизни, гоління операційного поля сухим способом). На операційному столі поле обробляється хімічними антисептиками (йодонат 1 %, йодоперон 1 %, 70 % етиловий спирт, 2,4 % первомур).
При цьому слід дотримуватись таких правил:
широке оброблення;
послідовність від центра до периферії;
багатократність оброблення в ході операції (правило Гроссіха—Філончикова): шкіра обробляється перед обмеженням, після обмеження, безпосередньо перед розтином, періодично в ході операції, перед накладанням шкірних швів і після нього;
забруднені ділянки обробляються останніми.
ОБРОБЛЕННЯ ІНСТРУМЕНТІВ
Інструменти послідовно обробляють у два етапи: виконуються передстерилізація і безпосередньо стерилізація.
Вид і обсяг передстерилізації визначаються ступенем інфікованості інструментів, а спосіб стерилізації залежить від виду інструментів.
ПРОВЕДЕННЯ ПЕРЕДСТЕРИЛІЗАЦІЙНОГО ОБРОБЛЕННЯ
1. Знезараження. Використані інструменти в розкритому або розібраному вигляді занурюють у дезінфекційні засоби кімнатної температури. Як дезінфекційні засоби використовують: 3 % розчин хлораміну (експозиція 40—60 хв), 6 % розчин пероксиду водню (90 хв). Після знезараження інструменти промивають проточною водою до зникнення запаху хлору.
2. Миття. Інструменти занурюють у спеціальний мийний (лужний) розчин, до складу якого входять мийний засіб (пральний порошок), пероксид водню і вода. Температура розчину 50—60 °С, експозиція 20 хв. Потім кожний інструмент миють у цьому розчині протягом ЗО с, обполіскують у проточній воді, потім — у дистильованій і викладають на решітку.
3. Висушування. Може здійснюватись природним чином або в сухожаровій шафі при 80 °С до зникнення вологи.
ОБРОБЛЕННЯ РУК
Оброблення (миття) рук — дуже важлива процедура. Існують певні правила миття рук. Послідовно треба виконати механічну і хімічну (знежирення) обробку. Руки ретельно миють під краном щіткою і милом від кінчиків пальців до верхньої третини передпліччя. При цьому дотримуються принципу: «Не торкатись обробленими ділянками рук менш чистої шкіри і предметів».
Для подальшої обробки використовують антисептичні засоби. Вони повинні мати сильну антисептичну дію і бути нешкідливими для шкіри.
Розрізняють такі способи оброблення рук.
Класичні методи:
Спасокукоцького — Кочергина: здійснюється в двох тазах по 3 хв у 0,5 % розчині нашатирного спирту;
Альфельда — Фюрбрінгера та ін.: мають лише історичний інтерес і зараз не застосовуються.
Сучасні методи:
Бруно: руки обробляють протягом 10 хв 96 % етиловим спиртом за відсутності проточної води;
оброблення первомуром: здійснюється в одному тазу 2,4 % розчином протягом 1 хв;
оброблення хлоргексидином, дегміном, дегміцидом тощо.
Первомур готують так. У колбі змішують 171 мл ЗО—33 % пероксиду водню і 69 мл 100 % мурашиної кислоти; ставлять на 1 год у холодильник, періодично збовтуючи.
Потім доливають до 10 л дистильованою водою (тобто доливають 9 л 760 мл дистильованої води).
Термін «антисептика» ввів у 1750 р. англійський хірург Прінгл, описавши антисептичні властивості хініну.
Англійський хірург Дж. Лістер запропонував для боротьби з мікробами в операційній використовувати 2—3 % розчин карболової кислоти (розпилювали в повітрі операційної, обробляли ним руки, інструмент, перев’язувальний і шовний матеріал).
Антисептика (anti— проти, septicus — гниття) — це система заходів, спрямованих на знищення мікробів у рані, організмі з використанням активних хімічних речовин і біологічних чинників, а також механічних і фізичних методів.
Розрізняють такі види антисептики:
1. Механічна — знищення мікробів механічними методами (мал. 4):

туалет рани проводиться при перев’язуванні і при першій медичній допомозі — оброблення країв рани 1 % розчином йодонату, промивання пероксидом водню, висушування;
первинна хірургічна обробка (ПХО) ран — вона перетворює забруднену бактеріями рану на асептичну завдяки вирізанню країв, стінок і дна рани з видаленням мертвих тканин, згустків крові, сторонніх тіл;
вторинна хірургічна обробка інфікованої рани — у разі її інфікування (гнійна рана), видалення нежиттєздатних тканин, гною, розтин кишень, набряків; доки не зроблений розтин і не видалений гній, жодні антибіотики і антисептики не дадуть ефекту;
розтин гнійників (абсцесів, флегмон) або їх пункція (плевральна пункція при гнійному плевриті).
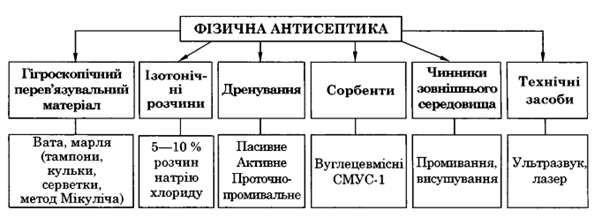
2. Фізична — знищення мікробів фізичними методами (мал. 5):
• дренування ран за допомогою тампонів, турунд з гігроскопічного матеріалу;
• укладати їх треба нещільно, функціонують 8 год, а потім стають перешкодою для відтоку;
• для поліпшення відтоку їх змочують гіпертонічними розчинами (10 % хлорид натрію, 25 % сульфат магнію), створюючи різницю в осмотичному тиску; використовують також гумові випускані, дренажі;
• використання сорбентів, які адсорбують на своїй поверхні мікроби і токсини; зазвичай це речовини на основі вуглецю у вигляді порошку або волокон; промивання, висушування (при опіках для утворення струпа постраждалих тримають у палатах з високою температурою і низькою вологістю);
• використання технічних засобів:
— ультразвуку при лікуванні гнійних ран; у рану наливають розчин антисептика і вводять наконечник приладу з низькочастотними ультразвуковими коливаннями; завдяки коливанню рідини поліпшуються мікроциркуляція і йонізація води, а це порушує окисно-відновні процеси в мікробній клітині (ультразвукова кавітація рани);
— лазерне випромінювання малої потужності (газовий вуглекислий лазер) впливає бактерицидно на стінки гнійної рани;
— рентгенотерапія для придушення інфекції в невеликих осередках (кістковий панарицій, гідраденіт).
3. Хімічна антисептика — знищення мікробів у рані, патологічному осередку або організмі за допомогою хімічних речовин (мал. 6).
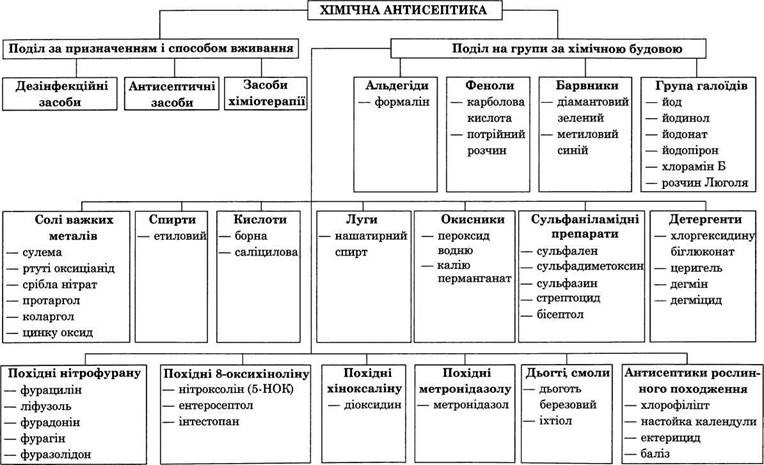
Класифікація хімічних антисептиків
1. За призначенням і способом вживання:
• для оброблення інструментів, предметів догляду, миття стін, підлог;
• зовнішні — для оброблення шкіри, промивання ран, слизових оболонок, оброблення рук;
• засоби хіміотерапії — вводяться всередину, діючи резорбтивно в організмі.
2. За хімічною будовою:
• група галоїдів:
– 1—5—10 % спиртові настойки йоду;
– 1 % йодинол для промивання ран;
– 1 % йодонат і йодопірон — органічні сполуки йоду;
– повідонйодин (0,1—1 % вільного йоду) — органічні сполуки у вигляді аерозолю;
– водний або спиртовий розчин Люголя для стерилізації кетгуту;
– 1—3 % розчини хлораміну Б;
• спирти 96 % і 70 %;
• альдегіди (формалін);
• феноли (потрійний розчин);
• барвники (1—2 % діамантовий зелений, 1—2 % спиртовий метиловий синій (може бути водний розчин));
• кислоти (саліцилова, 2—4 % борна); луги (нашатирний спирт);
• окисники (3 % розчин пероксиду водню, перманганату калію);
• детергенти (поверхнево-активні речовини) — хлоргексидину біглюконат, дегмін, дегміцид;
• похідні нітрофурану (фурацилін 1:5000, лифузоль (аерозоль), уроантисептики (фурадонін, фуразолідон, фурагін));
• похідні 8-оксихіноліну (5-НОК, ентеросептол, інтестопан); похідні хіноксаліну (0,1 % розчин діоксидину внутрішньовенно краплинно); похідні нітроімідазолу — метронідазол (трихопол); смоли, дьогті — дьоготь березовий, іхтіол, нафталан;
• антисептики рослинного походження — хлорофіліпт, календула, ектерицид, баліз;
• сульфаніламідні препарати — бактеріостатичний ефект за термінами дії, комбіновані (бісептол).
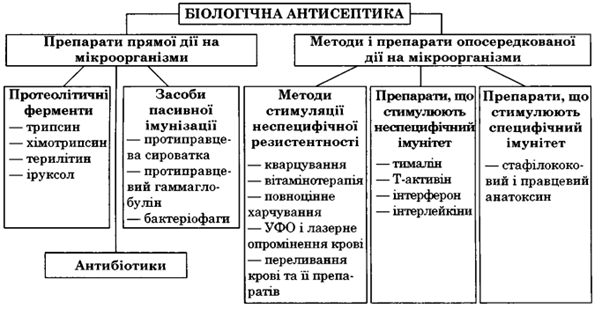
4. Біологічна антисептика (мал. 7).
Речовини біологічного походження, які безпосередньо впливають на мікроби, — біологічні антисептики прямої дії. Вони розсмоктують некротичні тканини, розріджують гній, діють протизапально, очищаючи рани від некротичних тканин і мікробів:
• протеолітичні ферменти тваринного походження: трипсин, хімотрипсин, хімопсин (їх виготовляють із підшлункової залози великої рогатої худоби); терилітин — продукт життєдіяльності плісеневого грибка;
• іруксол — мазь, до складу якої входить левоміцетин.
Засоби пасивної імунізації:
— ППС і протиправцевий гаммаглобулін для профілактики і лікування правця; протигангренозна сироватка;
— бактеріофаги: антистафілококовий, антистрептококовий, використовують місцево для промивання і лікування гнійних ран;
антистафілококова гіперімунна плазма — це нативна плазма донорів, імунізованих стафілококовим анатоксином; антисиньогнійна гіперімунна плазма.
Біологічні антисептики опосередкованої дії стимулюють спроможність організму хворого знищувати мікроорганізми.
Методи стимуляції неспецифічної резистентності: УФО, вітамінотерапія, повноцінне харчування покращують функцію імунної системи;
ультрафіолетове і лазерне опромінення крові (екстракорпоральне і внутрішньосудинне);
вживання препаратів ксеноселезінки (проводять перфузії через селезінку або готують з неї суспензії);
переливання крові та її препаратів, перш за все плазми і суспензії лімфоцитів.
Речовини, які стимулюють неспецифічний імунітет:
препарати загруднинної залози (тималін, Т-активін) великої рогатої худоби, продигіозан, левомізол, лізоцим, інтерферон, інтерлейкіни.
Препарати для стимуляції активного специфічного імунітету:
• вакцини, стафілококові і правцеві анатоксини.
5. Змішана антисептика.
Поєднує в собі різні види антисептики.