Шлунок ендоскопія
Анатомія і фізіологія
У шлунку розрізняють передню і задню стінки та малу і велику кривини. На малій кривині, ближче до виходу зі шлунка, є вирізка, де ділянки малої кривини сходяться під більш або менш гострим кутом, – кут шлунка. По поздовжній осі шлунка виділяють такі його основні частини:
кардія – верхньою її межею є EGJ, нижньою – кардіальна складка;
дно (або склепіння) шлунка міститься зліва від кардії, відмежоване від неї кутом Гіса;
тіло шлунка – найбільш містка частина шлунка, яка власне вкрита слизовою фундального типу, що забезпечує шлункову секрецію. У дистальному відділі тіло переходить в антральну частину, де складчастість втрачається. У тілі виділяють ділянку кута;
антральна частина – antrum piloricum, що проксимально межує з тілом, а дистально – з воротарем. В антральному відділі виділяють препілоричну ділянку – 0,5-2 см перед воротарем;
пілоричний канал – це сам пілорус та по 0,5 см з боку шлунка та дванадцятипалої кишки (ДПК).
Топографічно шлунок міститься в епігастральній ділянці, більшою частиною зліва від серединної лінії. При наповненні велика кривина проектується в пупкову ділянку.
Кардія розміщена зліва від хребта позаду хряща VII лівого ребра, його проекція відповідає XI грудному хребцю. Склепіння досягає нижнього краю V ребра по сосковій лінії.
Воротар порожнього шлунка лежить справа від серединної лінії напроти VIII реберного хряща, що відповідає I поперековому хребцю. Наповнений шлунок угорі контактує з нижньою поверхнею лівої частки печінки і лівим куполом діафрагми, ззаду – з верхнім полюсом лівої нирки і наднирником, з селезінкою та передньою поверхнею підшлункової залози, внизу – з брижею поперечної ободової кишки і самою кишкою. Середня довжина шлунка – 21-25 см.
Стінка шлунка складається зі слизової оболонки з добре розвинутою підслизовою основою, мʼязової і серозної оболонок.
Слизова оболонка має різну гістологічну будову і вигляд у різних частинах шлунка, вона містить три види залоз:
- кардіальні;
- шлункові залози (glandulae gastricae propriae) – численні (до 100 на 1 мм2), містяться у дні і тілі шлунка (інша назва – «фундальні»). Їх головні клітини виділяють пепсиноген, а обкладочні – соляну кислоту. У залозах цього типу також є ендокринні, у т. ч. ентерохромафінні клітини;
- пілоричні залози складаються тільки з головних клітин, виробляють слиз. Крім того вони містять ендокринні клітини, які секретують гастрин (G-клітини), соматостатин (D-клітини) та інші пептидні гормони.
Відповідно, гістологічно виділяють кардіальний тип слизової, фундальний і антральний типи (останній гістологічно подібний до кардіального).
Мукоцити, які містяться між залозами, продукують глікопротеїни (муцин) і гідро-карбонатіон. Крім того слизова оболонка містить поодинокі лімфатичні фолікули і численні ендокринні й ентерохромафінні клітини. Захисними від кислоти чинниками є муцини слизу (на поверхні слизу рН 1-2, під ним 6-7), поверхневі мембрани епітелію і зʼєднання між клітинами, а також трефоїлові пептиди слизівки.
Слизова оболонка тіла шлунка зібрана у складки, це забезпечує тісний контакт з їжею та ліпше її просочування соком. Складчастість забезпечується наявністю добре розвинутої власної мʼязової пластинки слизової оболонки і рихлої підслизової основи. Уздовж малої кривини складки мають поздовжній напрям, при скороченні шлунка ця ділянка стає каналом, по якому рідка їжа стікає до воротаря. Крім складок слизова оболонка має круглі підвищення діаметром 1-6 мм – шлункові поля, на поверхні яких видно численні дрібні отвори шлункових ямок, у ці ямки відкриваються шлункові залози.
Треба вказати, що слизова антрального типу по малій кривині поширюється в середньому на 8-9 см (максимально – на 15 см), по великій кривині – на 7-8 см (максимально – на 20 см).
Мʼязова оболонка шлунка містить три шари – зовнішній поздовжній, середній – циркулярний (сильніше виражений) і внутрішній – косий. Косі волокна петлеподібно охоплюють кардіальний отвір, утворюють в цьому місці опорну петлю і косо спускаються до великої кривини по передній і задній поверхні. При скороченні вони підтягують велику кривину до кардіального отвору.
Серозна оболонка вкриває майже весь шлунок, за винятком невеликої ділянки задньої поверхні зліва від кардії.
Моторика шлунка
Після надходження їжі у шлунок його дно і верхня частина розслаблюються (адаптивна релаксація), потім починається перистальтика у дистальному відділі тіла, змішування і подрібнення їжі. Надалі невеликі напіврідкі порції надходять у ДПК. Рецептивна релаксація стимулюється блукаючим нервом після ковтання, рухів глотки і стравоходу.
Перистальтичні рухи стрімко поширюються до пілоричної частини. Кожна хвиля спричиняє скорочення дистальної частини (антральні систоли), які можуть тривати до 10 с.
Такі хвилі відзначають 3-4 рази за хвилину. За скороченнями антруму настають послідовні скорочення пілоричного каналу і ДПК. В антральній частині особливо сильні скорочення зціджують (тонким струменем) напіврідку їжу у дванадцятипалу кишку, але затримують тверді маси, маятникоподібно скеровуючи їх у тіло, де вони подрібнюються.
У нормі дуоденогастрального рефлюксу (ДГР) не відбувається завдяки тому, що скорочення пілоричного каналу триває довше, ніж скорочення ДПК, а також через стимулювання холецистокініном і секретином пілоричного сфінктера.
Ентерогастральний рефлекс з ДПК починається з осморецепторів на стінках ДПК.
Потрапляння білкової їжі у ДПК і розтягнення її просвіту через ентерогастральний рефлекс стимулюють перистальтику шлунка. Натомість жири її пригнічують. У пригніченні випорожнення шлунка бере участь пептид YY. Найшвидше зі шлунка евакуюється вуглеводна їжа, повільніше – білкова, найповільніше – жирна.
Секреція шлунка
Секреція стимулюється мозковими впливами як за рахунок умовних рефлексів (вигляд їжі тощо), так і через рефлекси від їжі у ротовій порожнині. Мозкові впливи зумовлюють від 1/3 до половини секреції. Стимуляторами секреції є також гіпоглікемія, алкоголь і кофеїн, а також гнів. Натомість депресія і страх зменшують секрецію.
Шлунковий вплив. Іжа у шлунку збільшує секрецію через розтяг шлунка і подранення амінокислотами та спорідненими продуктами. Волокна від рецепторів ідуть до підслизового сплетення, а звідти до постгангліонарних парасимпатичних нейронів, синапси яких є на парієтальних клітинах. Така відповідь є місцевим рефлексом. Продукти травлення білків також збільшують секрецію гастрину.
Кишковий вплив. Жири, вуглеводи і кислота у ДПК інгібують секрецію кислоти шлунком та шлункову моторику за рахунок нейрогуморальнихмеханізмів: ентерогастроном (гормоном, що пригнічує секрецію), вірогідно, є пептид YY.
Ендоскопічна картина шлунка у нормі
Залежно від будови тіла шлунок може мати різноманітну форму («гачок», «ріг» тощо) і положення (поздовжнє, поперечне). Більшість таких варіантів не мають суттєвого значення для ендоскопіста.
Кардія є тубулярною структурою, подібною до стравоходу, з поздовжніми складками, які візуально виглядають продовженням складок термінального відділу страво ходу: судинний рисунок, як звичайно, відсутній. Обовʼязковим є огляд кардії у ретрофлексії з оцінкою стану кардіальної складки (див. стор. 9). При роздуванні слизова кардіальної складки розправляється, однак іноді при надлишковій слизовій поздовжні складки утримуються – їх необхідно диференціювати від патологічних змін на підставі еластичності і розтягування при інструментальній пальпації.
Дно (склепіння) шлунка. Після проходження кардії та роздування шлунка можна оглянути проксимальну частину тіла і дно шлунка. В U-ретрофлексії дно виглядає як округла заглибина проксимальніше від кардіальної складки. Щодо кардії воно розміщене зліва і спереду. На відміну від тіла, у дні шлунка у нормі може бути видно рисунок капілярів слизової і підслизових вен, їх виявлення лише в цій ділянці ще не свідчить про атрофічний гастрит. На відміну від патологічних, варикозно розширених вен, ці судини прямі, а їх діаметр не перевищує 2-3 мм. Звертають у вагу на вміст – «слизове озерце» у ділянці склепіння шлунка (за умови огляду на лівому боці). У нормі – це сірувато-білий вміст зі слиною, допустима невелика домішка жовчі, клінічна значущість якої досі не визначена.
Тіло шлунка. Має більш-менш конічну форму зі звуженням у бік кута. Для тіла характерні типові складки, найбільш виражені на великій кривині і прилеглих ділянках передньої і задньої стінок. Складки звивисті, створюють враження сітки, при роздуванні розпрямляються і стають плоскішими. На малій кривині складки поздовжні, при роздуванні можуть повністю розгладитися. Вважають, що нормальна висота складок – 4-5 мм, складки заввишки 5-10 мм називають «випнутими» (prominent), а понад 1 см – «великими» (large). Такі їх зміни можуть бути спричинені як гіпертрофією, так і пухлинним процесом.
Доволі частим анатомічним варіантом є каскадний шлунок (інша назва – у формі пісочного годинника – «клепсидри»), у таких випадках склепіння утворює кишеню, в яку спрямована оптична вісь при вході у шлунок. Ця кишеня відділена від тіла (задньої його стінки) більш чи менш вираженим гребенем. Такий анатомічний варіант може створювати суттєві технічні труднощі при введенні ендоскопа у тіло шлунка. У такому разі в тіло шлунка ендоскоп треба проводити по передній стінці, починаючи від кардії.
У нормі слизова оболонка рожевувато-червоного («лососевого») кольору. Він залежить від ступеня васкуляризації і розтягу, а також від потужності і типу лампи освітлювача (її спектра). Суцільний, рівномірний шар слизу зумовлює нормальний блиск.
Судинний рисунок, як звичайно, при роздуванні видно в кардіальній ділянці, у дні й антральному відділі. При максимальному роздуванні його можна бачити і в тілі шлунка (це імітує атрофію). Поверхня слизової дрібнозерниста за рахунок припіднятих шлункових полів, розділених світлішими lineae gastricae. При докладному ендоскопічному огляді нормальної слизової оболонки тіла шлунка видно характерний рисунок з рівномірно розміщених дрібних червоних крапок, утворений збираючими венулами – RAC. При збільшення буде такох видно капіляри, які оточують шлункові ямки.
Кут шлунка має вигляд дуги по малій кривині, для ділянки кута характерна поступова втрата складчастості. Слизова оболонка цієї ділянки така ж або дещо червоніша, ніж у тілі. Кут є одним з основних ендоскопічних орієнтирів при гастроскопії. При огляді в інверсії кут має вигляд симетричної поперечної складки завтовшки 5-10 мм з гладкою поверхнею. При описі топографії уражень у тілі візуально виділяють ділянку кута шлунка.
Антральний відділ шлунка має форму воронки, верхівкою якої є воротар. Довжина цього відділу коливається від 3 до 10 см. Складчастість, типова для тіла, тут втрачається, слизова оболонка гладка, колір варіабельний – від жовтувато-сірого до червонувато-оранжевого.
Препілорична ділянка (0,5-2 см перед воротарем) відзначається суттєвою варіабельністю складчастості. Приблизно в 10% пацієнтів у препілоричній ділянці можуть спостерігатися збільшені складки (понад 5 мм заввишки і понад 1 см завширшки). Один з варіантів – аркоподібна складка по малій кривині, інший – поздовжні складки. Самі по собі вони ще не свідчать про патологію, однак часто трапляються у поєднанні з ерозованими папулами антрального відділу. Необхідно також враховувати можливість наявності інфільтративних пухлин.
В антрумі іноді можна виявити одиничні фіксовані поперечні складки (з частотою 1-2%), вони можуть бути асимптомними знахідками, проте часом супроводжуються диспептичною симптоматикою. Циркулярні складки – кільця трапляються з частотою до 0,5%, здебільшого безсимптомні. Лише коли отвір менший за 5-10 мм, то вони можуть спричинити порушення евакуації. Таке кільце може бути помилково розцінене як воротар (псевдопілорус).
Пілоричний канал – округлий отвір, слизова якого може бути гладка або зі складками. Довжина каналу в середньому 1,5 см, ширина відкритого воротаря 1-1,5 см.
Він може бути як по центру антрального відділу, так і зміщений в бік малої чи великої кривини, відзначається суттєвими змінами вигляду відповідно до перистальтики. У момент проходження перистальтичної хвилі воротар зімкнутий, облямований випнутими радіальними складками. Зяючий воротар часто супроводжується дуоденогастральним рефлюксом або патологією цибулини ДПК, проте може бути і випадковою знахідкою, яка не супроводжується симптоматикою.
Варіанти анатомії шлунка
Дивертикули шлунка, як звичайно, є вродженими, містять усі шари стінки шлунка і локалізуються у дні або на задній стінці у верхній третині тіла шлунка.
Аберантна (додаткова, ектопічна) підшлункова залоза. Рідкісний утвір, який за розмірами рідко перевищує 1 см, має вигляд протрузії з центральним втягненням (може містити протоку, яка закінчується сліпо, а також ацинарну і острівцеву тканини), форма її варіабельна. Міститься переважно в антральному відділі шлунка по великій кривині.
Сторонні тіла шлунка
На відміну від стравоходу, сторонні тіла шлунка – переважно випадково або навмисне проковтнуті нехарчові предмети. Видаленню підлягають сторонні тіла розмірами понад 4 × 1 см, гострі предмети (голки, леза) та батарейки. Менші предмети, як звичайно, виходять природним шляхом.
Другу групу становлять безоари – щільні грудки з непертравлюваних речовин різного походження – з рослинних волокон, наприклад, хурми (фітобезоари), волосся (трихобезоари – синдром Рапунцеля). Казуїстичними є безоари іншого походження – зі смол (піксобезоари), шелаків тощо. Утворенню безоарів сприяє порушення секреції та евакуації зі шлунка – атрофічний гастрит, гастропарез при діабетичній нейропатії, перенесені операції (резекція шлунка, ваготомія). У таких хворих можуть утворюватися безоари із залишків їжі (food boli) та фармакобезоари (скупчення таблеток), у хворих із безоарами часто виявляють виразки шлунка.
Зміни слизової шлунка
При інтерпретації та описі змін слизової оболонки шлунка згідно з MST необхідно розрізняти еритематозну і застійну слизову оболонку. Еритема визначається як локальне чи дифузне почервоніння слизової оболонки, а застійна слизова оболонка – це комбінація еритеми з набряком. Вирішено, що термін «гіперемія» – це еквівалент «еритеми», а «набряк» – еквівалент «застійної слизової оболонки». Окрім того змінену слизову оболонку характеризують як зернисту, вузлувату, атрофічну, раниму, геморагічну.
Зміни слизової можуть бути локальними, вогнищевими або дифузними.
Прийом концентрованого алкоголю (особливо сурогатних напоїв) призводить до прямого ушкодження мікроциркуляторного русла слизової, судинного застою і, відповідно, до застійної гастропатії та геморагій.
Складки тіла шлунка можуть бути згладжені (при атрофії слизової) або збільшені, у тому числі гігантські. Подібно до змін поверхні слизової оболонки, зміни складок можуть бути локальними і дифузними. Збільшені складки зі збереженою пластичністю можна виявити при гастриті з гіперсекрецією, портальній гастропатії, гострих реактивних гастритах і гастропатіях або вони взагалі можуть не свідчити про патологію. Натомість гігантські складки, які не сплощуються при роздуванні, можуть бути наслідком як гіперплазії – хвороба Менетріє, залозиста гіперплазія при синдромі Золлінгера-Еллісона, гіперпластична гіперсекреторна гастропатія Шиндлера, еозинофільний гастрит, так і інфільтративних змін (інфільтративний рак або лімфома шлунка). Характерна риса нормальних шлункових складок – пластичність. При роздуванні вони стають плоскішими і прямішими. При пальпації біопсійними щипцями вони мʼякі і під час спроби взяти біопсію тягнуться за щипцями. Ригідність і крихкість (легка фрагментація – слизова не тягнеться за щипцями) при взятті матеріалу для біопсії наводять на думку про злоякісну пухлину. Проте для підтвердження інфільтративної карциноми або й гастропатії Менетріє щипцева біопсія часто неінформативна – необхідна петлева біопсія на всю товщу слизової.
Хвороба Менетріє
Хвороба Менетріє (Menetrier’s) – рідкісне набуте захворювання з ураженням дна і тіла шлунка, яке характеризується гігантськими гіперпластичними складками, гастропатією із втратою протеїну, посиленою секрецією муцину, гіпохлоргідрією, гіпоальбумінемією. Недавні дослідження засвідчили в таких хворих гіперпродукцію трансформуючого фактору росту-а з активацією рецепторів епідермального фактору росту.
Відтак відбувається експансія проліферативного компартменту. Гістологічно виявляють фовеолярну гіперплазію, кістозну дилятацію ямок, зменшення кількості головних і парієтальних клітин. У патогенезі припускають участь цитомегаловірусу.
Рефлюкс-гастрит. Синонім – «лужний гастрит». Багато сучасних морфологів зараховують це ураження до гастропатій через слабку вираженість запальних змін. Особливо виражена у хворих, які перенесли оперативні втручання на шлунку. Причиною є пошкодження епітелію жовчними кислотами, які мають детергентні властивості. Слизова гіперемована або застійна, можуть бути субепітеліальні петехії.
Класифікація гастритів
Модифікована (Хʼюстон, 1996) міжнародна Сіднейська класифікація гастритів передбачає у формулюванні діагнозу поєднання топографічної, гістологічної та етіологічної характеристик.
| Тип гастриту | Етіологічний фактор | Синоніми гастриту |
|---|---|---|
| Неатрофічний | Helicobacter pylori ? Інші причини | Поверхневий, дифузний антральний, хронічний антральний, інтерстиціальний фолікулярний, гіперсекреторний, тип В* |
| Атрофічний Автоімунний | Автоімунний процес | Тип А*, дифузний тіла шлунка, асоційований з перніціозною анемією |
| Мультифокальний | H. pylori, дієтичні фактори, ? фактори довкілля | Тип В*, тип AB*, метапластичний |
| Особливі форми Хімічний** | Хімічне подразнення Жовч НСПЗП ? Інші чинники | Реактивний реолюкс НСПЗП-асоційований Тип С |
| Радіаційний | Променеві ураження | |
| Лімфоцитарний | Ідіопатичний, ? імунні механізми, глютен, медикаменти (тиклопідин), H. pylori | Варіолоформний (ендоскопічно), асоційований з целіакією |
| Неінфекційний гранульоматозний | Ізольований гранульоматоз | Хвороба Крона, саркоїдоз, гранульоматоз Вегенера (та інші васкуліти), сторонні тіла/речовини, ідіопатичний |
| Еозинофільний | Харчова алергія, ? інші алергени | Алергічний |
| Інші інфекційні гастрити | Бактерії (відмінні від H. pylori), віруси, грибки, паразити | Флегмонозні зміни |
** Для станів, спричинених хімічними пошкодженнями, часто рекомендують термін «гастропатія» замість «гастрит».
Для обʼєктивізації оцінки вираженості запальних змін Хʼюстонська модифікація Сіднейської системи містить візуально-аналогову шкалу з еталонами напівкількісної оцінки морфологічних змін. Найточнішу картину отримують при аналізі не менш ніж 5 біоптатів: по два з тіла (мала кривина – на 4 см проксимальніше кута і велика – приблизно 8 см від EGJ) та антруму (2-3 см від воротаря по малій і великій кривині), а також з ділянки кута шлунка.
Оцінка важкості морфологічних змін слизової шлунка
Автоімунний гастрит повʼязаний з утворенням антитіл проти парієтальних клітин і внутрішнього фактору Кастла, наявний також Т-клітинний компонент захворювання.
Це порівняно рідкісне захворювання частіше трапляється в осіб з іншими імунними розладами (хвороба Грейвса, мікседема, тироїдит тощо).
Нині виділяють кілька основних патогенетичних механізмів Н. pylori-асоційованих захворювань:
- пряма дія на слизову оболонку та секреція токсинів;
- непряма дія через модуляцію гомеостазу шлункової секреції – зміни секреції гастрину, пепсиногену і кислоти;
- порушення сигнальних механізмів епітеліоцитів;
- активація клітин запалення і викид медіаторів запалення;
- H. pylori-стимульовані автоімунні реакції.
Первинним морфо-клінічним наслідком інфекції Н. pylori (Hp) є гастрит, із його характером і важкістю повʼязані як інші наслідки інфекції (пептичні виразки, аденокарцинома, MALT), так і наявність клініки взагалі – при наявності бодай мінімальних запальних змін у всіх інфікованих у переважної більшості колонізованих осіб симптоматика відсутня.
Пацієнти з переважно антральним гастритом – найчастішою формою Н.pylori-acoційованого гастриту (принаймні в більшості країн) мають схильність до утворення дуоденальних виразок. Гастрит з переважним ураженням антруму превалює у більшості країн, принаймні в Європі. Характерна інфільтрація lamina propria антруму лімфоцитами і плазматичними клітинами, особливо поверхнево. У глибині слизової виявляють великі лімфоїдні агрегати і фолікули, атрофія залоз із їх заміщенням фіброзною тканиною, як звичайно, відсутня або слабко виражена. Майже завжди наявна інфільтрація поліморф ноядерними нейтрофілами, яка віддзеркалює «активність» запалення. Колонізація H.pylori слизової, як звичайно, щільна і в пацієнтів з дуоденальними виразками вираженіша, ніж при невиразковій диспепсії чи виразках шлунка. Характерна різка різниця з колонізації антруму і тіла шлунка. У відповідь на запалення антруму незаселена Н.pylori слизова оболонка тіла шлунка зі збереженими залозами реагує підвищеною кислотопродукцією. Однак чітко розмежувати антральний і мультифокальний атрофічний гастрит важко – до 15% хворих із дуоденальними виразками мають суттєву атрофію і кишкову метаплазію слизової шлунка.
Гастрит з переважним ураженням тіла і мультифокальною атрофією несе в собі ризик виникнення виразок шлунка, атрооії слизової оболонки, кишкової метаплазії і карциноми шлунка. При гастриті з ураженням тіла шлунка кількість парієтальних клітин може бути нормальною, але їх функція пригнічена, після ерадикації Н. руогі вона відновлюється, якщо ураження було не надто важким. Серед факторів, які спричиняють пригнічення кислотопродукції, називають IL-1β, що інгібує викид гістаміну. Частка мультифокального атрофічного гастриту зростає з віком/тривалістю хвороби – приблизно на 1,2-1,9% на рік захворювання. Атрофія спочатку більш виражена в антрумі, ділянці кута, з часом мультифокальна атрофія поширюється на тіло. Із прогресуванням запалення, атрофії і метаплазії «фронт» між слизовою оболонкою фундального і пілоричного типу рухається в оральному напрямі, що сприяє заселенню Н. руlori тіла шлунка.
Колонізації тіла шлунка сприяє також тривалий прийом кислотознижуючих препараьтів (наприклад, при гастроезофагальній рефлюксній хворобі або тривалому прийомі НСПЗП). За таких умов запалення антруму зменшується, а тіла шлунка – посилюється.
Шанси розвитку атрофічного гастриту залежать від низки чинників з боку Нр і організму хазяїна, морфологічно це проявляється важкістю запалення з більшою ймовірністю руйнування залоз. При інфекції штамами CagA+ і тими, що містять ліпополісахарид який імітує Lewis × і у антигени, атрофія розвивається швидше. Крім генетичних чинників з боку організму хазяїна (HLA тип) розвитку атрофічного гастриту сприяють куріння та дефіцит вітаміну С.
| Для ендоскопічного заключення рекомендуються такі терміни: | Додаткові заключення |
|---|---|
| Гастропатія: Ерозивна Еритематозна (гіперемія) Гіпертрофічна Геморагічна Атрофія слизової оболонки шлунка Портальна гіпертензивна гастропатія Виразка шлунка Кривавляча виразка шлунка Пептична виразка анастомозу Злоякісна пухлина; якщо доречно – рак шлунка Поліпи | Ангіоектазія Доброякісна пухлина Кровотеча невідомого походження (джерело не виявлене) Виразка Дьєлафуа* Дивертикул Ранній рак шлунка Стиснення ззовні Нориця Стороннє тіло Гастростаз Helicobacter pylori Папульозна гастропатія Паразити Ознаки перенесеної операції (стан після …) Рубець Підслизова пухлина Варикозні вени |
При формулюванні ендоскопічного заключення слід лише вказувати підозру на гастрит, оскільки це морфологічний діагноз, який встановлюється на підставі множинної біопсії з різних ділянок. Подібна ендоскопічна картина може бути спричинена різним морфологічним субстратом, у тому числі й дистрофічними змінами без суттєвого запального компонента – гастропатією різної етіології.
Ерозії
У термінології, запропонованій OMED, використовували термін «афта» замість «ерозія». Після тривалого обговорення було вирішено використовувати термін «ерозія» для мінімальної термінології. «Ерозія» – це невеликий поверхневий дефект слизової з рівними краями, переважно вкритий ексудатом білого чи жовтого кольору, глибина якого не виходить за межі власної мʼязової пластинки слизової оболонки. Розміри ерозій коливаються від точкових до 1 см в діаметрі. Вона може кровоточити і в такому випадку термін «ерозія» можна використовувати тільки при видимій слизовій оболонці, не прикритій згустком крові. В антрумі ерозії можуть створювати лінійний рисунок уздовж складок до воротаря. Генез ерозій різноманітний – інфекція Н. pylori, прийом НСПЗП та інших токсичних середників, стресові ураження тощо.
Для папульозної (варіолоформної) гастропатії характерна наявність хронічних ерозій на припіднятій основі (папулах) у вигляді кратерів. Гістологічно такі папули відзначаються активним запаленням, гіпертрофією ямкового епітелію та пілоричних залоз, у частини хворих – лімфоцитарним гастритом. Дно хронічних ерозій відзначається фібриноїдним некрозом, однак він не виходить за межі lamina propria, такі ерозії можуть персистувати упродовж кількох років, папули утримуються довгий час після епітелізації ерозій. Патогенез їх не зʼясовано, як і співвідношення з колонізацією Н. руlori. Характерна картина рядів папул з верхівковими ерозіями або без них в антральному відділі шлунка в напрямку до воротаря.
НСПЗП-асоційована гастропатія
Причиною хронічного ураження слизової при прийомі нестероїдних протизапальних препаратів (НСПЗП) є блокування конститутивної форми циклооксигенази ЦОГ-1 і зниження синтезу простагландинів, а відтак порушення кровоплину у слизовій, зменшення продукції слизу і збільшення агресивності шлункового соку. Більшість НСПЗП мають властивості слабких кислот, тому накопичуються у слизовій шлунка у концентрації, достатній для порушеня окисного фосфорилювання. Підслизові геморагії і дрібні ерозії виявляють у 2/3 пацієнтів, які приймають традиційні НСПЗП, переважно вони виникають у перший місяць лікування і здебільшого мають безсимптомний перебіг, у більшості хворих такі ураження з часом зникають, однак у частини пізніше виникають гострі виразки.
Крім того, багато НСПЗП, а особливо аспірин, ушкоджують фосфоліпідзалежний гідрофобний барʼєр, що призводить до посилення зворотної дифузії іонів водню; аспірин має також місцевий пошкоджуючий вплив на слизову. Для викликаних аспірином пошкоджень слизової шлунка найхарактернішими є поверхневі ерозії з дном, вкритим фібрином, у препілоричній ділянці (можливе й ураження інших ділянок), можуть також бути глибші ураження – «штамповані» виразки, а також вогнища еритеми, розділені нормальною слизовою.
Виразки шлунка
Виразки – це дефекти слизової, які поширюються у глибину крізь muscularis mucosae у підслизовий шар і навіть глибше. Причиною переважної більшості пептичних виразок шлунка нині вважають колонізацію шлунка Н. pylori – до 70%. Друге місце посідають НСПЗП – пептичні виразки трапляються у 25% пацієнтів, які тривалий час отримують НСПЗП, причому в 15% утворюються виразки шлунка і лише в 10% – виразки дванадцятипалої кишки. Треба зазначити, що НСПЗП не лише спричиняють утворення гострих уражень слизової, а й сповільнюють загоєння хронічних виразок. Лише порівняно невелика кількість виразок є так званими ідіопатичними (викликаними гіперсекрецією, судинними причинами тощо).
Виразки шлунка переважно поодинокі, до 3 см у діаметрі, більші – гігантські, трапляються рідко.
Класифікація виразок шлунка за Н. D. Johnson (1965)
- 1 тип. У ділянці кута шлунка або проксимальніше від нього – у так званій антрокорпоральній перехідній ділянці.
- 2 тип. Такі ж виразки, але в комбінації з виразкою дванадцятипалої кишки (дуоденальна виразка могла бути раніше).
- 3 тип. Виразки препілоричної ділянки, як звичайно, у межах 2,5 см від воротаря.
У модифікованій класифікації виділяють також 4 тип – високі виразки біля шлунково-стравохідного зʼєднання і 5 тип – гострі НСПЗП-асоційовані виразки, які можуть бути множинними і локалізуватися в будь-якому відділі шлунка, але найчастіше в антрумі
Виразки тіла шлунка (1-2 тип) утворюються на малій кривині, рідше на задній стінці, переважно ближче до малої кривини. Натомість препілоричні виразки можуть утворюватися на будь-якій стінці, подібно як і гострі ушкодження слизової.
Виникнення Н. руlory-асоційованих пептичних виразок залежить як від особливостей організму хворого, так і вірулентності штамів Н. pylori: експресії VacA, сигнальної послідовності алелі s1, цитотоксину, CagA+, локусу пластичності Hp jhp0947-jhp0949 тощо.
У разі проксимальних виразок шлунка атрофія і кишкова метаплазія зʼявляються раніше і виражені більше, ніж у хворих з гастритом, запалення виражене сильніше. Для атрофічної слизової оболонки притаманні слабкий захисний шар слизу, знижена секреція факторів росту, сповільнена регенерація, що зумовлює персистенцію і прогресування дефектів. Атрофія і кишкова метаплазія найбільше виражені в ділянці кута шлунка – стику між слизовою фундального й антрального типу, чим можна пояснити найчастіше виникнення виразок шлунка саме в цьому місці. Кислотопродукція в таких хворих часто знижена, однак опірність «слабкого» місця ще менша, адже атрофія в тілі виражена менше, ніж у ділянці кута. Крім кислоти, ульцерогенами можуть бути НСПЗП і жовчні кислоти.
Зміщення «фронту» між двома типами слизової з віком може пояснювати, чому в похилому віці виразки розміщені ближче до кардії. Позитивний ефект ерадикації на загоєння (і вщухання запалення) та відсутність рецидивів виразок свідчать про більше значення в їх патогенезі бактеріальних та запальних чинників, ніж атрофії та кишкової метаплазії самих по собі.
Натомість препілоричні виразки виникають, як і дуоденальні, на тлі антрального гастриту і підвищеної кислотопродукції.
Основною характеристикою виразок є їх дно (основа), утворене грануляційною тканиною, яка вкрита зоною фібриноїдного некрозу та ексудатом (детритом). На ранній фазі розвитку виразка, як звичайно, овальна або кругла, з рівним дном. Край доброякісної виразки гладкий, дещо випинається порівняно з дном. На ранній фазі розвитку виразки край рівний, слизова не відрізняється від довколишньої, складки тягнуться до самого краю (фаза А1). Надалі край стає нерівним, (фаза А2), часом вузлуватим, це віддзеркалює запальну реакцію, яка супроводжує загоєння, виявляється його наповзання на дно з веретеноподібними виступами. У разі великих виразок може відзначатися обрив або зникнення складок на певній відстані від краю виразки через виражений запальний вал.
Надалі шар детриту і фібриноїдного некрозу витончується, епітелій «наповзає» на дно виразки (зона з сітчастим рисунком, подібним до поверхневого гастриту – шлункові поля і лінії, що їх розділяють), яке зменшується концентрично, глибина виразки стає меншою, а дно – нерівним. Іноді виразка у процесі загоєння набуває лінійної форми або розділяється перемичками на дочірні кратери («фрагментується») – фаза Н. Відзначається конвергенція складок до краю виразки.
На стадії рубцювання (S) регенеруючий епітелій повністю вкриває дно виразки, він червоний через велику кількість капілярів – це фаза «червоного рубця», або палісадна (S1). Через кілька місяців епітелій не відрізняється від довколишнього і місце виразки можна визначити за конвергенцією складок, більш чи менш вираженою деформацією, це фаза «білого рубця», або «рубця-бруківки» (S2).
Фази процесу загоєння пептичних виразок аналогічні до фази загоєння будь-яких ран і розпочинаються з секреції факторів росту у краях і дні виразки.
Запальна інфільтрація оточує некротичні тканини. Під впливом факторів росту відбувається дедиференціація клітин краю виразки і розвиток грануляційної тканини. Потім настає рання фаза швидкого загоєння – проліферація і швидка міграція епітеліоцитів краю виразки на її дно, ремоделювання грануляційної тканини – зміна запальних клітин фібробластами, її скорочення із зменшенням дна виразки.
Наступною є пізня фаза повільного загоєння, ключовим моментом якої є ангіогенез у грануляційній тканині, що забезпечує її живлення. У цій фазі триває ремоделювання грануляційної тканини, завершується епітелізація. Далі відбувається реконструкція залоз і глибоких шарів слизової і дозрівання спеціалізованих клітин. НСПЗП не лише спричиняють утворення гострих уражень слизової оболонки, а й сповільнюють загоєння хронічних виразок.
Особливий вигляд мають виразки, які пенетрують у сусідні органи, для виразок шлунка – це ліва частка печінки і тіло підшлункової залози. Такі виразки дуже глибокі, виразки, що пенетрують у печінку, мають дотемно-коричневого кольору. іх ускладненням є профузні кровотечі.
Хоч є низка особливостей, характерних для злоякісних виразок (виразкового раку) – ригідність і звуження складок, їх обрив, конвергенція і потовщення їх закінчення, однак жодна з них не є абсолютною – ракові виразки можуть загоюватися під впливом лікування і не мати жодних візуальних ознак, які відрізняють їх від доброякісних (див. стор. 93). Єдиним надійним методом є множинна біопсія. Нині вважають, що виразки шлунка не малігнізуються – злоякісні виразки є еволюцією карциноми від моменту їх появи.
Для медикаментозних виразок характерна множинність, довколишня слизова оболонка не має ознак запалення (див. рис. 2.41). При довготривалому прийомі НСПЗП виразки можуть зливатися, тривалий час персистувати, утворюючи дефекти складної форми на тлі рубцевих змін.
Виразки шлунка, повʼязані з діафрагмальними грижами
Виразка Камерона – виразкування шлунка, яке при наявності хіатальної кили утворюється на рівні ніжок діафрагми («виразка-вершник»), найчастіше – на малій кривині. Вважають, що частота таких виразок сягає 5% від усіх ковзних діафрагмальних гриж, насамперед вони виникають при великих розмірах останніх.
Причина таких виразок – механічна компресія шлунка у стравохідному отворі діафрагми, вони можуть спричиняти гострі шлункові кровотечі, однак частіше супроводжуються хронічною крововтратою та анемією. Окрім виразок у цій ділянці на гребенях складок можуть траплятися і поверхневі ерозії, що призводять до хронічної крововтрати. Набагато рідше трапляються виразки Кея – виразки шлунка у грижовому мішку, і виразки Квінке – у стравоході вище грижового мішка.
Шлункові кровотечі
Виразкові кровотечі становлять приблизно половину всіх кровотеч з верхніх відділів травного каналу. Лише 4-25% їх триває на час ендоскопії після госпіталізації. У більшості випадків на дні виразки виявляють стигмати (ознаки перенесеної кровотечі).
Окрім зʼясування джерела і зупинки триваючої кровотечі, важливим завданням ендоскопіста є оцінка ризику рецидиву кровотечі і запобігання йому шляхом ендоскопічного гемостазу.
| Оцінка активності кровотечі за модифікованою класифікацією Forrest-Rosch (Rosch W., 1986) | |
| FI | Триваюча кровотеча |
| FIA | Цівкова артеріальна кровотеча. Найбільш небезпечна ситуація, без ендокопічного втручання навіть за умови консервативної зупинки частота рецидивів сягає 70-80% |
| FIB | Просочування (підтікання) крові. Підтікання може мати різне клінічне значення, високим ризик рецидиву кровотечі вважають при “підтіканні” крові з “видимої судини” |
| FIx | Підтікання з-під щільно фіксованого згустку, який неможливо видалити будь-яким шляхом, без верифікації джерела кровотечі* |
| FII | Кровотеча, що зупинилась |
| FIIA | “Тромбована судина” (червона, чорна, біла) – утвір, що випинається над поверхнею виразки, розміром до 2 мм різного кольору. Власне “судину”, яка має білий колір, видно рідко, виявити її важко. Утвір, що випинається над поверхнею виразки, є «вартовим» згустком крові, який фіксований в боковому отворі судини, утворюючи «корок» або псевдоаневризматичну кришку. Сучасні відеоскопи дають змогу виявити перлисто-білу, власне видиму судину, в такому разі ризик рецидиву кровотечі особливо високий. Діаметр кривавлячої артерії у шлунку становить у середньому 0,7 мм. |
| FIIB | Фіксований згусток (червоний, чорний, білий) – утвір, що випинається над поверхнею виразки, розміром більше 2 мм різного кольору |
| FIIC | Дрібні тромбовані судини (чорні крапки). Ці крапкі та плями різного кольору повʼязані з низьким ризиком рецидиву кровотечі, однак їх диференціація з тромбованою судиною може бути утруднена. Лікувальної ендоскопії не потрібно |
| FIII | Кровотеча відсутня: дефект під фібрином. Вимагає ретельного пошуку альтернативного джерела кровотечі (інша виразка, розрив Меллорі-Вейсса) або “тромбованої судини” білого кольору (Форрест IIA) на дні виразки. Якщо трапляється рецидив кровотечі, то він зумовлений або цими двома причинами, або прогресуванням некрозу на дні виразки у важких хворих з переважанням катаболізму. |
| Ендоскопічні ознаки кровотечі | Частота виявлення (%)* | Частота РК (%)* | Частота виявлення (%)** | Частота РК без ЕК (%)** | Частота РК після EK (%)** |
| FIA | 4-11,7 | 80-85 | 6,1 | 12 | |
| FIB | 10-17 | 50 | 7,9 | 6,1 | |
| FIx | 1,1 | ||||
| FIIA | 7-40 | 19-50 | 13,9 | 42,6 | 10,5 |
| FIIB | 10-30 | 20-50 | 14 | 22,5 | 5,9 |
| FIIC | 10-20 | 5-10 | 8,9 | 6,75 | 4,3 |
| FIII | 30-42 | 1-5 | 48,1 | 5,25 |
За даними Laine L., Peterson W.L. (1994), Wara P., 1985, Ell C. et al. (1995), Панцырев Ю.М. и соавт. (2001), Грубник В.В. и соавт. (2001).
* Нікішаєв В.. Ендоскопічна діагностика та мініїнвазивна ендохірургія при кровотечах з гастродуо-денальних виразок та варикозно-розширених вен стравоходу і шлунку // Автореф. дис. … д. мед. наук. – Київ, 2003. – 38 С.
Ризик рецидиву кровотечі вищий при розмірах виразок понад 2 см та їх локалізації у проекції великих артерій. За даними Swain C.P. et al. (1986), серед хворих з видимою судиною на дні виразки рецидив кровотечі трапляється у 78% при її локалізації на зад-ній і нижній стінках цибулини ДПК порівняно з 35% при виразках передньої і верхньої стінок та 78% при високих виразках тіла шлунка на противагу 15% при препілоричних виразках.
Кровотечі рецидивують переважно протягом перших 3-х діб. Якщо рецидиву кровотечі немає, то “вартовий тромб” через фазу “плоскої плями” зникає в межах 3-4 діб.
Надалі виразка має сіре дно. Інші стигми кровотечі зникають швидше, ніж видима судина.
Для системної оцінки ризику смерті та рецидиву кровотеч із верхніх відділів травного каналу запропоновано шкалу Роккалла (Rockall T.A. et al., 1996), аналіз її застосування засвідчив інформативність у передбаченні летальності.
Шкала Роккалла
| Клінічні критерії | 0 балів | 1 бал | 2 бали | 3 бали |
| Вік | <60 | 60-79 | ≥80 | ー |
| Шок | ー | AT > 100 ЧСС > 100 | AT < 100 ЧСС > 100 | ー |
| Хвороби | ー | ー | IXC, ХСН, важка супутня патологія | Недостатність нирок, печінки; пухлини |
| Ендоскопічні критерії | 0 балів | 1 бал | 2 бали | 3 бали |
| Причина | Тріщина Маллорі-Вейсса, без змін | Інші | Новоутвори | |
| Стигмати перенесеної кровотечі | Немає, пігментоване дно | Кров, струменева кровотеча, згусток, видима судина |
Методи ендоскопічного гемостазу
Аплікаційні методи:
нанесення плівкоутворюючих полімерів, клеїв, капроферу, 96% спирту, розчину амінокапронової кислоти тощо (останнім часом не застосовуються).
Термічні методи ендоскопічного гемостазу:
монополярна електрокоагуляція (гідродіатермокоагуляція), біполярна (мультиполярна) електрокоагуляція, термокаутеризація (за допомогою термозонда), лазерна фотокоагуляція, аргоноплазмова коагуляція.
Ендоскопічна інʼєкційна терапія (IT):
введення склерозантів (полідоканолу, натрію тетрадецилсульфату, етанолу), розчинів адреналіну, фібринового клею, фізіологічного розчину тощо.
Механічні методи:
кліпування, лігування.
Гастродуоденальні ерозії зумовлюють 8-15% шлунково-кишкових кровотеч (ШКК), основними їх причинами є прийом аспірину і НСПЗП та стресові ушкодження слизової оболонки. В обох випадках окрім ушкодження слизової наявне порушення зсідання крові. Такі гострі ушкодження слизової можуть перебігати у формі геморагічної гастропатії.
Для неї характерна поява плям червоного або коричнево-чорного кольору, розміри коливаються від точкових петехій до зливних екхімозів. Крововиливи у слизову оболонку можуть поєднуватися із кровотечею у просвіт шлунка.
На ранньому етапі утворення ушкоджень слизової є множинні дрібні дефекти слизової червоного кольору, які кровоточать на час огляду або вкриті згустками крові.
Надалі вони вкриваються нальотом фібрину, часто імбібованого гематином. У важких випадках стресового ураження слизової на тлі коагулопатії (ДВ3-синдрому) може спостерігатися дифузне просочування крові із застійної слизової шлунка без видимих дефектів.
Стресові ураження слизової шлунка є наслідком переважання ушкоджуючих чинників над протективними. Ішемія і реперфузійні ушкодження відіграють центральну роль у патогенезі, уможливлюючи пошкодження слизової кислотою і пепсином.
| Захисні чинники | Ушкоджуючі чинники |
| Адекватний кровоплин Бікарбонатний барʼєр Клітинні мембрани і міжклітинні зʼєднання | Кислота і пепсин Ішемія з тканинним ацидозом Реперфузійні ушкодження і утворення вільних радикалів Жовчні кислоти? H. pylori? |
Фактори ризику стресових уражень
- Пролонгована штучна вентиляція (> 48 годин)
- Коагулопатія
- Шок
- Важкий сепсис
- Травма/операція на ЦНС
- Поліорганна недостатність
- Важкий опік (>30% площі поверхні тіла)
- Ниркова недостатність
- Печінкова недостатність
- Політравма
- Стан після трансплантації органів
Судинні ураження шлунка
Загалом судинні ураження слизової оболонки травного каналу поділяють на такі групи (Lewis B., 1992):
I Ангіодисплазії – дилятовані тонкостінні судини, стінка яких містить малу кількість мʼязової тканини, переважно це підслизові вени. Трапляються найчастіше в осіб похилого віку і є набутим ураженням. Можуть мати круглу, зірчасту або павукоподібну форму з чітким краєм. Часом облямовані «гало» блідої слизової
а) спорадичні
b) повʼязані з нирковою недостатністю
с) повʼязані з хворобою Віллебранда
d) застійна гастропатія
e) GAVE.
II Венозні ектазії – дилятовані підслизові вени з витонченням вкриваючої їх слизової, не повʼязані з ураженням печінки
ІІI Телангіектазії – характерним є ураження всіх шарів стінки органів травлення, а також шкіри. Спадкові системні захворювання з рецидивуючим перебігом
IV Гемангіоми
V Артеріовенозні мальформації (аномалії розвитку) – вроджені ураження, товстостінні артерії і вени з утворенням артеріовенозних фістул. В утворенні АВМ беруть участь всі шари стінки органа
VI Ураження Дьєлафуа
Переповнені, варикозно розширені вени можуть імітувати поліпоз шлунка. Проте вена має синюватий колір і переважно трапляється разом із варикозно розширеними венами стравоходу. Така комбінація свідчить про портальну гіпертензію. Ізольоване розширення вен шлунка є ознакою тромбозу селезінкової вени, зокрема, після гострого панкреатиту або при карциномі підшлункової залози.
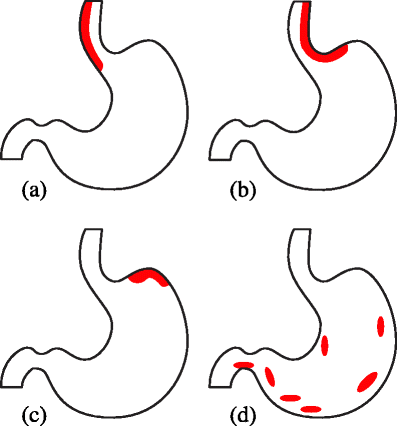
GOV – варикозне розширення вен стравоходу і шлунка
GOV1 (a) – варикозне розширення вен стравоходу з переходом на малу кривину шлунка (не менш ніж на 2-5 см)
GOV2 (b) – варикозне розширення вен стравоходу і дна шлунка
IGV – ізольоване варикозне розширення вен шлунка
IGV1 (c) – ізольовані, варикозно розширені вени шлунка, локалізовані у дні
IGV2 (d) – ізольовані, ектопічні, варикозно розширені вени, які можуть локалізуватися в інших відділах шлунка
Класифікація варикозно розширених вен шлунка за розмірами
І ступінь – діаметр до 5 мм, вени ледве вирізняються на тлі слизової шлунка
II ступінь – розмір від 5 до 10 мм, солітарно-поліпоїдного характеру
III ступінь – вени діаметром понад 10 мм, це обширний конгломерат вузлів, тонкостінні, поліпоїдного характеру
Модифікована класифікація портальної гіпертензивної гастропатії
| Легкий ступінь | Рожевувато-червоні плями («скарлатиноподібний рисунок») на слизовій і/або поверхнева еритема і/або мозаїкоподібний набряк слизової («зміїна шкіра») |
| Важкий ступінь | Характеризується наявністю дифузних вишневих або темно-червоних плям |
| Портальна гастропатія, ускладнена кровотечею | Геморагії, як при геморагічному гастриті |
Портальна гастропатія є наслідком портальної гіпертензії з дилятацією капілярів і розкриттям внутрішньослизових судинних шунтів. Вона вказує на важкість ураження печінки, але може бути й у хворих з підпечінковим портальним блоком. При морфологічному дослідженні відзначають дилятацію судин як слизової, так і підслизового шару.
Крововиливам у слизову сприяє тромбоцитопенія, яка розвивається при цирозі печінки. При портальній гастропатії збільшується чутливість слизівки до різних ушкоджуючих чинників: аспірину, алкоголю тощо. Відзначають регрес портальної гастропатії після транспечінкового портосистемного шунтування і погіршення – після склеротерапії або лігування варикозно розширених вен стравоходу.
New Italian Endoscopic Club (1997) рекомендує встановлювати діагноз портальної гастропатії на підставі чотирьох ознак: мозаїчний вигляд слизової, ураження у вигляді червоних крапок, вишнево-червоні плями, чорно-коричневі плями. Уражене насамперед тіло шлунка.
GAVE (gastric antral vascular ectasia) – порівняно рідкісне ураження слизової шлунка, для якого характерні смуги зі звивистих червоних ектатичних судин, локалізованих в антрумі по гребенях складок, з конвергенцією в бік воротаря. Через характерний вигляд це захворювання отримало назву «шлунок-кавун» («watermelon stomach»).
Рідше трапляється дифузна або плямиста картина ураження («honeycomb stomach»).
Патофізіологію ураження не зʼясовано, однак відзначають, що до 30% хворих з GAVE мають цироз печінки (тому необхідна диференціальна діагностика з портальною гастропатією), крім того, часто виявляють автоімунні захворювання сполучної тканини, хронічну ниркову недостатність, серцеву недостатність тощо. Патогномонічними є гістологічні особливості: гіперплазія власної пластинки слизової – фіброгіаліноз і проліферація веретеноподібних клітин, ектазія і тромбоз капілярів, аномальні судини під слизового шару. Це захворювання частіше супроводжується хронічною анемією, ніж гострими шлунково-кишковими кровотечами.
Виразка Дьєлафуа (Dieulafoy disease). Поверхневий дефект округлої або овальної форми, діаметром < 5 мм на тлі незміненої слизової оболонки, у дні дефекту – арозована велика артерія. Найчастіше локалізується у проксимальному відділі шлунка, проте може бути в будь-якому відділі травного каналу. В основі патології лежить розрив вроджено аномальної великої звивистої підслизової артерії (яка не зазнала зменшення діаметра у процесі галуження) без ознак васкуліту чи аневризми. Причиною утворення дефекту слизової вважають розрив аномальної судини. Це захворювання є причиною 0,5-5% усіх кровотеч з верхніх відділів травного каналу.
Сифіліс шлунка може нагадувати гіпертрофічну гастропатію (інфільтративне ураження при вторинному сифілісі), а також при утворенні гум у шлунку – екзофітні пухлини або виразки/виразковий рак (унаслідок розпаду гум). Краї таких виразок вузлуваті, нерівні, слизова довкола них інфільтрована. Диференціальну діагностику провести важко – окрім біопсії доцільні специфічні тести.
Легкі
Середньої важкості (помірні)
Важкі ураження
Каустичні ушкодження шлунка поділяють на три ступені (за Silverstein F.E. & Tytgat G.N.J., 1997)
Вогнищеве або смугасте почервоніння слизової шлунка
Поодинокі виразкування до 5 мм у діаметрі, крововиливи, незначна кровоточивість
Поширені некротичні зміни слизової – численні ерозії, виразки, слизова вкрита темним некротичним струпом і ексудатом.
Пізніше – грубі рубцеві зміни. Особливо часто ураження захоплює антральний відділ через спазм воротаря і скупчення тут агресивного вмісту.
Поліпи шлунка
Поліпом прийнято називати будь-який утвір (протрузію) не лише епітеліального, а й сполучнотканинного походження, на широкій основі або на ніжці, який випинається над поверхнею слизової. Поліпи трапляються у 2-3% хворих, яким виконували гастроскопію, як звичайно, вони безсимптомні. Найчастіше виявляють епітеліальні поліпи, які можуть бути неопластичними (аденоматозними або злоякісними) і не неопластичними (пухлиноподібними). До останніх, які трапляються у 80-90% випадків, зараховують поліпи з фундальних залоз та гіперпластичні (гіперплазіогенні) поліпи.
Поліпи з фундальних залоз – залозисті кісти Ельстера, кістозні гамартомні епітеліальні поліпи – становлять до 47% усіх поліпів. Частіше трапляються в жінок 40-69 р. Іх патогенез невідомий, вони можуть бути спорадичні або супроводжувати сімейний аденоматозний поліпоз (САП). Самі по собі не мають злоякісного потенціалу.
Гістологічно це видовжені і кістозно розширені фундальні залози без ознак метаплазії або запалення. Під час ендоскопії виглядають як дрібні поліпи на широкій основі з гладкою поверхнею в тілі і дні шлунка, колір подібний на колір довколишньої слизової.
Розміщені солітарно або формують тісні кластери, через малі розміри, переважно 2-3 мм, можуть ховатися між складками. Частота дисплазії спорадичних поліпів з фундальних залоз – 1-1,9%. При САП частота поліпів з фундальних залоз становить 25-44%, дисплазію в них виявляють набагато частіше, трапляється малігнізація.
Гіперплазіогенні (гіперпластичні) поліпи містять гіперплазовані шлункові залози і є дисрегенераторними утворами. Становлять 28-75% усіх поліпів шлунка – різна частота зумовлена відмінностями дефініцій. Жінки і чоловіки хворіють однаково часто, переважно у віці понад 60 р.
Частина авторів виділяє фовеолярну гіперплазію як початкову стадію розвитку поліпів. Це бляшкоподібні або конусоподібні дрібні розростання слизової шлунка, пере важно множинні, які трапляються як у тілі, так і в антральному відділі. Слизова оболонка потовщена за рахунок видовження ямок і високих валиків.
Гіперпластичні поліпи при мікроскопічному дослідженні містять розгалужені, видовжені гіперплазовані шлункові залози, на їх поверхні можуть бути ерозії та виразки.
На відміну від поліпів з фундальних залоз, гіперпластичні поліпи виникають на тлі не здорової слизової, а гастриту, особливо – автоімунного і Нр-асоційованого як активна регенераторна відповідь. У віддалені терміни після ерадикації Н. ру може настати регрес гіперпластичних поліпів.
Раніше вважали, що гіперпластичні поліпи не мають онкопотенціалу, за даними
Dalibo et al. (1987), частота вогнищ карциноми сягає 2,1%, дисплазії – ще у 4%, загалом літературні дані про частоту дисплазії коливаються від 1,9 до 19%, аденокарциноми – від 0 до 13%. Частіше виявляють рак у ділянці, прилеглій до поліпа – атрофічний гастрит, на тлі якого власне й виникають поліпи, супроводжується метаплазією і дисплазією. Зважаючи на це, рекомендують скринінгові обстеження хворих з гіперпластичними поліпами шлунка.
Більшість гіперпластичних поліпів є «сидячими» (хоча трапляються поліпи на довгих ніжках), часто – множинними. Гіперпластичні поліпи бувають запалені, ерозовані, можуть містити грануляційну тканину, ускладнюватися кровотечею. У дрібних поліпів слизова, як звичайно, не відрізняється від довколишньої, але в поліпів розмірами понад 5 мм вона переважно еритематозна, часом – ерозована. Ураження поліпами може охоплювати більшу частину органа, їх кількість може сягати десятків і сотень.
Запально-фібротичні поліпи – найрідкісніший тип поліпів – серед шлункових становлять до 3%, виникають у відповідь на хронічне пошкодження – Н. pilori, НСПЗП тощо. Можуть виникати у різних відділах ШКТ, у шлунку – найчастіше, частіше трапляються в жінок, середній вік хворих – 64 р. Гістологічно походять зі строми глибоких шарів СО і підслизового шару, містять рихлу строму й еозинофільний інфільтрат, поверхня гладка, але можуть бути ерозії і виразки.
Гамартомні поліпи шлунка трапляються при синдромі Пейтца-Єгерса, у шлунку їх виявляють у половини хворих на цей синдром. Серед гамартом можуть траплятися й аденоми, ризик раку шлунка в таких хворих підвищений (докладніше – див. розділ «Товста і клубова кишка»).
При ювенільному поліпозі виявляють гамартомні поліпи з вираженим запаленням строми, часто на ніжці, середній розмір 1 см. Можуть мати білу верхівку. Можливе ізольоване ураження шлунка. Ризик раку шлунка сягає 15-20%, рекомендований гастроінтестинальний скринінг з 25 років.
Неопластичні – аденоматозні поліпи становлять 7-10% усіх поліпів, як звичайно, вони солітарні і виникають у всіх відділах шлунка. Поверхня їх гладка або “часточкова” червоніша від довколишньої слизової, при детальному огляді поліп нагадує ягоду шовковиці. Частіше трапляються «сидячі» аденоматозні поліпи. За гістологічною будовою виділяють тубулярні, тубулярно-папілярні та папілярні аденоми, які найбільш схильні до малігнізації. Для шлунка виділяють також четвертий тип – аденоми з пілоричних залоз, які мають особливі імуногістохімічні характеристики.
Гістологічною особливістю аденом шлунка є псевдобагатошаровий епітелій, видовжені ядра, підвищена мітотична активність. Частіше аденоми належать до кишкового типу (містять бокалоподібні клітини і клітини Панета) і виникають на тлі атрофії і кишкової метаплазії слизової шлунка. Рідше бувають аденоми шлункового типу – як і поліпи з фундальних залоз, вони найчастіше повʼязані з САП.
Дисплазія важкого ступеня і рак in situ особливо часто трапляються у поліпах розміром понад 2 см і вільозних аденомах, які можуть бути сланкими. Конверсія аденом з пілоричних залоз в аденокарциному сягає 30%, що подібне до вільозних аденом. Аденоми, що виникають на тлі атрофії, є маркером ризику раку в інших ділянках шлунка (ретельно оглядають довколишню слизову!), синхронний або метахронний рак шлунка виявляють у 10% хворих з аденомами, а рецидиви аденом після поліпектомії – до 16%.
Порушення прохідності шлунково-стравохідного зʼєднання та воротаря трапляються у випадку поліпів даної локалізації, особливо якщо ці поліпи мають довгу ніжку і можуть “пролабувати” (мігрувати) у стравохід або дванадцятипалу кишку.
| SUTURA.ORG.COM | Гіперпластичні поліпи | Аденоматозні поліпи |
| Величина понад 2 см | < 10% | > 80% |
| Структура поверхні | Гладка або часточкова | Сосочкова |
| Наявність ніжки | < 30% | > 40% |
| Множинність | > 30% | 0 |
| Одночасна наявність карциноми | < 10% | > 40% |
| Мікроскопічні особливості | ||
| Злоякісна трансформація | 0 | ++ |
| Анаплазія | Відсутня | Суттєва |
| Гіперплазія | Слабка або помірна | Суттєва |
| Пілорична метаплазія | Суттєва | Відсутня або слабка |
| Кишкова метаплазія | Відсутня або слабка | Суттєва |
| М’язова тканина | Наявна | Відсутня |
| Кістозні залози | Часто | Рідко |
| Запалення | Виражене | Не виражене |
Рекомендації ASGE щодо тактики при поліпах шлунка (2006)
Аденоматозні поліпи шлунка мають підвищений ризик злоякісної трансформації і повинні бути видалені. Гіперпластичні поліпи мають низький потенціал малігнізації. Окільки вигляд поліпів не дає змоги диференціювати їх гістологічні підтипи, то рекомендується біопсія або видалення з гістологічним дослідженням виявлених поліпів.
Поліпи необхідно видаляти, якщо це можливо і клінічно доцільно. Якщо ендоскопічна поліпектомія неможлива, необхідна біопсія і при виявленні аденоматозної або диспластичної тканини (а також якщо біопсія не виключила повністю наявності диспластичних елементів) – хірургічне втручання.
При множинних поліпах шлунка біопсію беруть з найбільшого поліпа з різних місць (або його видаляють і досліджують). Подальше лікування ґрунтується на гістологічних результатах.
Після видалення аденоматозного поліпа доцільний ендоскопічний нагляд упродовж 1 року для виявлення рецидиву в місці видалення, нових або не виявлених під час попереднього дослідження поліпів. При негативному результаті – повторні ендоскопії з інтервалами 3-5 років. Нагляд після видалення поліпів, що містять ділянки дисплазії високого ступеня або ранній рак, має бути індивідуалізований.
Після адекватного гістологічного підтвердження або видалення недиспластичних поліпів шлунка ендоскопічний нагляд не потрібний.
- Чіткого консенсусу щодо видалення гіперпластичних поліпів немає
- Більшість експертів радить видаляти усі ГП понад 1 см і ретельно зважити питання про видалення поліпів 0,5-1 см (Ginsberg G.G. et al., 1996; Muehldorfer S.M. et al., 2002)
- Вважають, що ерадикація Н. ру може запобігти рецидиву ГП і навіть зумовити їх регрес при довготривалому спостереженні
Рекомендації Української асоціації лікарів-ендоскопістів
- Хворі з гіперпластичними поліпами розміром менше 5 мм повинні перебувати під динамічним ендоскопічним контролем (не рідше 1 разу кожні 6 місяців)
- Аденоматозні поліпи навіть невеликих розмірів підлягають ендоскопічному видаленню, оскільки належать до абсолютно передракових станів
- Поліпи, що досягають розмірів 20-30 мм при товщині ніжки не більше 15 мм, повинні підлягати ендоскопічному видаленню в умовах хірургічного стаціонару лікарем-ендоскопістом високої кваліфікації, що володіє методами ендоскопічного гемостазу та має необхідне технічне оснащення
Рак шлунка
Нині не виявлено єдиного етіологічного фактору раку шлунка, вважають, що це захворювання поліетіологічного походження. Його виникненню сприяють наявність інфекції Helicobacter pylori (до 80% випадків раку), європейський тип харчування: вживання великої кількості смаженого і копченого мʼяса, а також їжі, бідної на вітаміни, консервованої їжі з високим вмістом нітритів та нітратів, зловживання міцними алкогольними напоями, куріння.
В Європі, як і в Північній Америці, знижується частота некардіального раку шлунка (процес почався ще у 30-ті рр.), частота раку кардії і EGJ зростає, більшість пацієнтів має вік 50-70 рр., але зростає частота виявлення в осіб молодшого віку. В Україні захворюваність становить 30,8 на 100 000 населення.
Комітет ВООЗ рекомендував розрізняти два поняття:
- передракові стани – захворювання, наявність яких збільшує ризик утворення пухлини;
- передракові зміни – морфологічні зміни, при яких рак виникає вірогідніше, ніж за їх відсутності.
Гістологічні типи раку шлунка
Дифузний тип. Туморозні клітини утворюють скупчення, оточені дрібними дочірніми вогнищами, лежать поодинці або шнурами, між ними – волокна мукоїдної строми. Пухлина не має чітких країв. Багато клітин містять муцин – перснеподібні. Виникає в осіб порівняно молодшого віку, локалізується з переважно у проксимальному відділі, характеризується інфільтративним ростом, гіршим прогнозом.
Кишковий тип. Пухлина має залозисту структуру і чіткі краї. Можуть бути ділянки солідного або папілярного росту. Злоякісні клітини циліндричні або кубоподібні, з базальним розміщенням ядер. Характерний тривалий передраковий період, вузлова або поліпоподібна форма, виразкування пухлини, частіший розвиток у дистальних відділах шлунка. До 16% пухлин не вдається класифікувати – зарахувати до дифузного чи кишкового типу.
| Аденокарцинома | 45,9% |
| Скір | 27,1% |
| Солідний рак | 12,9% |
| Недиференційований | 6% |
| Слизовий | 3,3% |
| Плоскоклітинний | 0,6% |
| Змішані форми | 4,2% |
Хронічний гастрит вважають передраковим станом виходячи з явищ дисрегенерації, при якій проліферація може вийти з-під контролю. Кишковий тип раку шлунка розвивається з метапластичного епітелію на тлі мультифокального атрофічного гастриту і кишкової метаплазії, роль останньої визначається диспластичними змінами – важливо, що дисплазія при неповній метаплазії трапляється значно частіше. Про передраковий характер неповної метаплазії може свідчити і наявність у ній лактоферину. Він відіграє важливу роль в обміні заліза, яке потрібне для синтезу ДНК, тому в підвищеній кількості потрібний для реплікації ракових клітин. Нині вважається доведеним, що Helicobacter pylori відіграє важливу роль у розвитку кишкового типу раку, призводячи до мультифокального атрофічного гастриту. Автоімунний атрофічний гастрит також повʼязаний з розвитком кишкової метаплазії, і ризик раку шлунка при ньому підвищений, хоча й нижчий, ніж при Н. plori-асоційованому мультифокальному атрофічному гастриті.
Дифузний рак не має таких чітких прекурсорів, як кишковий тип, однак частота дифузного раку шлунка в Н. руlori-інфікованій популяції вища, ніж у не інфікованих осіб.
Фактори ризику раку шлунка, що потребують нагляду
- Сімейний аденоматозний поліпоз
- Аденоми шлунка
- Виявлення дисплазії високого ступеня при біопсії
Доведені фактори ризику
- Хронічний атрофічний гастрит
- Метаплазія при біопсії
- Інфекція H. pylori
- Спадковий неполіпозний колоректальний рак (синдром Лінча II)
Ймовірні
- Резекція шлунка в анамнезі (>20 р.)
- Перніціозна анемія
- Куріння (аденокарцинома кардії)
Можливі
- Надмірне вживання алкоголю
- Гамартоми
- Зловживання солоною, пряною і копченою їжею
- Споживання в малій кількості фруктів та овочів
- Хвороба Менетріє
- Синдром Пейтца-Єгерса
- Куріння (крім раку кардії)
Проблематичні
- Доброякісні виразки шлунка
- Поліпи з фундальних залоз
- Гіперпластичні поліпи
Ранній рак шлунка
Проблема виявлення раннього раку шлунка має принципове значення для забезпечення доброго прогнозу для хворого – саме завдяки впровадженій системі ендоскопічного скринінгу раннього раку серед населення в Японії вдалося досягти значних успіхів у лікуванні раку шлунка.
Для оцінки поверхневих карцином шлунка, як і інших відділів травного каналу, у Парижі (2002) прийнято ендоскопічну класифікацію поверхневих пухлинних уражень на основі класифікації Japanese Gastric Cancer Association (JGCA) (див. с. 43). Для вчасного виявлення таких неоплазій необхідне застосування сучасних технологій – хромоендоскопії, електронної хромоскопії (NBI, FICE), конфокальної ендоскопії, ендоцитоскопії Для якісного огляду деталей слизової відсмоктують вміст і застосовують піногасники, (у випадках хромоендоскопії – ацетилцистеін).
За даними М. Sasako (Паризький воркшоп 2002 р.), у ділянці кардії частота різних типів поверхневих неоплазій така ж, як і в CLE, – переважають ураження типу 0-II, причому вдавлені (0-ІІc) трапляються рідше, ніж в інших відділах шлунка. Для решти ділянок шлунка теж переважають новоутвори 0-ІІ, однак серед них найчастіше трапляються вдавлені (0-ІІc) – до 70-80%. Сумарна частота неоплазій 0-І і 0- ІІІ не перевищує 5%.
Глибина підслизової інвазії збільшується з діаметром пухлини і найвища при поліпоподібних (0-І) і вдавлених 0-ІІс новоутворах, особливо з комбінованим виглядом поверхні (0-ІІc + ІІa, 0-ІІa + ІІc, O-ІІc + III)).
Поверхневий рак, тип 0-І, відзначається еритематозною нерівною поверхнею, часом з вузликами. Поверхневий рак, тип 0-lІa – припіднята площадка, відзначається нерівною поверхнею, з фактурою, відмінною від довколишньої, може нагадувати сланку вільозну аденому. Поверхневий рак, тип 0-ІІb, виявити найважче. Це ділянки слизової зі зміненим кольором та фактурою поверхні. Поверхневий рак, тип 0-Іс, – вдавлені ділянки зміненої слизової, можуть бути вкриті фібрином. Останні два підтипи можуть нагадувати виразки на стадії загоєння, диференціація дуже важка. Однак, якщо для доброякісних виразок характерні гладкі довколишні складки, що закінчуються в ділянці загоєння, то при поверхневих раках закінчення складок випнуті або потовщені. На стадїї загоєння доброякісних виразок слизова має вигляд червоного обідка з сітчастим рисунком lineae gastricae.
Натомість у разі наявності карциноми слизова інтенсивно червона або ділянки почервоніння чергуються з сірувато-блідими, вони чітко відмежовані від довколишньої слизової.
Особливі труднощі виникають при виявленні виразкового (заглибленого) поверхневого раку шлунка 0-ІІI. Вогнище карциноми може бути тільки в одному з країв виразкування – вважають, що до 5% виразок шлунка, на вигляд доброякісних, є раннім раком. Важливо, що підритий тип раку шлунка під впливом лікування може загоюватися, як і доброякісні виразки, переходячи у тип 0-ІІс, а пізніше під впливом кислотної агресії знову виникає виразкування (злоякісний цикл за Sakita et al., 1971). Цей тип поверхневого раку досі переважає у західній статистиці через «пропускання» плоских неоплазій (0-IІ) та обстеження хворих із клінікою диспепсії, а не зі скринінговою метою.
| Ознаки | Доброякісні виразки | Виразковий рак |
| Дно | Як звичайно, гладке і гомогенне | Як звичайно, нерівне |
| Край | Рівний, слизова має інтактний вигляд | Нерівний, його порушують пухлинні вузли |
| Край відносно довколишніх складок | Край і складки зливаються рівномірно | Складки «обриваються» або деформуються пухлинним ростом |
| Розміри | Малі виразки (при розмірах до 1 см доброякісні у 95% випадків) | Великі виразки (при розмірі понад 2 см злоякісні у 20% випадків) |
Жодна з візуальних ознак не має абсолютного значення!
3a Japanese Gastric Cancer Association (JGCA) – Паризькою класифікацією неоплазій травного каналу, передбачається 5 типів поширеного раку шлунка:
- Поліпоїдний тип (3-20%).
- Виразковий рак з чітко відмежованими і піднятими краями (20-40%).
- Інфільтративно-виразковий рак (12-15%).
- Дифузно-інфільтративний (не виразковий) рак (до 30%).
- Занедбаний рак, що не підлягає класифікації.
Поліпоїдний рак шлунка найчастіше трапляється у тілі шлунка, однак може бути також у кардії або препілоричній ділянці. Має вигляд екзофітного утвору без виразкування з сірою, нерівною поверхнею, добре відмежованого від довколишньої слизової.
Виразковий рак шлунка – це вузол із центральним виразкуванням (вважають, що це виразкування екзофітного раку) і довколишнім пухлинним валом або виразка із вузлуватими, еритематозними краями, які добре відмежовані від довколишньої слизової і на які не переходять її складки. На дні таких виразок серед некротичних мас може бути грануляційна тканина, у тому числі з ділянками пухлинного росту.
Інфільтративно-виразковий рак. Виражена інфільтрація стінки шлунка з центральним виразкуванням. Інфільтрація має вигляд потовщених складок, а не чітко демаркованої пухлини без чіткої межі з неураженою стінкою шлунка. Слизова довкола виразки може бути почервоніла, але може мати і звичайний вигляд, підтвердження діагнозу з допомогою біопсії утруднене.
Дифузно-інфільтративний (не виразковий) рак може мати локальний або дифузний характер (linitis plastica). Новоутвори цього типу локально частіше уражають тіло шлунка. При підслизовому рості пухлини ендоскопічна діагностика цього типу раку доволі складна. Вона ґрунтується на «побіжних» ознаках: ригідності стінки шлунка в ділянці ураження, згладженості рельєфу слизової. Уражена ділянка дещо випнута, складки нерухомі, погано розправляються повітрям, перистальтика ослаблена або відсутня. Однією з ознак інфільтративного раку шлунка є «ефект шельфу». У цьому випадку дистальний край інфільтративної пухлини тіла шлунка доволі різко припіднятий над неураженою ділянкою. Гістологічна верифікація при простій щипцевій біопсії проблематична: інфільтративний ріст пухлини відбувається насамперед у підслизовому шарі – характерною є ригідність складок («симптом шатра»). При поширенні процесу шлунок перетворюється на вузьку малорухому трубку або набуває вигляду «шкіряної пляшки» (linitis plastica). Поверхня слизової може бути не зміненою або еритематозною, матовою, нерівною, з брудно-сірими нашаруваннями – останнє свідчить про ураження її поверхні.
Рак кукси шлунка. За сучасними оцінками, ризик раку кукси шлунка через 20 і більше років після неонкологічної резекції зростає у 12 разів порівняно із загальною популяцією. Факторами, які сприяють розвитку пухлини, вважають атрофічний гастрит (унаслідок денервації кукси і видалення гуморально активного антрального відділу) та рефлюкс жовчі.
Неепітеліальні доброякісні і злоякісні новоутвори шлунка
Шлунково-кишкові стромальні пухлини – gastrointestinal stromal tumor (GIST) нині вважають найчастішими мезенхімальними неоплазіями травного каналу, вони виникають переважно в осіб похилого віку, щороку виявляють до 10-20 випадків таких новоутворів на 1 млн. населення. До 60-70% їх міститься у шлунку. Вони можуть локалізуватися підслизово, інтрамурально і навіть субсерозно, мають овальну форму, іноді – багаточасткову, часом – ніжку. На верхівці такого утвору може виникати виразкування унаслідок некрозу (кістозних змін), у такому разі може виникнути кровотеча.
Гістологічна структура їх різна – вони можуть містити веретеноподібні або епітеліоїдні клітини, а також гігантські клітини та пучки колагенових волокон. Від гладкомʼязових новоутворів (на які їх будова подібна під час світлової мікроскопії) їх відрізняють імуногістохімічним методом – для них характерна експресія с-kit протоонкогену (CD117) – мембранного рецептора тирозинкінази і CD34. Нині вважають, що GIST виникають не з мʼязових клітин, а з плюрипотенціальних мезенхімальних клітин, які є попередниками пейсмекерних клітин Кахаля.
Під час ендоскопії GIST виглядають як вузли, що випинаються у просвіт органа і вкриті нормальною слизовою, часом – з виразкуванням. Злоякісність утвору важко визначити за гістологічними особливостями – вона визначається схильністю до метастазування до і після видалення. Важливими факторами ризику злоякісності вважають розміри понад 5 см і кількість мітозів більше 5 на 50 полів зору при великому збільшенні.
Лейоміома шлунка виникає з мʼязової оболонки або власної мʼязової пластинки слизової, частіше в тілі шлунка. Гістологічно складається з веретеноподібних клітин з сигароподібними ядрами без підвищеної кількості мітозів. На доброякісний характер вказує чіткість контурів і відмежованість від довколишніх тканин.
Лейоміоми при ендоскопічному дослідженні виглядають як пухлиноподібні утвори круглястої форми, величина яких сягає 6-8 см, але частіше не перевищує 1-2 см. Слизова, яка їх вкриває, нормальна або витончена, здебільшого не фіксована до пухлини. На відміну від стравоходу, справжні лейоміоми у шлунку трапляються рідко – імуногістохімічні дослідження засвідчили, що більшість таких новоутворів у шлунку насправді є GIST. Подібний вигляд може мати також шваннома. Лейоміосаркома гістологічно містить більше клітинних елементів, негомогенна, має ділянки сітчастої будови. Відрізняється більшими розмірами, нерівним контуром.
Карциноїд виникає з ентерохромафіноподібних клітини або ECL-клітин слизової і має вигляд гладкого, круглого, жовтого вузлика. При більших розмірах його форма може бути неправильною, з втягненням або виразкуванням.
Гломусні пухлини, як звичайно, локалізуються в антрумі, мають невеликі розміри, виглядають як синьо-червоні вузлики, що походять з мʼязової оболонки. Гістологічно – містять круглі дрібні гломусні клітини у стінках дилятованих судин.
Ліпома у шлунку трапляється рідше, ніж у товстій кишці, здебільшого – в антрумі, має вигляд блідожовтуватого мʼякого підслизового утвору.
Лімфоми шлунка
Шлунок є найчастішим місцем виникнення лімфом травного каналу (до 10% усіх лімфом і до 3% злоякісних пухлин шлунка). Вони виникають із лімфоїдної тканини, повʼязаної зі слизовою (MALT – mucosa associated lymphoid tissue), і у шлунку є В-клітинними: агресивна дифузна крупноклітинна В-клітинна лімфома (DLBCL) та індолентна В-клітинна лімфома маргінальної зони MALT-типу. їх виникнення повʼязують з інфекцією H. pylori, яка стимулює розвиток лімфоїдної тканини слизової шлунка.
Ендоскопічно лімфоми шлунка можуть мати вигляд пухлинних вузлів, ділянок з виразкуванням або ерозіями, множинними поверхневими виразками, а також гіпертрофічних, вузлуватих складок. Щипцева біопсія малоінформативна через підслизовий характер росту – доцільна біопсія «джамбо»-щипцями, забір матеріалу кілька разів з одного й того ж місця, ендоскопічна резекція слизової і тонкоголкова пункція. У разі інфільтративних змін при роздуванні не виявлено такої ригідності шлунка, як при інфільтративному раку.
MALT-лімфома низького ступеня злоякісності проявляється насамперед гастритоподібним ураженням за типом антрального гастриту, ерозивного гастриту або локального потовщення складок (обмеженого гіперпластичного гастриту). Нерідко ця форма MALT-лімфом проявляється поодинокими виразками, а також пухлинним ураженням у вигляді бляшок і вузлів. Цей тип MALT-лімфом відзначається високою частотою регресії і стійкої ремісії після ерадикації Н. pylori.





