Рани та раньовий процес
ВСТУП
Гнійно-запальні захворювання та післяопераційні гнійні ускладнення є актуальною проблемою сучасної клінічної хірургії.
Незважаючи на постійне удосконалення методик оперативних втручань, частота інфекційних ускладнень в хірургії становить у середньому 3-15%, а за даними окремих авторів сягає 30%. В теперішній час 35-40% хворих хірургічного профілю становлять пацієнти з гнійно-запальними захворюваннями.
Інфекційні ускладнення збільшують показники післяопераційної летальності, обсяги витрат на лікування, кількість додаткових діб, провезених у стаціонарі. Це свідчить про значну медичну й соціально-економічну зна-чимість проблеми профілактики та підвищення ефективності лікування інфекційних ускладнень в масштабах України.
При інфекційних ускладненнях поряд з хірургічною обробкою та системною терапією, важлива роль відводиться місцевому медикаментозному лікуванню гнійних ран під пов’язкою, яке є економічним, технічно простим й доступним. У порівнянні з іншими методами лікування даний спосіб має суттєву перевагу завдяки безпосередньому лікувальному впливу на осередок інфекції.
Метод не має альтернативи при наданні допомоги в умовах рейсових уражень при ліквідації катастроф, стихійних лих, війскових конфліктів. Загальні принципи місцевого лікування ранового процесу було викладено раніше («Місцеве медикаментозне лікування ран», Київ-Харків, 1994 р.)-
В теперішній час, удосконалення підходів до вирішення питань підвищення ефективності лікування ран та профілактики ранових інфекційних ускладнень неможливе без клініко-лабораторного, патогенетичного та фармакологічного обгрунтування принципів, паказань до призначення, критеріїв вибору та схем місцевого застосування принципово нових комбінованих препаратів на полімерних гідрофільних основах а також системного введення сучасних антибіотиків.
Саме тому метою даної відомчої інструкції є обгрунтування раціональної системи лікувальних заходів на всіх етапах ранового процесу (хірургічна обробка, місцеве медикаментозне лікування, антибіотикопрофілактика та сучасна системна антибіотикотерапія), впровадження яких дозволить удосконалити ефективність надання хірургічної допомоги лікувально-профілактичними закладами України.
Видання призначено лікарям хірургічного профілю, викладачам кафедр хірургії, студентам старших курсів вищих медичиних закладів, лікарям-інтернам, сімейним лікарям, та має на меті удосконалення медикаментозного лікування ранового процесу в залежності від його фази та характеру мікрофлори.
РАНОВИЙ ПРОЦЕС. ВИЗНАЧЕННЯ ТА КЛАСИФІКАЦІЯ
Рановий процес – комплекс загальних та місцевих реакцій організма у відповідь на ураження тканин, який спрямовано на загоєння рани.
Класифікація ран:
- За характером ураження: вогнепальна, різана, колота, рублена, розмізджена, забита, рвана, подряпина, садно, вкушена, скальпована, змішана.
- За глибиною:
- поверхнева;
- проникаюча (без ураження та з ураженням внутрішніх органів);
- глибока;
- За причиною:
- Операційна;
- випадкова (побутова, виробнича, автодорожна, військового часу);
- В залежності від локалізації ураженої частини тіла (шкіри та підшкірної клітковини; покривів черепу; мозку та його оболонок; шиї; грудинної стінки; плевральної порожнини; легенів; межистіння; органів черевної порожнини та черевини; органів тазу; кісток та суглобів).
- За ступенем інфекування:
- асептична (“чиста” або умовно “чиста” – тільки при планових операціях та рани після первинної хірургічної обробки);
- інфікована (після хірургічного втручання з приводу гострих гнійних захворювань);
- В залежності від терміну виникнення
- свіжа (якщо постраждалий звернувся за допомогою впродовж перших 24 годин після поранення);
- запізніла (якщо постраждалий звернувся за допомогою пізніше 24 години після поранення).
В свою чергу, операційні рани в залежності від вірогідності та ступеня контамінації можуть бути класифіковані наступним чином:
Чисті рани – неінфіковані операційні рани без ознак запалення, які не проникають в дихальні шляхи, травний тракт, статеві та сечовивідні шляхи. На чисті рани накладаються первинні шви. Рани за необхідністю дренуються закритими дренажами. Операційні різані рани після непроникаючої (тупої) травми теж відносяться до цієї категорії, якщо вони відповідають наведеними в таблиці критеріям.
Умовно-чисті рани – рани, які проникають в дихальні шляхи, травний тракт, статеві та сечовивідні шляхи в контрольованих умовах та при відсутності незвичайного зараження. До цієї категорії відносять операції на жовчних шляхах, апендиксі, піхві, ротоглотці при відсутності ознак інфекції та грубих порушень техніки операції.
Чисті або умовно-чисті рани, у більшості випадків, загоюються по типу первинного натягнення, якщо краї рани співставлені без виникнення дефекту тканин.
| Клас рани | Характер оперативного втручання | Ускладненя, % |
| І. Чисті хірургічні операції | Нетравматичні, неінфіковані операційні рані без ознак запалення, які не зачіпають респираторний, травний або сечовивідний тракт; під час проведення операції не було порушень асептики | 1-5 |
| II. Умовно чисті хірургічні операції | Операції, при яких в контрольованих умовах було порушено цілісність респираторного, травного або сечовивідного тракту, але без незвичної контамінації (значного витікання вмісту полого органу) | 8-11 |
| III. Контаміновані хірургічні операції | Операції, які пов’язані з відкритими, травматичними ранами; суттєвими порушеннями стерильності під час операції, значним витіканням вмісту полих органів; гострим гнійним запаленням | 15-29 |
Забруднені (контаміновані) рани – відкриті свіжі травматичні рани, операції із значним порушенням техніки стерильності або із значним проникненням вмісту із травного тракту, а також розрізи, які залучують ділянку гострого негнойного запалення.
Брудні або інфіковані рани — травматичні рани, в яких е мертві тканини, а також рани із вираженою клінічною інфекцією або перфорацією внутрішніх органів. Важливо, що мікроорганізми, які визвали післяопераційну інфекцію, були присутніми в операційному полі до початку операції.
В сучасних умовах особливого значення набуває проблема внутрішньолікарняних інфекцій, зокрема – хірургічних ранових інфекцій. Для того, щоб втановити діагноз внутрішньолікарняної інфекції необхідно виключити всі ознаки того, що інфекція була присутньою в маніфестній формі чи в інкубаційному періоді на час госпіталізації. Виключення складають випадки визначення нового патогенного збудника або зміни характеру клінічної симптоматики, які свідчать про приєднаня нової інфекції.
Хірургічні ранові інфекції поділяють на інфекції в ділянці розрізу та глибокі.
Хірургічні ранові інфекції в ділянці розрізу виникають протягом 30 діб після хірургічного втручання, залучають шкіру, підшкірні тканини або м’язи, які знаходяться над фасціальним шаром.
Діагностичні критерії:
- гнійний відділок із розрізу або дренажу, які розташовані вище фасціального шару;
- виявлення мікроорганізмів у посіві рідини із рани, яка загоялася первинним натягом;
- хірург навмисно відкриває рану, за виключенням випадків, коли мікробіологічне дослідження дає негативні результати.
Глибокі хірургічні ранові інфекції виникають в ділянці хірургічного втручання протягом 30 діб після операції (при відсутності імплантанту), або протягом одного року при його наявності. В інфекційно-запальний рановий процес залучаються тканини в ділянці фасціального шару та глибше нього.
| Фактори ризику та засоби профілактики хірургічних ранових інфекцій* | ||
| Фактори ризику | Засоби профілактики | Обгрунтування |
| Тривале перебування пацієнта у лікарні перед операцією | Вкорочення термінів госпіталізації. Передопераційне тестування в поліклініці | Зниження вірогідності хірургічних ранових інфекцій |
| Гоління хворого напередодні операції | Перевага віддається голінню волос безпосередньо перед початком операції | Зниження вірогідності хірургічних ранових інфекцій |
| Неадекватний вибір препарату для антибактеріальної профілактики (терапії), його дози та часу введення | Раціональний вибір відповідних антибіотиків; застосування оптимальних доз, способів та кратності введення; адекватна тривалість курсів лікування; обгрунтована ритмічна зміна антибіотиків | Досягнення необхідної концентрації антибіотику у тканинах під час операції |
| Неадекватний вибір препаратів для місцевого лікування ран | Патогенетичне обгрунтований вибір засобів місцевого медикаментозного лікування ранового процесу в залежності від фази та характеру мікрофлори. Скорочення термінів госпіталізації. | Зниження вірогідності хірургічних ранових інфекцій |
| Застосування неефективних антисептиків (наприклад нітрофуранових розчинів) | Застосування антисептиків широкого спектру дії (діоксидин, мірамістин, повідон-йод) | Зниження ризику перехресної контамінації рани |
| Застосування великих флаконів з антисептиками, які заповнюються без попереднього промивання | Застосування маленьких флаконів. При застосуванні великих флаконів, їх слід промити та повністю висушити перед повторним наповненням. | Зниження ризику контамінації |
| Недотримання принципів профілактики ранової інфекції на кінцевих фазах лікування ранового процесу та після виписки пацієнта із стаціонару | Призначення препаратів для профілактики ранової інфекції на кінцевих фазах лікування ранового процесу та після виписки пацієнта із стаціонару. Моніторинг випадків повторної госпіталізації в результаті ранової інфекції на протязі одного місяця після більшості хірургічних втручань, та на протязі одного року після встановлення імплантатів | Зниження вірогідності та профілактика хірургічних ранових інфекцій |
Примітка. * – дані приведені згідно (О.О. Шалімов та співавтор., 2000 р ) із змінами та доповненнями
Важливо, що мікрофлора сучасних ран стійка до часто застосовуваних антибіотиків.
За цих умов, для місцевого лікування ран більш доцільним є використання:
- комбінації кількох речовин, які мають різноспрямований спектр протимікробної активності (наприклад, стрептоцид з нітазолом);
- нових синтетичних протимікробних речовин (наприклад, офлоксацину), до яких не сформувалась висока резистентність мікрофлори;
- антисептиків (діоксидину, мірамістину та інших), до яких немає ні природної, ані набутої резистентності мікроорганізмів (в тому числі їх госпітальних штамів).
ЗАГАЛЬНІ ПРИНЦИПИ ЛІКУВАННЯ РАН
Першим обов’язковим етапом лікування ран є адекватна хірургічна обробка, яка має вирішувати наступні задачі:
- якомога повне очищення рани від гнійно-некротичних тканин та інородних тіл;
- зниження рівня мікробного засіменіння;
- забезпечення умов для повноцінного відтоку ранового ексудату;
- профілактика подальшого розвитку нагноєння та генералізації інфекції;
- створення оптимальних умов для раннього закриття та швидкого загоєння.
Розрізняють наступні види хірургічної обробки рани:
Первинна хірургічна обробка рани – проводиться в “свіжій” (без ознак запалення) рані в перші години після ушкодження, спрямована на попередження розвитку інфекції і завершується накладанням швів.
Вторинна хірургічна обробка рани – проводиться за вторинними показами у тих випадках, коли після первинної хірургічної обробки в рані розвивається запальний процес з утворенням гнійної порожнини та вторинних некрозів.
Відстрочена хірургічна обробка рани – проводиться у тих випадках, коли операції передує підготовка хворого напротязі 2-5 діб. Часто така операція має на меті закриття ранової поверхні.
Доцільно також виділяти:
Повну хірургічну обробку рани – радикальне висічення в межах здорових тканин.
У випадку, коли анатомічні умови або ступінь розповсюдження запального процесу не дозволяють здійснити обробку у повному обсязі, здійснюють часткову хірургічну обробку рани. При якій обмежуються висіченням рани, розкриттям затіків, дренуванням й тільки частковим виділенням некротичних тканин.
МЕТОДИ МІСЦЕВОГО ЛІКУВАННЯ РАН
До методів, які підвищують ефективність хірургічної обробки рани та її наступне лікування відносяться:
Застосування гіпертонічних розчинів Мета – створення осмотичного відтоку в рані та її очищення.
Метод реалізується за допомогою введення в рану тампонів, змочених 10% розчином натрію хлориду, 3-5% розчином борної кислоти та інших речовин.
До суттєвих недоліків методу відносяться:
- короткочасна дія, яка призводе то того, що вже через 2-3 години після нанесення розчини розбавляються рановим вмістом та втрачають осмотичну активність;
- переважно поверхнева активність;
- пересушування ранової поверхні;
В теперішній час застосування гіпертонічних розчинів повинно обмежуватись тільки першою добою після розкриття гнійників.
Застосування розчинів антисептиків Метод полягає у введенні в рану пов’язок з антисептичними розчинами (фурацилін, хлоргексидин, перекис водню та інші).
До недоліків методу відносяться:
- недостатня антисептична активність
- відсутність осмотичної дії
- поверхнева активність.
Традиційне застосування перекису водню відповідає здебільшого вимогам механічної обробки рани, але не її мікробного очищення.
За цих умов доцільно застосовувати сучасні ефективні антисептики:
- інгібітори синтезу (обміну) ДНК (діоксидин, Діоксизоль)
- катіонні антисептики (Мірамістин, цетилпирідінію хлорид)
- йодофори (полійодідні комплекси полівінілпіролідону – розчини повідон-йоду, йодопірону та інш.)
Дренування ран (активне або пасивне)
Накладання лікувальних пов’язок з препаратами на сучасних гідрофільних основах, які забезпечують комбіновану дію:
- протимікробну
- знеболюючу
- протизапальну
- контрольовану дегідратаційну
Крім того, препарати на гідрофільних основах ефективно проводять лікарські речовини вглибину осередка ураження, ранові канали, порожнини та в мікробні клітини.
Застосування додаткових методів (кварцування, ультразвукова кавітація гнійних порожнин, гіпербарична оксигенація, обробка ран високоенергетичним лазером, тощо).
ХАРАКТЕРИСТИКА ОСНОВНИХ ФАЗ РАНОВОГО ПРОЦЕСУ
Для практичної роботи, у перебігу ранового процесу доцільно виділяти три послідовні фази:
- гнійно-некротичну, яка характеризується наявністю некротичних тканин, гнійного вмісту в рані, інфільтрацією її країв. В цій фазі спостерігається високий рівень бактеріальної забрудненості, а порушення метаболічних процесів призводе до підвищення осмотичного тиску в тканинах, яке на тлі ацидозу та порушення мікроциркуляції в осередку запалення призводе до розвитку вторинних некрозів. Саме в глибині рани, в осередку вторинних некрозів, а не на її поверхні локалізується мікрофлора, яка визначає важкість та напрямок перебігу ранового процесу;
- фазу грануляцій, яка визначається очищенням рани від гнійно-некротического секвестру, наявність серозного ексудату, відсутністю ранового процесу проявляється появою та розвитком грануляційної тканини, яка поступово виповнює рану;
- фазу епітелізації, яка клінічне проявляється епітелізацією ранової поверхні та реорганізацією (стверденням) рубця.
Незважаючи на спільність біологічних законів загоєння ран, які не залежать від її генезу та локалізації, клінічний перебіг ранового процесу суттєво розрізняється при загоєнні ран первинним, вторинним натягненням або при загоєнні під струпом.
Первинне загоєння ран (первинне натягнення) – при стиканні країв рани і відсутності інфекції. Загоєння відбувається за 6-8 діб. Операційні рани, у більшості випадків, загоюваться саме первинним натягненням.
Вторинне загоєння ран (вторинне натягнення) – при наявності ранового дефекту зі значною зоною ураження навколо рани фозмідження країв), великої кількості нежиттєспроможних тканин, згустків крові, інородних тіл та мікробної флори.
У цьому випадку загоєння відбувається через нагноєння рани шляхом заміщення ранового дефекту грануляційною тканиною та формування рубця. Процес характеризується тривалим перебігом впродовж декількох тижнів.
Загоєння рани під струпом – при наявності поверхневих ран, коли вони покриваються кіркою з крові та клітинних елементів. Епітелізація відбувається під кіркою.
ЗАГАЛЬНА ХАРАКТЕРИСТИКА ПРЕПАРАТІВ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ РАН
КЛАСИФІКАЦІЯ
Лікарські засоби, що використовують для місцевого лікування ран, поділяються на дві основні групи:
• монопрепарати на жировій основі з односпрямованою (протимікробною, ранозагоювальною та ін.) дією, до яких належать стрептоцидова, гентаміцинова, еригроміцинова, фурацилінова, метилураідилова мазі, лінімент синтоміцину та інші;
Основними недоліками монопрепаратів на жировій основі є:
- односпрямована дія. що у багатьох клінічних випадках є недостатнім для раціонального лікування, а у практичних умовах вимагає одночасного застосування кількох препаратів;
- погане вивільнення діючих речовин;
- порушення відтоку ранового вмісту та герметизація рани.
Таким чином, застосування цієї групи препаратів недоцільне, особливо в першій фазі ранового процесу у зв’язку з високим мікробним навантаженням, гнійно-некротичним вмістом рани та гіпергідратацією тканин.
• монопрепарати на синтетичних гідрофільних водорозчинних основах (гель Левоміцетин, крем Дермазин та ін.);
Для монопрепаратів на синтетичних гідрофільних водорозчинних основах протизапальної, осмолярної дії.
• комбіновані препарати :
А) на жировій основі (вазелин-ланоліновій, олійній або бальзамічній), до яких належать мазі «Альгофін», «Фастин-1», лінімент бальзамічний за Вишневським та ін.;
Б) на синтетичних основах:
– першого покоління (на основі комбінації поліетиленоксидів 400/1500 -Левомеколь та Левосин);
– сучасні препарати на удосконалених водорозчинних синтетичних основах (у складі пропиленгліколю, проксанолу та поліетиленоксиду 400) -розчин Діоксизоль, мазі Офлокаїн, Нітацид, Мірамістин, Стрептонітол, Метилурацил, гель Пантестин), що здійснюють комплексний вплив на основні ланки патогенезу ранового процесу.
Суттєвою перевагою комбінованих препаратів на синтетичних основах є можливість одночасного впливу на різні ланки патологічного процесу у відповідності до основних задач місцевого лікування ран.
ХАРАКТЕРИСТИКА ОСНОВ ПРЕПАРАТІВ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ РАН
Ефективність місцевого лікування ранового процесу визначається:
- раціональним вибором діючих речовин;
- лікарською формою препарату;
- сорбційними характеристиками основи
В останні роки, підвищення ефективності лікування та профілактики гнійно-запальних ран стало можливим завдяки широкому впровадженню в хірургічну практику лікарських засобів, яких створено на принципово нових комбінованих основах.
Це уможливлює цілеспрямоване надання необхідних властивостей препаратам, зокрема – керування інтенсивністю та напрямком процесу дифузії при аплікаціях препаратів на рану з метою їх диференційованого застосування у різних стадіях ранового процесу.
В результаті, при накладанні пов’язок між препаратом та ушкодженою тканиною швидко створюється осмотична рівновага, яка запобігає зневодненню тканин рани та водночас рановий вміст ефективно поглинається основою, при цьому діючі речовини препарату ефективно проникають навіть у глибокі шари рани.
Наявність осмотичної рівноваги необхідна як у фазі ексудації (мал.І-В), так і в фазі регенерації чи репарації (мал.І-Г). Різниця – тільки в її інтенсивності.
Порівняльна характеристика сорбційної та проникної спроможності різних основ препаратів для місцевого лікування ран
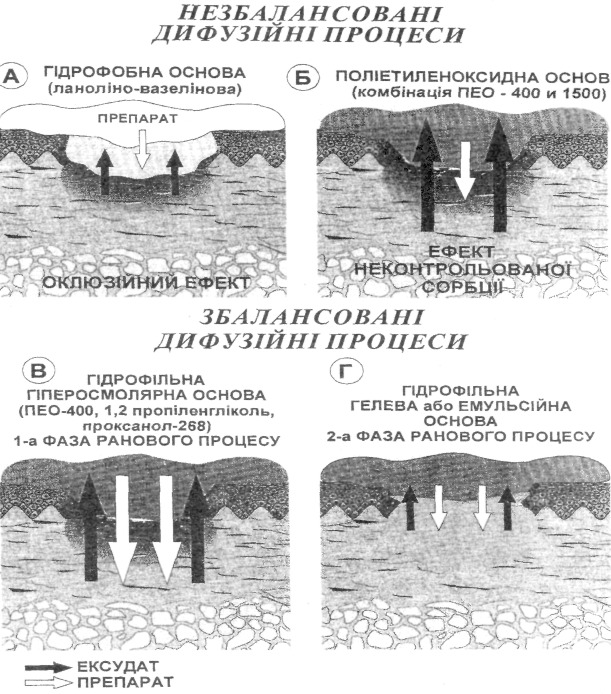
В сучасних багатокомпонентних препаратах застосовується гідрофільна основа, яка є водорозчинною сумішшю розчинників та полімерів -поліетиленоксиду-400 (ПЕО-400), 1,2-пропіленгліколю та проксанолу-268.
ПЕО-400 – є водорозчинним похідним етилену та володіє низькою токсичністю і вираженими осмотичними властивостями. Він добре наноситься на ранову поверхню, рівномірно на ній розподіляється, що покращує контакт мазі з тканинами та вмістом рани, добре змішується з рановим ексудатом. Характеризується повільною дифузією всередину клітин. Молекули ПЕО-400 спроможні проникати вглибину тканин, де вони розподіляються вже через 2 години після застосування препарату. Створюючи комплекси із протимікробними сполуками, ПЕО-400 проводить їх вглибину ушкоджених тканин – основних місць локалізації мікробів. Це принципово відрізняє препарати, створені на основі ПЕО, від мазей на жирових основах, які не впливають на глибинну мікрофлору.
Важливою особливістю ПЕО є опосередкована некролітична дія, яка приводить до відторгнення некротичного струпу за рахунок проникнення у мікрощелини на периферії зони відторження і збільшення там об’єму рідовини, яка розсуває змертвілі тканини.
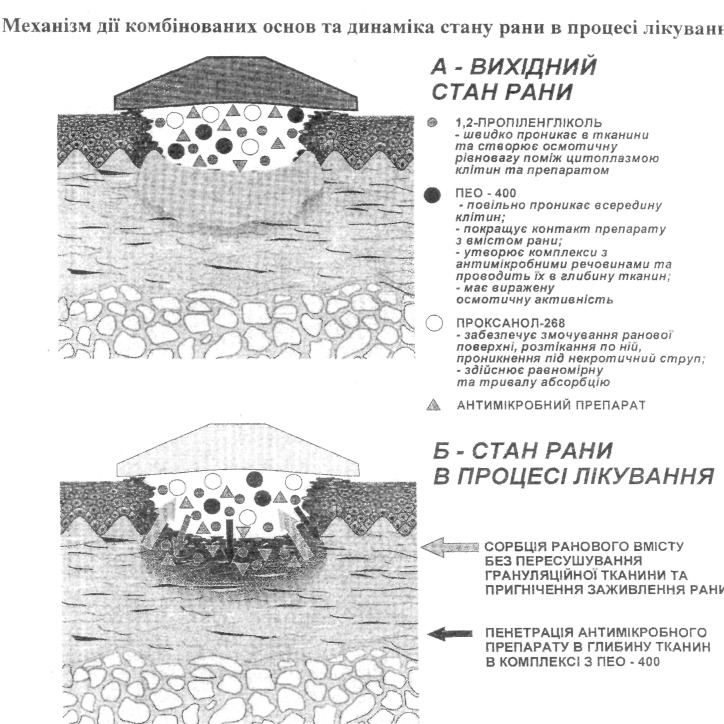
1,2-пропіленгліколь – є низькомолекулярною сполукою, яка швидко проникає у клітини і, таким чином, створює осмотичну рівновагу поміж цитоплазмою клітин і препаратом. Після нього до клітин проникає ПЕО-400, де його завдання – тривала та висока абсорбція ранового вмісту. Проксанол-268 – забезпечує більш рівномірну та тривалу абсорбцію (ніж ПЕО -1500, що входить у склад «Левосину» та «Левомеколю»). Він має кращі поверхнево-активні властивості – змочування ранової поверхні, розтікання по ній, проникнення під некротичний струп. Таким чином, застосування комбінації ПЕО-400, пропіленгліколю. проксанолу дає змогу регулювати силу осмотичної дії, забезпечувати ефект контрольованої сорбції та водночас захищати життєспроможні клітини рани від надмірної втрати ними води.
Основні переваги сучасних гідрофільних полімерних основ:
- залежно від стадії ранового процесу – виражена абсорбуюча активність (яка істотно перевищує за силою і тривалістю дії активність 10% хлориду натрію) або помірна осмотична дія;
- легкість нанесення на ранові поверхні та добра проникність в тканини;
- швидка розчинність антибактеріальних препаратів на синтетичній основі;
- здатність до посилення антимікробного ефекту та розширення спектра дії протимікробних засобів, які введено до складу препаратів;
ПРЕПАРАТИ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ В І-й ФАЗІ РАНОВОГО ПРОЦЕСУ
Основні вимоги:
- широкий спектр антимікробної дії що обумовлено:
- поліморфністю мікроорганізмів в осередках ураження;
- наявністю шпитальних штамів бактерій;
- полірезистентністю до багатьох антибіотиків;
- відносно тривалими термінами ідентифікації збудників гнійно-запальних процесів та встановлення їх чутливості до хіміопрепаратів;
- місцевоанестезувальна та протизапальна дія;
- гідрофільна гіперосмолярна основа, яка спроможна поглинати рановий ексудат до 350-600 % на протязі 20-24 годин;
- препарати не повинні визивати осмотичного шоку здорових клітин;
- відсутність місцевоподразнювальної та алергізуючої дії;
- відновлення мікроциркуляції в рані, стабілізація клітинних мембран;
- добре розтікання по рановій поверхні, змочування її та проникнення в ранові порожнини;
- інгібіція протеолітичних ферментів для попередження вторинних некрозів.
В І-й фазі – гнійно-некротичній у зв’язку з наявністю больового синдрому, некротичних тканин та гнійного ексудату в рані, вираженій інфільтрації, високого рівня бактеріальної забрудненості доцільно застосування препаратів, які здійснюють комбіновану дію – антимікробну, знеболюючу, дегідратуючу та протизапальну. Більшість традиційних водних або спиртових розчинів (таблиця) не відповідає сучасним вимогам, що обумовлено односпрямованою, переважно – корткочасною протимікробною дією, відсутністю осмолярної та знеболювальної активності. Це зумовлює низьку якість лікування ран, значні додаткові витрати
| Препарат/ Форма випуску | Особливості застосування |
| Хлоргексидину ; біглюконат* Розчин 0,05%, флакон по ЮОмл | Ефективен щодо грам «+» та «- » мікроорганізмів, дріжджів, дерматофітів та ліпофільних вірусів. Не діє на спори та віруси. Застосовується для обробки опера-ційного поля, рук, стерилізації інструментарію. Не можна поєднувати з йодом, милами, аніонними детергентами. Сухість шкіри, дерматити. Протипоказане тривале застосування. Відсутні осмолярна та пенетруюча активності. |
| Перекис водню* Розчин 3%, флакони по 25,40 мл | Застосовується лише для механічного очищення невеликих поверхневих ран, інактивації органічних сполук (білків, крові, гною). Слабка антисептична дія. тимчасове зменшення кількості мікроорганізмів. Швидко втрачає акшвшсть. Відсутня осмолярна та пенетруюча активність. |
| Фурацилін* Розчин,флакони по 10 та 25 мл | Активен переважно пито грам «+» мікроорганізмів (стафіло-. сгрептококків та інш.). Висока резистентність грам «-» флори, палички синьо-зеленого гною. Нетривала дія. Залежність активності від Рн рани. Слабка сорбційна активність. |
| Димексид* Розчин, флакони по 50 та 100 мл | Протимікробна, протизапальна та помірна анестезуюча дія. Проводе лекарські препарати вглибину тканин. Підвищує токсичність інших лікарських речовин. Швидко висихає, що травмує здорові тканини. Необхідно накривати салфеїки поліетіленовою плівкою та робити перев’язки декілька раз на добу. Не застосовують при надмірної гідратації тканин. Неприємний запах, алергічні реакції. |
| Діоксидин* Розчин для ін’єкцій 1% | Діє на резистентні штами мікроорганізмів, зокрема стафіло-, стрептококів, протею, синьогнійної палички, анаеробів (зокрема збудників газової гангрени). Місцеве застосування водного розчину обмежене, що обумовлено дозозалежним зростанням токсичності а також непереносимістю у багатьох хворих Застосування препарату здійснюється під пильним наглядом лікаря. Відсутня осмолярна активність. Нетривала (до 6-8 годин) поверхнева протимікробна дія. |
| Повідон-йод (Бетадин*, Вокадин) Розчин, флакони по З0 – 1000 мл | Бактерицидний ефект обумовлено окисленням мембранних та внутрішньоклітинних структур. Не визиває подразнення шкіри алергізацн, менш токсичний ніж звичайні препарати йоду. Вузький спектр активності, яка обмежується протимікробним ефектом, переважно щодо поверхневої мікрофлори. Відсутність впливу на важливі ланки – гіпергідратацію, ацидоз, порушення мікроциркуляції. Не можна призначати у комплексі з ензиматичними мазями. |
| Мікроцид* Розчин 40 Ед, Флакони по 100мл | Антибіотик групи пеніциліну. Активен по відношенню до окремих грам «+» І а грам «-» мікроорганізмів. При застосуванні з іншими препаратами для місцевого лікування ран швидко втрачає активність. При порушенні герметичності упаковки необхідно використати препарат протягом 3-х діб. |
| Левоміцетин* Розчин спиртовий 0,25%, Флакони по 5, 20, 25 мл | Активен по відношенню до грам «+ «-стафіло- (окремі штами), стрепто- та грам «- » аеробних коків (гоно-, менінгоків); а також Е. СоК, гемофільна паличка, клебсієла. Слабка активність щодо кислото-стійких бактерій, клостридій, простіших. Резистентність до Pseudomonas aerugmosa -100%, Staph Aureus -74,8%, Enterobacter – 90,9%, Proteus – 68,4%. Протипоказаний при лікуванні інфекційно ускладнених ран змішаної (мікробно-грибкової) етіології. |
| Примітка: * – тут, та в наступних таблицях відмічено препарати, яких внесено до наказу Міністерства охорони здоров’я України N 479 “Про внесення змін до Переліку лікарських засобів вітчизняного та іноземного виробництва, які можуть закуповувати заклади й установи охорони здоров’я, що повністю або частково фінансуються з державного та місцевого бюджетів” |
| Препарат | Склад та форма випуску | Особливості застосування |
| Йоддицерин* | Йод-5 г/л; ДМСО-300 г/л; Глицерол-695 г/л; Розчин, флакон по 25 мл | Володіє бактерицидною та вибірковою противірусною активністю. Проявляє активність щодо простіших. Подразнююча дія йоду на шкіру та слизові оболонки, виражений больовий синдром при нанесенні. Застосування неімобілізованого (на полімерних носіях) йоду може призвести до развитку йодизму. Відносно висока бактерицидна експозиція. Обмежений термін застосування (протягом 3-4 діб), що обумовлено можливим ушкодженням здорових тканин, які оточують рану. Можлива комулятивна дія. Необхідно попередньо розводити ізотонічними розчином натрію хлориду при введенні в порожнини. Доцільно застосовувати тільки після купірування гідратації тканин. Підвищенна чутливість, алергічні реакції, сухість шкіри, дерматити. |
| Фукорцин* | Кислота борна 0,8%; Фенол 3,9%; Резорцинол 7,8%; Ацетон 4,9%; Фуксин основний 0,4%; Спирт етіловий 9,6 %; Розчин, флакон по 25 мл | Проявляє помірну антисептичу дію. Добре проникає через шкіру та слизові оболонки. Кислота борна повільно виводиться та спроможна накопичуватись у організмі. У зв’зку з побічними ефектами має обмеження до застосування. Фенол володіє бактерицидною активністю щодо вегетативних форм мікроорганізмів; на спори не діє. Визиває сильну подразнюючою та припікаючу дію. Препарат швидко всмоктується і тому не застосовується на велики площах ураження шкіри та слизових оболонок. |
| Ектеріцид* | Водорозчинні продукти окислення риб’ячого жиру. Рідина, флакон по 250 мл | Відсутня обьєктивна інформація щодо антибактеріального спектру. Низька ефективність при глибоких ранах. При лікуванні ран відкритим способом необхідно зміщувати з новокаїном, що вносить додаткові незручності при застосуванні. |
Комбіновані розчини з протимікробною активністю на спиртових, водних або жирових основах, в залежності від складу того чи іншого препарату, мають багато недоліків, які притаманні попередній групі препаратів – недостатній спектр протимікробної активності, обмежені можливості при лікуванні великих (або глибоких) ранових процесів, необхідність комбінувати з системними засобами лікування.
За цих умов, в залежності від вираженості больового синдрому, ступеня ексудації та характеру мікрофлори доцільне застосування комбінованих препаратів на сучасних гідрофільних основах – розчину Діоксизоль або мазі Офлокаїн. Препарати забезпечують подвійну знеболювальну дію (місцевоанестезувальна та пригнічення продукції медіаторів болі), тому на відміну від анестезину, новокаїну, лідокаїну купірують больовий синдром на протязі 24 годин.
Критеріями призначення розчину Діоксизоль (завдяки введенню до його складу 6 % лідокаїну та полімерної гідрофільної водорозчинної основи, яка сорбує до 300-350 % рідини на добу) є виражений больовий синдром на тлі помірної інфільтрації та гнійної ексудації, а також II фаза ранового процесу за наявності зон некрозу та запалення.
Розчин Діоксизоль є препаратом вибору щодо грамнегативних мікроорганізмів з родини Enterobacteriaceae та роду Pseudomonas, й особливо – синьогнійної палички.
Етіологічна роль цих збудників у розвитку тяжких хірургічних інфекцій останнім часом значно зросла. Встановлено, що ці збудники стійкі до більшості антибактеріальних препаратів, що обумовлює доцільність застосування розчину Діоксизоль-Дарниця перш за все для профілактики та місцевого лікування ранової госпітальної інфекції.
Бактеріцидний ефект препарату Діоксизоль-Дарниця обумовлений здатністю діоксидину активізувати процеси перекисного окислення. Препарат порушує біосинтез ДНК, спричинює глибокі структурні зміни в цитоплазмі мікробних клітин, що призводить до їх загибелі. Зазначений механізм практично виключає можливість розвитку резистентності мікроорганізмів.
| Препарат | Склад та форма випуску | Особливості застосування |
| 1. На сучасних синтетичних гідрофільних основах | ||
| Діоксизоль* | Діоксидин – 1,2%; Лідокаїн – 6%; Синтетична осмолярна основа Розчин, Флакони по 1 00 мл | Тривала бактерицидна дія щодо грам «-» та грам «+» мікроорганізмів, аеробної та анаеробної, спороутворюючої та аспорогенної мікрофлори (синьогнійної палички, стафілококів, стрептококів, клостридій, бактероїдів, пептококів та інш), мікробних асоціацій, в тому числі госпітальних штамів з резистентнісіью до інших протимікробних препаратів. Препарат вибору для лікування грам «-» госпітальної інфекції, хронічних гнійно-запальних та об’ємнопорожнинних процесів. Доцільне застосування в фазі альтерації при помірній ексудації та вираженому больовому синдромі. |
| Офлокаїн* | Офлоксацин- 0,1%; Лідокаїн – 3% Синтетична гіперосмолярна основа (поліетиленоксид, проксанол-268, пропіленгліколь) Мазь, туба 15,30г, банка 1000г | Протимікробна дія щодо аеробних грам «-» мікроорганізмів, внутрішньоклітинних мікробів та мікробних асоціацій, у тому числі госпітальних штамів з полі-резистентністью до антибіотиків. Доцільне застосування в фазі альтерації при вираженій ексудації та помірному больовому синдромі; на догоспітальному етапі допомоги; при масових ураженнях для “консервування рани”, для відкладання первинної хірургічної обробки до 48 годин. Дозволяє відмовитись від додаткового прийому антибіотиків та анальгетиків або знизити їх застосування. Кратність застосування – 1-2 рази на добу. |
| 2. На синтетичних основах першого покоління | ||
| Левосин* | Левоміцетин- 1,0 %; Сульфадиметок-син-4,0%; Метилурацил-4,0 %; Тримекаїн-3,0 %; Полиетеленоксидна основа (ПЕО 400 та 1500 у співвідношенні 4:1) Мазь, туба 40 г | Відноситься до першого покоління препаратів на синтетичних основах. Низька активність щодо кислотостійких бактерій, клостридій, простіших. Резистентність до Pseudomonas aeruginosa становить 100%, Staph. Aureus 74,8%, Enterobacter – 90,9%, Proteus – 68,4%. Незбалансована основа з переважно односпрямованою дифузією (із рани в мазь), призводе до надмірної дегідратації, пересушуванню неуражених тканин. Можливе порушення барьєрної функції клітинних мембран, що призводе до швидкого проникнення хіміотерапевтичних речовин у системний кровотік. Має відносно низькі поверхневоактивні властивості. Протипоказами є супутні захворювання шкіри (псориаз, екзема та інш.), грибкові захворювання, інфекційне ускладнені рани змішаної (мікробно-грибкової) етіології. |
| 3. На жирових основах | ||
| Фастин-1* | Фурацилін – 2%; Хлорамфенікол – 1 ,6%; Анестезин – 3%; Жирова ланоліно-вазеліно-стеаринова основа. Мазь, туба 15г, банка ЗО г | Висока резистентність грам «-» мікроорганізмів, особливо палички синьо-зеленого гною. Низька активність щодо кислотостійких бактерій, клосіридій, простіших. Помірна та нетривала знеболююча активність. Можливі порушення відтоку рановою ексудату. Погане вивільнення діючих речовин. Розвиток оклюзійного ефекту. Нетривала дія (до 3-4-х годин). |
У порівнянні із водним розчином діоксидину препарат Діоксизоль діє в 3 рази триваліше, не має дозозалежного зростання токсичності. Добре розтікається по рановій поверхні, проникає в осередок ураження, ранові порожнини. Застосування препарату особливо доцільне у тих клінічних ситуаціях, коли існує складність проведення повноцінної ревізії гнійної рани, що обумовлене анатомотопографічними особливостями зони хірургічного втручання (локалізація процесу в ділянці судинно-нервових пучків, суглобових сумок та ін.), наявністю глибоких ран складної конфігурації з заглибинами, гнійними карманами й некротичними секвестрами.
Препарат потребує застосування лише 1 раз на добу. Загальна кількість розчину при місцевому застосуванні не перевищує 100 мл на добу, а при введенні в порожнини – 50-60 мл. Важливо, що пов’язка з препаратом не травмує ранову поверхню (не пересушує рану та не прилипає до неї).
Препарат Офлокаїн показаний при помірному больовому синдромі (так як місцевий анестетик лідокаїн, введений до складу в більш низький 3%-й концентрації) на тлі сильної інфільтрації тканин та вираженій гнійній ексудації (препарат проявляє гіперосмолярну активність, сорбуючи на протязі доби до 600% ексудату).
Завдяки офлоксацину – протимікробному засобу фторхінолонового ряду, препарат Офлокаїн має широкий спектр бактеріцидної дії, зокрема на аеробну грамнегативну мікрофлору, внутрішньоклітинних мікроорганізмів та мікробних асоціацій (особливо шпитальних штамів із полірезистентністью до антибіотиків (таблиця).
| Препарат | Резистентні штами, % | |||
| PSEUDOMONAS AERUGINOSA | STAPHYLOCO-CCUS AUREUS | PROTEUS SPP. | ENTERO-BACTER SPP | |
| Офлокаїн | 4,4 | 3,9 | 4,7 | 4,5 |
| Мазь гентаміцинова | 42,2 | 22,3 | 5,3 | 12,1 |
| Мазь левоміцетинова | 100 | 74,8 | 68,4 | 90,9 |
Таким чином, доцільність застосування препаратів Діоксизоль та Офлокаїн в І-й фазі (підфазі альтерації) ранового процесу, визначається наступними основними чинниками:
- варіабельністю больвого синдрому;
- введенням до складу ефективних протимікробних засобів широкого спектру дії сильного антисептику діоксидину або сучасного фторхінолонового похідного – офлокаїну;
- емпиричним характером протимікробної терапії за умов високого рівня мікробної забрудненості рани на даній стадії лікування.
Застосування препаратів на жирових ланолин-вазелинових або емульсійній основах (таблиця) при гнійній ексудації протипоказано, оскільки вазелінова основа володіє оклюзійним ефектом, а емульсійна – не забезпечує гіперосмолярну дію та не абсорбує гнійний ексудат. Крім того, сам склад цих мазевих основ є суттєвою перепоною для вивілнення діючих речовин (протимікробних, знеболюючих, протизапальних та ін.) з препарату.
Таким чином застосування препаратів на жировій в сучасній клінічній хірургії недоцільне, що обумовлено порушенням відтоку ранового ексудату, поганим вивільненням діючих речовин, розвитком окклюзійного ефекту, нетривалою дією (до 3-4-х годин). Це призводе до суттєвого зниження ефективності лікувального процесу, зростання термінів госпіталізації, додаткових витрат на лікувальні засоби.
| Препарат | Склад та форма випуску | Особливості застосування |
| Гентаміцин* | Гентаміцину сульфат- 0,1% або 0,3%; Жирова (вазелін-ланолінова) основа Мазь, крем туба 15 г-40г | Бактеріцидний ефект щодо грам «-» аеробних мікроорганізмів E.coli, Enterobacter, Klebsiella, Proteus, Acientobacter, H. influenzae), а також окремих штамів грам «+» аеробних коків. Резистентні: грам «+»: стрептококи груп A,B,C,G; стафілококи: Staph. Aureus (резистентні штами); Staph.epidernudis (+-). Гр «-» : N.Gonorrhoeae, Aeromonas; анаероби. Резистентність до Pseudomonas aeruginosa сягає 42,2%, Staph.Aureus – 22,3%, Enterobacter 12.1%, Proteus – 5,3%. Протипоказано тривале застосування на великих ранових поверхнях (можливі резорбція та розвиток нефротоксичного ефекту). |
| Синтоміцин* | Хлорамфенікол -5% або 10% Жирова основа (касторова олія) Лінімент, мазь туби, банки 20, 25 г | Група левоміцетину. Активен щодо окремих штамів грам «+» – стафіло-, стрепто- та грам «-» аеробних коків (гоно-, менінго-); деяких бактерій (Е.Соїі, гемофільна паличка, клебсієла). Активен щодо штамів, стійких до пеніциліну, стрептоміцину, сульфаніламідам. Слабка активність щодо кислотостійких бактерій, клостридій, простіших.Резистентність щодо Pseudomonas aerugmosa сягає 100%, Staph. Aureus – 74,8%, Enterobacter – 90,9%, Proteus – 68,4%. |
| Еритроміцин* | Еритроміцин- 1 % Жирова (вазелін-ланолінова) основа Мазь, туба 15 г | Вузький спектр дії. Активен переважно щодо грам «+» мікроорганізмів (стафіло-, стрептококів). Швидко розвивається резистентність, зокрема – перехресна. Як і інші макроліди, накопичується у фагоцитуючих клітинах. |
| Стрептоцид* | Сульфаніламід -5% або 10% Жирова (риб’ячий жир або вазелін) основа Лінимент, мазь туба 15 -30г | Має найменшу протимікробну активність в групі сульфаніламідних препаратів, частіше визиває побічну дію. не Відсутня бактеріостатична дія щодо більшості збудників ранової інфекції (Staph. Aureus, Proteus, Pseudomonas aerugmosa, Cl. Perfrmgens). Застосування при рановій інфекції вкракрай обмежано, так як у присутності гною, некротичних тканин, які містять велику кількість параамінобензойної кислоти, активність майже не проявляється. |
| Метронідазол (метрогіл) | Метронідазол- 10 % Гель, туба ЗО г | Вузький спектр протибактеріальної дії – тільки на збудників анаеробної клостридіальної та неклостридіальної інфекції (не діє на аеробну й факультативну анаеробну мікрофлору – St. aureus, E. coli, Pr. vulgaris, Ps. aerugmosa й др.). Необхідно поєднувати з антибіотиками, які активні щодо аеробних мікроорганізмів. |
| Полімиксин* | Полімиксин М сульфат- 10000 Од\г Лінімент, банка 15г | Група циклічних поліпептидів. Активні щодо переважно грам «-» збудників (E.Coli, Pseudomonas aerugmosa). Діє на внутрішньоклітинні мікроорганізми. Не діє на кокові аеробні мікроорганізми (стафіло-, стрепто-, гоно- та інш), анаеробні мікроорганізми, більшість штамів Proteus, клостридії та гриби. |
Останнім часом спостерігаються випадки призначення (рекомендації) препаратів природного походження на жировій основі, які набули певної популярності завдяки не своїм лікувальним властивостям, а масованій рекламі.
| Препарат | Склад та форма випуску | Особливості застосування |
| Спасатель | Природні компоненти: ефірні олії, вітаміни, облепихова олія, бджолиний воск, нафталан. Жирова основа. Бальзам, туба ЗО г | Не має прямої протимікробної та анестезувальної дії. Застосування при рановій інфекції вкракрай обмежано, так як у присутності гною, некротичних тканин активність препарату майже не проявляється. Низька трансдермальна проникненість. |
| Альгофін* | Природні компоненти: натрієвих солей жирних кислот, каротиноїдів, похідних хлорофілу. Жирова (вазелін-ланолінова) основа 25 г | Обмежані лікувальні властивості. Доцільне застосування тільки при невиликих поверхневих ранах, за відсутності значного ранового ексудату, гною, високого супеню мікробної забрудненості. Відсутня об’єктивна інформація щодо протимікробної активності. |
Примітка: ** – бальзам “Спасатель” зареєстровано як косметичний засіб, а не як лікарський препарат
Треба підкреслити, що склад даних засобів не відповідає заявленому в інструкціях спектру дії і тому їх застосування не узгоджується із сучасним принципам профілактики та лікування ранового процесу на всіх його фазах, в тому числі у амбулаторних умовах, після виписки пацієнта із стаціонару.
Після купірування больового синдрому (в перші 1-4 доби після хірургічної обробки рани), основною ланкою патогенезу ранового процесу, поряд із збереженням високої мікробної забрудненості, є виражена гіпергідратація тканин (підфаза ексудації), яка, за умов неадекватної лікувальної тактики, може призвести до поглиблення порушень живлення тканин з наступним розвитком некрозів. В цьому зв’язку, доцільно застосування комбінованих препаратів на гідрофільній синтетичній основі (таблиця), які мають сильний та тривалий дегідратуючий ефект на протязі доби.
Серед зазначених засобів, препарат Левомеколь має певні обмеження до застосування, що зумовлено незбалансованою основою з переважно односпрямованою дифузією (із рани в мазь), яка призводе до:
- надмірної дегідратації, пересушуванню неуражених тканин;
- порушенню барьєрної функції клітинних мембран;
- швидкого проникнення хіміотерапевтичних речовин у системний кровотік.
Крім того до антибіотику левоміцетину, який входе до складу препарату Левомеколь існує висока резистентність основних збудників ранової хірургічної інфекції, яка сягає 70%-100%.
Цих недоліків не мають сучасні препарати на удосконалених основах -мазі Нітацид та Мірамістин. Препарати мають виражену та тривалу гіперосмолярну дію, абсорбуючи протягом доби до 600% рідини. Завдяки цьому вони в короткі терміни купірують рановое та перифокальне запалення, поглинають гнійний ексудат та вибірково зневоднюють некротичні ткани. При цьому препарати не ушкоджують грануляції та життєздатні клітини.
Оптимальна комбінація нітазолу (2,5%) та стрептоциду (5,0%), дозволяє розглядати мазь Нітацид-Дарниця як препарат вибору для місцевого лікування неклостридіальної анаеробної інфекції (пептококи, пептострептококи) у асоціаціях з аеробами та факультативними анаеробами (стафілококом, кишковою паличкою та ін.).
Завдяки широкому спектру протимікробної дії, Нітацид повинен замінити низькоефективні мазі стрептоцидову, лінімент стрептоциду а також препарати на основі метронідазолу, які мають досить обмежену дію (тільки на анаеробну флору).
Препарат Мірамістин, який містить сучасний катіонний антисептик мірамістин, показаний при змішаних бактеріальних, грибкових та вірусних інфекціях. Незамінний при тяжких та тривалих за перебігом гнійно-запальних ранових прооцесах (особливо у послаблених хворих, при різкому порушенні резистентності організму, при великих та глибоких ранах, у хворих похилого віку). Важливим є те, що період призначення цих препаратів (в середньому 3-7 доба лікування) співпадає з результатами бактеріологічного дослідження складу мікрофлори та встановлення її чутливості. Це дозволяє провести диференційоване призначення препаратів Нітацид або Мірамістин.
Диференційоване призначення сучасних комбінованих препаратів Діоксизоль або Офлокаїн, відразу після хірургічної обробки рани, забезпечує етіотропну терапію та швидке купірування больового синдрому на протязі 1-4-ї доби лікування, що дозволяє зменшити дозу або відмовитись від додаткового застосування аналгетиків та антибіотиків.
Після купірування больового синдрому, у підфазі ексудації доцільне застосування препаратів Нітацид або Мірамістин. У порівнянні з традиційним лікуванням мазями на жирових основах або препаратами Левомеколь/Левосин, застосування Нітациду або Мірамістину є патогенетичне виправданим, що дозволяє:
- на 2-5 діб скоротити терміни нормалізації загального стану та лабораторних показників;
- до 50% підвищити ефективність ліквідації перифокального набряку та інфільтрації тканин;
- на протязі 1-ї фази забезпечити достатній протимікробний ефект, який обумовлено високою чутливістю патогенних штамів, у тому числі внутрішньолікарняних (у середньому -94%, в той час як до мазей Левосин/Левомеколь нечутливі від 30% до 48% госпітальних штамів).
- на 2-4 доби скоротити терміни очищення рани від гнійно-некротичних тканин;
- наприкінці 2-4 доби лікування досягти зниження мікробного обсеменіння рани нижче критичного рівня; до 5-11 доби (в залежності від збудника) досягти практично повної санації рани.
| Препарат | Склад та форма випуску | Особливості застосування |
| Нітацид* | Нітазол-2,5% ; Стрептоцид-5 ,0% Синтетична гіперосмолярна основа (поліетиленоксид, проксанол-268, пропіленгліколь) Мазь, туба 15, ЗО г, банка 1000г | Розширений спектр протимікробної дії (щодо стафілококів, стрептококів, кишкової палички, палички синьо-зеленого гною, протею, облігатних анаеробних бактерій – бактероїдів, пептококів, пептострептококів). Має протистоцидну дію на простіших, зокрема трихомонади. Препарат ефективен щодо госпітальних штамів бактерій із полірезистентністю до антибіотиків Має виражену гіперосмолярну та протизапальну активність. Показаннями до застосування в 1-й фазі ранового процесу є: – анаеробна та змішана аеробно-анаеробна інфекція рани; – інфіковані рани м’яких тканин із вираженою гнійною ексудацією; – ексудативно-запальні захворювання шкіри, які ускладнені піодермією; – хронічні ранові процеси (трофічні виразки та інш.). |
| Мірамістин* | Мірамістин- 0,5% Синтетична гіпер-осмолярна основа (поліетиленоксид, проксанол-268, пропіленгліколь) Мазь, туба 15, ЗО т, банка 1000 г | Виражена антисептична дія при змішаних бактеріальних, грибкових та вірусних інфекціях, а також трепонемо-гонококко- й трихомоноцидних інфекціях. Володіє вибірковою дією щодо патогенних мікроорганізмів, попереджує їх резистентність. Показаннями до застосування в 1-й фазі ранового процесу є: – початковий етап лікування інфекційне ускладнених ран до ідентифікації збудників; – виражена гнійна ексудація; – змішані бактеріально-грибкові або вірусні інфекції |
| Левомеколь* | Левоміцетин -0,75 % Метилурацил- 4,0 % Поліетеленоксидна основа (ПЕО 400 та 1500 у співвідношенні 4:1) Мазь, туба 40 г та 100г | Відноситься до першого покоління препаратів на синтетичних основах. Низька активність щодо кислотостійких бактерій, клостридій, простіших. Резистентність до Pseudomonas aeruginosa становить 100%, Staph. Aureus -74,8%, Enterobacter – 90,9%, Proteus – 68,4%. На відміну від препарату «Левосин» має менш тривалий протимікробний ефект. Незбалансована основа з переважно односпрямованою дифузією (із рани в мазь), призводе до надмірної дегідратації, пересушуванню неуражених тканин. Характерно порушення барьєрної функції клітинних мембран, що може призводити до швидкого проникнення хіміотерапевтичних речовин у системний кровотік. Має відносно низькі поверхневоактивні властивості Протипоказами є супутні захворювання шкіри (псориаз, екзема та інш.), грибкові захворювання. Інфекційне ускладнені рани змішаної (мікробно-грибкової) етіології. |
ПРЕПАРАТИ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ В ПЕРЕХІДНОМУ ПЕРІОДІ РАНОВОГО ПРОЦЕСУ
В процесі очищення рани від гнійно-некротичного вмісту та зниження мікробного обсіменіння, хірург стикається з непростою клінічною ситуацією, коли у окремих ділянках рани дозрівають грануляції, а в інших продовжується гнійна ексудація. Цей стан рани називається перехідним періодом поміж 1-ю та 2-ю фазами ранового процесу.
Основні задачі місцевого лікування:
- забезпечення помірної осмотичної активності (без ушкодження молодої грануляційної тканини), яка сприяє повному очищенню рани від гнійно-некротичного осередка;
- створення умов для скорішого переходу у ІІ-у фазу ранового процесу;
- широкий спектр протимікробної дії, для попередження вторинного нагноєння за рахунок власної мікрофлори або госпітальної інфекції;
- купірування ранового та перифокального запалення у тканинах за рахунок помірної дегідратуючої дії;
- підтримка життєспроможності ушкоджених тканин;
- відновлення мікроциркуляції;
- стабілізація клітинних біомембран;
- імуномодулюючий ефект
Виходячі з наведених задач, на даному етапі лікування доцільно застосування препарату Стрептонітол, який має помірну осмотичну активність (видаляє надлишок рідини, але не пересушує рани з млявим ексудатом), що сприяє повному очищенню рани від гнійно-некротичного осередка без ураження грануляцій та скорішому переходу до 2-ї фази ранового процесу. Починати лікування з препарату Стрептонітол доцільно за відсутності рясної ексудації (після розкриття флегмон та абсцесів, при лікуванні пролежин, трофічних виразок, діабетичних гангрен, бешихового запалення та ін.).
ПРЕПАРАТИ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ У ІІ-й ФАЗІ РАНОВОГО ПРОЦЕСУ
Друга фаза (фаза грануляцій) ранового процесу характерізується:
- суттєвим пригніченням вірулентності патогеної мікрофлори, зниженням її кількісних характеристик;
- згасанням запальної реакції;
- очищенням рани від гнійно-некротичного вмісту;
- ліквідацією перифокальної інфільтрації;
- досягненням бактеріологічної санації рани;
- появою грануляційної тканини.
Оперативне закриття ран шляхом накладання швів, або за допомогою автодермопластики показане за умов великих розмірів рани. Кваліфіковано та своєчасно виконана операція скорочує терміни заживлення рани, покращує результати лікування. Слід зазначити, що в сучасних умовах тільки обгрунтовані протипокази (важкий стан пацієнта, невеликі за розмірами рани) є підставою для відмови від оперативного закриття рани та призначення місцевого медикаментозного лікування препаратами, які відповідають основним вимогам для лікування ран у другій фазі ранового процесу.
Основні вимоги:
- надійний захист грануляційної тканини від механічного ушкодження та дії інших негативних чинників (висихання та ін.);
- профілактика вторинного інфекування рани, особливо шпитальними штамами патогенних мікроорганізмів;
- помірна підсушувальна дія;
- нормалізація обмінних процесів завдяки відновлення мікроциркуляції;
- направлена стимуляція репаративних процесів в рані.
В клінічній хірургії на даній фазі ранового процесу традиційно продовжують застосовуватись різноманітні за складом та властивостями препарати на гідрофобних (здебільшого вазелин-ланолінових основах) або незбалансованих синтетичних основах (таблиця). Більшість з наведених препаратів не відповідає сучасним вимогам, для оптимального заживлення ран у другій фазі ранового процесу, оскільки не володіють бактерицидною дією для попередження можливого вторинного інфікування, пригнічення вегетуючої
| Препарати, які стимулюють метаболічні процеси та регенерацію тканин | ||
| Препарат | Склад та форма випуску | Особливості застосування |
| Лінімент бальзамічний (за Вишневським)* | Дьоготь- 3%; Ксероформ- 3%; Гідрофобна основа (олія касторова)- 94% Лінімент, банка, туба по 25г,40г,100г та 2 кг | Помірний дезінфікуючий, протизапальний, місцевоподразнюючий ефект. Відсутня осмотична активнісь. Виключно поверхнева дія. Препарат не здатний очищувати рани від залишків гною та некротичних тканин, що уповільнює регенерацію ранового дефекту. При тривалому застосуванні можливе подразнення шкіри. |
| Вінілін (бальзам Шостаков-ського)* | Полівінілбутиловий ефір- 100г Рідина, флакон 100 мл; Лінімент, флакон 100 г | Є гідрофобною речовиною. Місцево застосовують 20% олійний розчин, що значно обмежує його всмоктування та проникнення у тканини. Немає даних щодо спектру протимікробної активності. Має специфічний запах. |
| Календула* | Настоянка календули- 10%; Жирова основа (емульсія вода\вазелин). Мазь, банка 40 г; Гель, туба 15г | Виключно поверхнева дія. Слабка антисептична та протизапальна дія. Відсутня осмотична активність. Застосовується тільки для лікування чистих поверхневих гранулюючих ран та опіків, невеликих тріщин. |
| Вулнузан | Екстракт маточників соляних озер 12%; Жирова основа (олія касторова, ланолин) Мазь, туба 45 г | Відсутні протимікробна та осмотична активність Доцільне застосування тільки для лікування чистих гранулюючих ран. |
| Аекол* | Ретинолу ацетат; Ретинолу пальмитат; а-токоферолу ацетат; Вітамін К3; Каротин Жирова основа (олія/вода) | Відсутні протимікробна та осмотична активність. Доцільне застосування тільки для лікування чистих гранулюючих ран. |
| Ацемін* | Кислота епсилон-аміно-капронова-22 1 ,8 г\л; Натрію гідрокарбонат-107,7г\л | Сприяє очищенню ран від некротичних тканин, зменшує ексудацію, прискорює регенерацію. Перед застосуванням необхідно очистити та продезінфікувати ранову поверхню. Не можна застосовувати при залишках гною та мікробній забрудненості рани. До протипоказів відноситься вагітність. |
| Метилурацил* | Метилурацил- 1 0% Жирова основа (ланолін\вазелин) Мазь, туба 15, 25, 30г | Відсутня протимікробна активність. Недоцільне застосування для профілактики вторинного інфекування рани. Жирова основа перешкоджає вивільненню та проведенню метилурацилу в тканини, створює умови для розвитку анаеробної інфекції у рані, особливо за умов повільного загоєння. |
| Мефенат | Мефенаміну натрієва сіль- 0,5%; Вінілін-10%; Синтетична основа (ПЕО) Мазь, туба 40г | Має помірний протизапальний, знеболюючий та протизапальний ефект. Немає даних щодо спектру протимікробної активності. Недоцільне застосування для профілактики вторинного інфекування рани. Незбалансова синтетична основа може призводити до пересушуванню тканин, печії, онемінню ураженої ділянки. |
Серед інших недоліків слід зазначити відсутність помірної підсушувальної дії. Більш того, часто спостерігається протилежний ефект – рана “розкисає”, що пов’язано з її герметизацією жировою основою.
| Препарати природного походження, які стимулюють регенерацію тканин | ||
| Препарат | Склад та форма випуску | Особливості застосування |
| Актовегич* | Гемодериват з телячої крові депротеінізо-ванний. Допоміжні речовини. Мазь, крем, гель – 20% Туба 20г Желе-10%, мазь-5%, гель-20% Туба 20г | Препарати містять амінокислоти. олигопептиди. нуклеозиди, мікроелементи, електроліти, продукти метаболізму ліпідів. Підвищують енергетичні процеси в клітинах шляхом накопичення глюкози та кисню, прискорення метаболізму АТФ. Монокомпонентні препарати, які мають досить обмежений спектр застосуванняпри гнійній рановій інфекції. Відсутність у їх складі протимікробних речовин обумовлює доцільність застосування тільки при «чистих» ранах. В інших ситуаціях необхідно призначення протимікробних засобів. Відносно висока ціна. |
| Солкосерил* |
Препарати природного походження (Актовегин, Солкосерил та ін.) є ефективними стимуляторами метаболічних процесів та регенерації тканин, але відсутність протимікробної активності суттєво звужує спект їх терапевтичної дії, який обмежено тільки “чистими” ранами.
За цих умов доцільне призначення комбінованого препарату Метилурацил, який містить метилурацил та катіонний антисептик мірамістин на синтетичній основі. Це дозволяє ефективно пригнічити можливе виникнення осередків гнійного запалення, а синтетична основа забезпечує добре вивільнення лікарських речовин, підсилює їх протимікробну та репаративну дію, створює помірний рівень дегідратації в рані.
| Препарат | Склад та форма випуску | Особливості застосування | |
| Метилурацил | Метилурацил – 5%; Мірамістин- 0,5%; Синтетична гідрофільна основа (пропіленгликоль, поліетиленоксид , проксанол) Мазь, туба 15г | Препарат забезпечує протекторну дію (захищає від механічної травми та висихання), попереджує вторинне інфекування, стимулює рост грануляційної тканини, проявляє імуномодулюючу дію. Особливо показаний при ранових процесах з млявим перебігом (в першу чергу – променевих та трофічних виразок, у хворих на діабетичну ангіопатію, опікових ран, у послаблених хворих з суттєвим пригніченням імунітету. Препарат має м’яку осмотичну дію, яка не впливає зростання молодої грануляційної тканини, але сприяє очищенню та підсушуванню рани. |
Таким чином, комбінована терапевтична дія та висока ефективність якісно вирізняє препарат Метилурацил від інших препаратів, зокрема -мазі метилурацила 10% на вазелин-ланоліновій основі, що дозволяє в 1,5-2 рази (в залежності від тяжкості патології) скоротити терміни заповнення ранового дефекту грануляційною тканиною.
ПРЕПАРАТИ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ У ІІІ-Й ФАЗІ РАНОВОГО ПРОЦЕСУ
Поряд з ростом грануляційної тканини в рані розвивається процес епітелізації, який здійснюється, переважно за рахунок проліферації клітинного епітелію, що оточує рану.
Пригнічення розвитку грануляцій призводе до затримки процесу епітелізації. Міцною епітелізація рани залишається лише у випадку, коли епітелій наростає на грануляційну тканину. В інших випадках він відмирає.
Лікування ран у ІІІ-й фазі (фаза епітелізації та реорганізації рубця) ранового процесу здійснюється за принципами, які багато в чому співпадають з принципами ліківання у другій фазі. Основні вимоги:
- ефективний захист грануляційної тканини від впливу негативних чинників (механічної травми, висихання та ін.);
- профілактика вторинного інфекування рани, особливо шпитальними штамами патогених мікроорганізмів;
- профілактика аномальної проліферації та диференціювання фібробластів з формуванням гіпертрофічних та келоїдних рубців;
- прискорення швидкості епітелізації та зниження інтенсивності контракції рани, особливо при великих за площею ранах;
- спрямована стимуляція та регуляція репаративних процесів в рані із забезпеченням оптимальних умов для реорганізації рубця (формування гладкої, еластичної рубцьової тканини якомога меншої площі).
Цим вимогам відповідають препарати на основі декспантенолу, який широко застосовується у світовій медичній практиці. Декспантенол швидко абсорбується шкірою, перетворюючись у пантотенову кислоту, що є складовою коферменту А, котрий у вигляді коферменту ацетил-КоА відіграє важливу роль в обміні речовин кожної клітини, зокрема сприяє:
- нормальному функціонуванню циклу трикарбонових кислот (доставка АТФ тканинам);
- оптимізації обміну жирних кислот, фосфоліпідів (які входять до складу клітинних мембран), синтезу ацетилглюкозамінів та мукополісахарідів (основних компонентів сполучної тканини), утилізації продуктів дезамінування амінокислот.
Виходячи з наведених властивостей, декспантенол забезпечує оптимізацію регенераторних процесів ділянки ураження з формуванням повноцінного регенерату (з упорядкованим розташуванням колагенових волокон та формуванням епітеліального шару із чітким диференціюванням його шарів).
| Препарати, які застосовуються у фазі епітелізації та реорганізації рубця | ||
| Препарат | Склад та форма випуску | Особливості застосування |
| Пантестин* | Декспантенол- 50 мг; Мірамістин-5 мг; Синтетична гідрофільна гелева основа Гель, туба 15г | Сприяє послабленню запальної реакції, інтенсифікує ріст грануляційної тканини та стимулює епітелізацію. Новоутворена тканина швидко набуває зрілого характеру. Забезпечує надійний протимікробний, протигрибковий та противірусний захист рани. Володіє імонумодулюючою активністю (підвищує тканову резистентність за рахунок стимуляції функціональної активності нейтрофільних гранулоцитів), що також сприяє зниженню бактеріального обсеменіння, кількості мікробних асоціацій. Попереджує пересушування рани. Гідрофільна гелева основа, сприяє пенетрації активних компонентів мазі без проникнення в системний кровотік, що призводе до пролонгуванню лікувальної дії. Завдяки позитивному впливу на процеси реструктуризації та стверднення рубця, забезпечує мінімальну площину, гладку поверхню та еластичну консистенцію рубцьової тканини. |
| Бепантен | Декспантенол- 50 мг; Хлоргексидину гідрохлорид-5 мг Крем, туба 30г Декспантенол- 50 мг; Мазь, туба 30г Декспантенол- 25 мг; Розчин, 200 мл | Хлоргексидин поступається за спектром дії мірамістину. Ефективен що грам «+» та «-» мікроорганізмів, дріжджів, дерматофітів та ліпофільних вірусів. Не діє на спори та віруси. Протипоказане тривале застосування при лікуванні гнійно-запальних процесів. Визиває сухість шкіри, дерматити. Препарати у вигляді мазі та розчину не забезпечують протимікробний захист рани. |
| Пантенол | Декспантенол Аерозоль 130 мг/г, Флакон, 140мл | Препарат не забезпечує протимікробний захист рани. |
Застосування препаратів, які стимулюють процеси епітелізації особливо доцільно при лікуванні ранових процесів з торпідним перебігом. В цих випадках стимуляція процесів репаративної регенерації призводе до скорочення термінів лікування, зменшення частоти ускладнень (зокрема інфекційних). Це стосується в першу чергу лікування променевих та трофічних виразок у хворих на діабетичну ангіопатію, опікових ран, послаблених хворих, пацієнтів із суттєвим пригніченням імунологічної реактивності. За цих умов застосування препарату Пантестин має певні перемоги, враховуючи його широкий спектр протимікробної активності.
Таким чином, препарат Пантестин доцільно застосовувати:
- для профілактики та лікування інфекційних ускладнень на кінцевих фазах ранового процесу та після виписки пацієнта із стаціонару;
- при лікуванні великих раневих поверхонь;
- за умов надшвидкого дозрівання грануляційної тканини із порушенням процесу колагеноутворення;
- для профілактики аномальної проліферації та диференціювання фібробластів з формуванням гіпертрофічних та келоїдних рубців.
6.7. ДОДАТКОВІ ГРУПИ ПРЕПАРАТІВ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ РАНОВОГО ПРОЦЕСУ
Для профілактики надлишкових грануляцій та при виражених рубцьових змінах країв рани доцільно застосовувати сучасні комбіновані кератолітичні та гормономістні препарати. Як кератолітичні засоби традиційно використовуються саліцилова, молочна, бензойна кислоти, сірка, резорцин, а також препарати на основі сечовини. Сечовина відрізняється нешкідливістю, бо є природним продуктом організму. До сучасних лікарських форм на основі сечовини належить крем Карбодерм на гідрофільній емульсійній основі, що містить 10% сечовини та антисептик цетилпіридинію хлорид.
| Препарат | Склад та форма випуску | |
| Мазь саліцилова* | Кислота саліцилова 2%, 5%, 1 0%, Жирова (вазелін-ланолінова) основа Мазь, банка 25 г |
| Розчин кислоти саліцилової | Спиртовий розчин кислоти саліцилової Флакони по 25 та 40 мл – 2%, |
| Карбодерм* | Сечовина- 10%; Цетилпіридинію хлорид -0,4%, Гідрофільна основа (пропіленгликоль) Крем, туба З0 г |
Навідміну від препаратів на основі саліцилової кислоти, крем “Карбодерм” може застосовуватись тривало та на великій площі ураження, оскільки він не подразнює шкіру, не порушує її функції, не проникає в організм.
Застосування топічних монопрепаратів глюкокортикоїдів (ГКС), хоча й має виражений протизапальний лікувальний ефект, проте може ініціювати розвиток вторинної бактеріальної та грибкової ранової інфекції. Саме тому є виправданою тенденція до поєднання глюкокортикоїдів з антибіотиками, антисептиками, протигрибковими засобами, кератолітиками.
| Препарат | Склад та форма випуску |
| Фокорт* | Триамцинолону ацетонид – 0,1%; Цитілпиридинію хлорид – 0,5% Гідрофільна емульсійна основа (олія вазелінова, пропіленгліколь, вода), Крем, туба 15г |
| Флуцар* | Флуоциналону ацетонід – 0,1%; Нипагін – 0,1%; Трилон-Б Гідрофільна емульсійна основа (олія вазелінова, пропіленгліколь, вода), Крем, туба 15 та ЗО г |
| Кортонітол* | Гідрокортизону ацетат – 1,0%; Нітазол – 2,0%; Гідрофільна емульсійна основа (олія вазелінова, пропіленгліколь, вода), Мазь, туба 1 5 г |
| Тримістин* | Триамцинолону гідрохлорид – 0,025%; Мірамістин – 0,5%; Гідрофільна основа (В-циклодекстрин, пропіленгликоль, вода) Мазь туба 14 г |
| Бетаметазону валерат* | Бетаметазону валерат – 0,1%; Цитілпиридинію хлорид – 0,4% Гідрофільна емульсійна основа (олія вазелінова, пропіленгліколь, вода) Крем, туба 1 5 г |
МЕТОДИКА ЗАСТОСУВАННЯ ПРЕПАРАТІВ ДЛЯ МІСЦЕВОГО ЛІКУВАННЯ РАНОВОГО ПРОЦЕСУ
Місцеве лікування ран проводиться після їх адекватної хірургічної обробки або (у подальшому) стандартного туалету (розчини сучасних антисептиків, перекис водню та ін.). Комбіновані препарати на сучасних синтетичних основах вводять в рану із тампоном, який просякнутий відповідним лікарським засобом, потім накладають тонким шаром на ранову поверхню. Поверх серветок накладають стерильну пов’язку, яку фіксують бинтом або лейкопластирем.
Перев’язки проводять 1 раз на добу. Кількість препарату на одну перев’язку визначається характером та розмірами рани й коливається від 6 до 30-40 грамів.
При лікуванні об’ємнопорожнинних гнійних утворень (піддіафрагмальний абсцесе, емпієма плеври, міжпетлевий абсцесе, остеомієлит та ін.) препарати підігрівають до З0″ та вводять у порожнину катетером за допомогою шприця або мікроеригатору у кількості від 5 до 20 мл 1 раз на добу.
При лікуванні запальних інфільтратів та флегмон м’яких тканин (у початковій стадії розвитку), враховуючи високі показники трансдермального проникнення при запаленні шкіри, доцільно застосовувати копреси із препаратами, що сприяє зворотному розвитку запального процесу.
Показаннями до відміни препаратів є:
- в першій фазі – повне очищення рани від гнійно-некротичного секвестру та її бактеріологічна санація;
- в другій та третій фазах – позитивна динаміка утворення грануляцій та епітелізації ранового дефекту.
ДОДАТКОВІ МЕТОДИ ЛІКУВАННЯ РАНОВОГО ПРОЦЕСУ
Стандартну методику хірургічної обробки гнійної рани, місцеве патогенетичне обгрунтоване лікування із застосуванням сучасних комбінованих препаратів в окремих випадках, доцільно доповнювати фізіотерапевтичними методами. У першій фазі ранового процесу застосовують кварцування ран, ультразвукову кавітацію гнійних порожнин, різні види зрошення, гіпербаричну оксигенацію, обробку ран високоенергетичним лазером.
Поряд з фізичними методами, певне значення мають біологічні засоби місцевого лікування (зокрема, застосування бактеріофагів при антибіотикостійкій мікрофлорі ран). Важливим є також застосування ферментних препаратів – хімопсину, хімотрипсину, террилітину, стрептокінази. Ці препарати визивають лізис некротизованих тканин, прискорюють очищення рани а також впливають на оболонки мікробних клітин, збільшуючи їх чутливість до антибактеріальних засобів, що використовуються.
КЛНІКО-ЕКОНОМІЧНА ЕФЕКТИВНІСТЬ ПОСЛІДОВНОГО ЗАСТОСУВАННЯ КОМБІНОВАНИХ ПРЕПАРАТІВ
Послідовне патогенетичне обгрунтоване застосування комбінованих препаратів на сучасних синтетичних гідрофільних основах для місцевого лікування ран дозволяє підвищити ефективність і скоротити тривалість лікування:
у І фазі – забезпечити тривале й швидке купірування больового синдрому на 1-2-у добу лікування (що дозволяє зменшити дозу чи відмовитися від додаткового застосування анальгетиків). У порівнянні з традиційним місцевим лікуванням або застосуванням препаратів Левомеколь/Левосин на 2-5 діб скоротити терміни нормалізації загального стану і лабораторних показників пацієнтів, ліквідації перифокального набряку та інфільтрації тканин, гнійного осередку та очищення рани; до кінця 2-ї доби забезпечити зниження мікробного обсеменіння рани нижче критичного рівня, а до 5-11 доби (у залежності від збудника) забезпечити повноцінну санацію рани.
у ІІ та ІІІ фазах – у 1,5-2 рази прискорити утворення грануляцій і термінів епітелізації рани (або термінів чергового етапу хірургічного лікування), у 94% випадків виключити імовірність повторного інфікування;
Таким чином, послідовне застосування комбінованих препаратів дозволяє поліпшити еффективность місцевого лікування ран (в 1,5-2 рази скоротити вартість і тривалість курсу лікування), що відбивається на показниках работи хірургічної служби в цілому (скорочення кількісті ліжко-діб, інфекційних ускладнень, показників інвалідності, смертності), а також сприяє раціональному використанню бюджетного фінансування.
АНТИБІТИКОПРОФІЛАКТИКА РАНОВОЇ ІНФЕКЦІЇ
Антибіотикопрофілактика (АП) – передопераційне введення антибіотиків з метою зниження ризику розвитку післяопераційної ранової інфекції.
Мікробна контамінація операційної рані практично є неминучою, навіть при ідеальному дотриманні правил асептики й антисептики. До кінця операції в 80-90% випадках рани контаміновано різною мікрофлорою, найчастіше стафілококами. Суть АП полягає в досягненні необхідних концентрацій антибіотиків у тканинах до моменту їх можливої мікробної контамінації і підтримка цього рівня протягом всієї операції та перших 3-4 годин після оперативного втручання. Доведено, що профілактичне призначення антибіотиків знижує частоту післяопераційного нагноєння ран та виникнення абсцесів з 25-30 % до 1-5 %.
ПРИНЦИПИ АНТИБІОТИКОПРОФІЛАКТИКИ
АП базується на наступних принципах:
- при проведенні АП не слід прагнути повної ерадикації бактерій. Значне зменшення кількості бактерій вже полегшує роботу імунної системи і запобігає розвитоку гнійної інфекції;
- ефективна концентрація антибіотика в операційній рані повинна бути досягнута до початку операції і зберігатися до її закінчення;
- в/в введення антибіотиків із профілактичною метою, як правило, здійснюється за 30-40 хв до початку операції;
- продовження введення антибіотика більш ніж через 24 г після операції не приводить до підвищення ефективності АП.
ПОКАЗАННЯ ДО ПРОВЕДЕННЯ АП
Враховуючи можливість негативного впливу антибіотиків на організм, їх профілактичне застосування повинне обмежуватися лише ситуаціями, при яких є обґрунтованим ризик виникнення ранової інфекції.
При чистих (асептичних) ранах післяопераційні ускладнення становлять не більш 1-5% випадків, тому антибіотики призначають тільки при операціях, коли розвиток інфекції може звести нанівець ефект складного оперативного втручання чи являти загрозу для життя і здоров’я хворого. До них, зокрема, відносяться:
- великі за обсягом операції;
- окремі відновні операції на судинах;
- будь-які чисті операції тривалістю більше 3-х годин.
При умовно чистих ранах, які супроводжуються контамінацією нормальною мікрофлорою хворого при проведенні планових операцій (зокрема на органах черевної та грудної порожнини, малому тазі) частота післяопераційних ускладнень досягає 7-9%, що є показанням до проведення АГІ.
Усі травматичні рани відносяться до бактеріальна забруднених ран, при яких частота ранової інфекції досягає 25% і вище. У цьому випадку введення антибіотиків повинно бути якомога раннім, а тривалість застосування обмежуватись 48-72 г, якщо перебіг захворювання не вимагає продовження антибіотикотерапії. При цьому необхідно контролювати ступінь контамінації рани шляхом кількісного визначення змісту мікробних тіл у рані (критичний рівень бактеріального обсеменіння -100 тис. мікробних клітин на 1 г тканини), при якому профілактика ранової інфекції повинна бути найбільш повною.
Значення профілактичного застосування антибіотиків зростає при відстроченій, пізній обробці рані чи у випадках, коли взагалі її неможливо зробити, а також в умовах, що сприяють ослабленню резистентності організму до інфекції (похилий вік, ожиріння, цукровий діабет і ін.) та при значному бактеріальному забрудненні рани, високій вірулентності інфекції, несприятливому стані контамінованих тканин.
Операші на інфікованих (брудних) ранах, при яких є гній, перфоровані органи або старі травматичні рани (частота післяопераційних ускладнень досягає 40%), вимагають, окрім адекватного місцевого лікування, проведення антибіотикотерапії. що обумовлює доцільність призначення препаратів перед операцією, під час операції й у післяопераційному періоді під бактеріологічним контролем стану рани.
ТЕРМІНИ ПРОВЕДЕННЯ АП
По тривалості розрізняють 4 схеми АП:
- профілактика однією дозою (під час премедикації; 2-а доза вводиться тільки при 3-х годинних та більш тивалих операціях);
- надкоротка (під час премедикації, потім 2-3 дози препарату протягом доби);
- короткочасна (за 1,5-2 годин до операції і протягом 48 годин – після операції);
- тривала (за 12 годин і більше до операції і кілька днів після операції).
Серед наведених схем АП найбільш доцільно застосовувати профілактику однією дозою та введення антибіотиків за надкороткою схемою. Така тактика цілком ефективна, так як знижує ймовірність побічних дій антибіотиків, більш низьку вартість лікування. Передчасне (за кілька годин до операції), чи запізніле введення першої дози антибіотика знижує ефект профілактики. Невиправдано тривале проведення АП, веде до збільшення частоти післяопераційних ускладнень. Це обумовлено тим, що профілактичне застосування антибіотиків задовго до операції чи більше ніж 48 годин у післяопераційному періоді призводе до порушення біоценозу шлунково-кишкового тракту і колонізації верхніх відділів мікрофлорою товстої кишки з можливим розвитком ендогенної інфекції завдяки бактеріальній транслокації умовних патогенів через лімфатичну систему тонкої кишки. Крім того, зростає небезпека виникнення суперінфекції в оперованих хворих за рахунок селекції антибіотико-резистентннх штамів. Тому антибіотик варто вводити хворому у відповідній дозі безпосередньо за ЗО хв перед операцією (внутрішньовенне під час наркозу) з наступними повторними ін’єкціями за показами, але не більше 24 годин.
10.4. КРИТЕРІЇ ВИБОРУ АНТИБІОТИКА ДЛЯ АП
Спектр активності антибіотиків повинний включати найбільш поширених збудників післяопераційних інфекцій (в першу чергу стафілококи), тому що вони викликають до 80% випадків від загального числа післяопераційних нагноєнь.
Доза антибіотика при АП відповідає звичайній терапевтичній дозі. Час введення антибіотика є найбільше важливим чинником при проведенні АП. Концентрація антибіотика в тканинах повинна бути співставимою з концентрацією в сироватці крові й досягатись через З0 хв після внутрішньовенного введення препарату. Для більшості планових та екстрених оперативних втручань оптимальним слід вважати введення антибіотика під час вступного наркозу – за 30-40 хв до операції.
Кратність введення визначається періодом напіввиведення. Повторна доза вводиться при тривалості операції, що перевищує в 2 рази період напіввиведення антибіотика. Призначення антибіотиків з метою профілактики ранової інфекції після завершення операції є неефективним і недоцільним.
Шлях введення. Найбільш оптимальним при АП є внутрішньовенний шлях введення, що забезпечує його оптимальну концентрацію в сироватці крові під час операції. При окремих операціях можливо застосовувати антибіотики внутрішньом’язово та усередину.
Препарати вибору. Для профілактики післяопераційних інфекційних ускладнень використовують переважно цефалоспорини 1-го покоління (цефазолин). що зумовлено адекватним спектром дії проти провідних збудників хірургічної ранової інфекції (зокрема стафілококів), наслідки якої можуть викликати інвалідизацію хворого, а її лікування по вартості багаторазово перевищує витрати на проведення АП.
Профілактику вважають за неефективну, якщо в ділянці первинного розрізу відбувається розвиток інфекції, а також у випадку невиправданого застосування антибіотиків протягом 4 тижнів після первинної операції. Інфекцію у віддалених ділянках (наприклад, пневмонію, інфекцію сечовивідних шляхів, інфікування внутришньосудинних систем і пристроїв) не розглядають як неефективність АП.
Таким чином, при проведенні АП ранової інфекції, слід враховувати:
- широке застосування антибіотиків із профілактичного метою неминуче веде до селекції резистентних штамів і підвищує ймовірність виникнення суперінфекції в оперованих хворих. Цей ризик можна звести до мінімуму, якщо антибіотик застосовується безпосередньо перед операцією, а не задовго до її, і використовується менш ніж 24 годин у післяопераційному періоді.
Така тактика виправдана і з економічних позицій; - для профілактики ранової інфекції й антибіотикотерапії бажано уникати
застосування однакових антибіотиків; - АП не виключає необхідність дотримання правил асептики під час оперативного втручання (в бригади, що оперує, не повинно виникати помилкового відчуття повної безпеки хворого від інфекції у зв’язку з введенням антибіотика).
11. АНТИБИОТИКОТЕРАШЯ РАНОВОЇ ІНФЕКЦІЇ Тактика раціональної антибактеріальної терапії передбачає: ”
- правильний вибір препаратів з урахуванням природної та набутої резистентності виявлених чи передбачуваних (до одержання результатів
- бактеріологічного дослідження) збудників;
- застосування оптимальних доз для досягнення терапевтичної концентрації у вогнищі інфекції;
- оптимальні способи і кратність введення препаратів;
- адекватну тривалість курсів лікування;
- обгрунтовану ритмічну зміну антибіотиків чи призначення їх у припустимих комбінаціях, що підсилюють терапевтичний ефект.
Аналіз етіологічної структури ранової інфекції при різних формах перебігу і локалізації процесу а також знання основних характеристик антибіотиків є основою для проведення емпіричної (у тому числі комбінованої) антимікробної терапії до виділення збудника. Наступна корекція лікування здійснюється з урахуванням характеру виділеної мікрофлори та її чутливості до антибіотиків. При можливості вибору перевагу віддають препаратам першого ряду, що при необхідності заміняють антибіотиками резерву чи препаратами другого ряду за обгрунтованими показами.
При відкритих ранах з ознаками нагноєння призначають комбіновану терапію до виділення збудника, виходячи з уявлень про провідну роль стафілококів та високу питому вагу мікробних асоціацій при пост-травматичних ранових інфекціях. Зазвичай використовують аміногликозиди (3-4.5 мг/кг/на добу) v сполученні з оксациліном (4-6 г/на добу), цефазолін (3 г/на добу).
З цефалоспоринов 3-го покоління використовують цефтриаксон (препарат пролонгованої дії, який застосовувається одноразово в добовій дозі). Застосування інших цефалоспоринів 3-го покоління є обмеженим, так як вони в 2-4 рази менш активні у відношенні стафілококів і в кілька разів дорожчі за препарати 1-го і 2-го поколінь.
При інфікуванні післяопераиійних ран використовують наступні варіанти емпіричної антибіотикотерапії в залежності від тяжкості ранової інфекції й особливостей формування резистентності бактерій до антибіотиків в умовах конкретного стаціонару:
• при інфекціях м’яких тканин без ознак сепсису препаратами вибору є
ципрофлоксацин без чи в сполученні з ампіциліном або лінкоміїшном (так само як і комбінація останнього з аміногликозидами);
при сепсисі до виділення збудника частіше використовують комбіновану терапію: ципрофлоксацин + метронідазол: або починають з монотерапії карба-пенемами (меропенем чи імепенем). Після отримання бактеріологічних резуль-татів, проводять етіотропну теріпію у відповідності до виявлених збудників.
Цефалоспорини 3-го покоління (зокрема, аефотоксим) доцільно застосовувати в терапії важких і змішаних інфекцій за участю грамнегативної флори. У цьому випадку цефотаксим може бути препаратом вибору оскільки він забезпечує мінімальну вартість лікування у порівнянні з комбінацією інгібіторозахисний амінопеніцилін/ клавуланат.
Для правильного трактування результатів бактеріологічного аналізу та проведення раціональної антибіотикотерапії необхідно пам’ятати, що:
- стафілококи, які продукують пеніциліназу (стійкі до бензилпеніциліну), резистентні до амінопеніцилінів (ампіцилін і амоксицилін), карбокси-пеніцилінів (карбеніцилін) та уреїдопеніцилінів;
- стафілококи, стійкі до метициліну й оксациліну, резистентні до всіх бета- лактамних антибіотиків й, як правило, стійкі до аміногликозидів та лінкозамінів;
- для грамнегативних бактерій резистентність до аміногликозідів частково перехресна: мікроби, які стійкі до гентаміцину (тобраміцину), чутливі до нетилміцину, амікацину, але не навпаки.
Таким чином, урахування спектру антимікробної дії антибіотиків і здійснення моніторингу антибіотикорезистентності збудників ранової інфекції є основою раціонального застосування антимікробних препаратів. Для прогнозування клінічного ефекту антибіотиків при проведенні етіотропної терапії необхідно враховувати його ймовірну концентрацію у вогнищі інфекції а також дані про результати застосування препарату для лікування конкретних інфекцій.
РЕЗЮМЕ
У відомчій інструкції обгрунтовано основні переваги сучасних комбінованих препаратів для місцевого лікування ран та клініко-економічну ефективність їх послідовного патогенетично обгрунтованого застосування. Доведено, що такий підхід дозволяє у 1,5-2 рази поліпшити еффективность, скоротити тривалість та загальну вартість місцевого лікування ран.
Сформульовані та обгрунтовані сучасні принципи, паказання до проведення, критерії вибору та раціональні схеми застосування антибіотиків при проведенні антибіотикопрофілактики та антибіотикотерапії ранових інфекцій.
В відомча інструкція є основою для впровадження раціональної системи лікувальних заходів на всіх етапах ранового процесу (хірургічна обробка, місцеве медикаментозне лікування, системна терапія), що дозволить удосконалити ефективність надання хірургічної допомоги та сприятеме раціональному використанню бюджетного фінансування лікувально-профілактичними закладами України.