Порушення серцевого ритму та провідності
ПЕРЕДМОВА
Проблема серцево-судинних захворювань – питання вели кої соціальної та медичної важливості. Смертність від захворювань серця і судин складає 64%. За цим показником Україна займає одне з перших місць в Європі. Це спонукає до активної праці з профілактики, діагностики та лікування кардіологічних захворювань.
У кардіології найбільш інтенсивно серед інших галузей охорони здоров’я використовуються результати доказової медицини. Аритмологія є однією з найбільш складних клінічних дисциплін: постійно уточнюються підходи до лікування різних порушень ритму та провідності серця, поновлюються та конкретизуються міжнародні та вітчизняні рекомендації. Активно розвиваються інвазивні методи лікування аритмій.
У даному навчальному посібнику коротко охарактеризовані основні види порушень серцевого ритму та провідності, їх критерії та методи надання хворим першої невідкладної та спеціалізованої медичної допомоги.
Широкий та двоступеневий рівень тестів сприяє більш живому засвоєнню матеріалу, що також закріплюється атласом анотованих електрокардіограм. Книга рекомендована студентам медичних вищих навчальних закладів, кардіологампочатківцям та лікарям загальної практики.
Автори будуть вдячні за критичні зауваження, пропозиції читачів і врахують їх у подальшій роботі.
В широкому значенні слова в поняття «аритмії серця» можна включати всі порушення, при яких змінюються ті функції серця, які забезпечують ритмічне і послідовне скорочення його відділів. Сюди входять різні порушення автоматизму, збудливості, провідності та їх сполучення.
За відсутності дії зовнішніх подразників у серці автоматично здійснюється фізіологічне управління, що забезпечує хронотропну координацію скорочень. Центром автоматизму І порядку є синоатріальний вузол, клітини якого мають максимальну швидкість діастолічної деполяризації й автоматичної активності завдяки різній проникливості клітинних мембран для К+, Nа+, Са2, Сl тощо. Центрами автоматизму ІІ та ІІІ порядку є відповідно передсердно-шлуночкове з’єднання (30– 40 за 1 хв.) і нижня частина пучка Гіса з волокнами Пуркіньє (15–20 за 1 хв.).
Хвиля збудження, генерована синоатріальним вузлом, поступово охоплює міокард передсердь і шлуночків, поширюючись через провідну систему серця, яку за функціональними та морфологічними особливостями поділяють на:
- синусно-передсердний, синоатріальний вузол (стара назва «синусовий вузол») або вузол Кіса-Флека;
- міжпередсердні та міжвузлові провідні шляхи (міжвузлові: передній – Бахмана, він же і міжпередсердний, середній – Венкенбаха і задній – Тореля);
- передсердно-шлуночковий, або атріовентрикулярний вузол (вузол Ашоффа-Тавара);
- пучок Гіса, його права і ліва ніжки (відповідно до кожного шлуночка), ліва з передньою та задньою гілками; 5) субендокардіальні волокна Пуркіньє.
Крім зазначених, існують додаткові провідні шляхи: Паладіно-Кента, Джеймса, Махайма та ін. Імпульс із передсердь поширюється ними в обхід атріовентрикулярного з’єднання (Паладіно-Кета, Джеймса) без фізіологічної затримки в атріовентрикулярному вузлі (у нормі вона дорівнює 0,12–0,18 с), що часто спричинює аритмії. Додаткові провідні шляхи, особливо Паладіно-Кента, можуть бути причиною атріовентрикулярної реципрокної тахікардії (АВРТ) – ортодромної (імпульс для шлуночків «проходить» звичайним шляхом, а ретроградно – через додатковий шлях проведення) або антидромної (до шлуночків імпульс із синусового вузла «добирається» додатковим шляхом проведення, а ретроградно – класичним шляхом).
Синусовий вузол – це маленька (2–6 мм) еліпсоїдна структура, розміщена субепікардіально в місці впадіння верхньої порожнистої вени в праве передсердя. Кровопостачання вузла здійснюється правою коронарною артерією, іннервація – переважно гілками блукаючого нерва.
Атріовентрикулярний вузол розміщується в нижній частині правого передсердя, разом із стовбуром пучка Гіса утворює атрівентрикулярне з’єднання, яке складається із трьох гістологічно різних частин: передсердно-вузлової (перехідної), вузлової (саме вузла) та вузлово-пучкової.
Атріовентрикулярне з’єднання виконує такі функції:
- проведення біоелектричних імпульсів від передсердь до шлуночків;
- затримку імпульсу на час, необхідний для скорочення передсердь і вигнання крові у шлуночки, що на ЕКГ визначається інтервалом Р-Q (0,12–0,8 с);
- захист шлуночків від надмірної кількості імпульсів, що утворюються в передсердях у разі передсердних тахіаритмій шляхом функціональної атріовентрикулярної блокади;
- у разі порушення функції синусового вузла атріовентрикулярне з’єднання стає водієм ритму.
Функціонально атріовентрикулярне з’єднання складається із α- і β-волокон (зон), у яких різна швидкість проведення імпульсів. Ці волокна утворюють два пучки, що відрізняються швидкістю проведення. Рефрактерний період α-пучка коротший, а швидкість проведення менша, ніж у β-пучка. Рефрактерний період β-пучка довший, ніж α-пучка, а швидкість проведення імпульсів ним більша, ніж α-пучком. Така функціональна неоднорідність атріовентрикулярного з’єднання створює можливості для виникнення поздовжньої дисоціації і може бути патофізіологічною основою виникнення атріовентрикулярної вузлової реципрокної тахікардії – АВВРТ (імпульс, пройшовши від передсердь до шлуночків через зону α, може повернутися ретроградно через зону β і навпаки – slow-fast і fast-slow тахікардії).
Пучок Гіса (довжина 10 мм) і його ніжки (права та ліва) є центром автоматизму ІІІ порядку, вони забезпечують проведення імпульсу з дуже високою швидкістю (3–4 м/с), що зумовлює майже одночасне збудження всіх клітин міокарда шлуночків.
Безпосередній зв’язок провідної системи з волокнами робочого міокарда здійснюється численними розгалуженнями волокон Пуркіньє, які розміщується субендокардіально. Поширення збудження відбувається завдяки контактним мембранам (нексусам), які містять щілини (канали), через які вільно проходять йони. Швидкість поширення імпульсів по міокарду в 5 разів менша, ніж по провідній системі серця.
В основі виникнення електричних потенціалів у міокарді лежить процес різноспрямованого руху йонів через протоплазматичну мембрану кардіоміоцитів. У середині клітини у не збудженому стані в період діастоли концентрація К+ у 30 разів вища, ніж поза клітиною, а Na+ – у 20 разів вища (Са 2+ – у 25 разів) поза клітиною, ніж у клітині. Різниця у концентраціях підтримується завдяки активній функції йонних каналів, через які в клітину поступають Na+, Са 2+, Сl–, після чого К+ виходить із неї. Такі процеси здійснюються за допомогою енергії розпаду АТФ за участі Na+– і К+ -АТФ-аз.
У стані спокою трансмембранна різниця потенціалу спокою становить – 90 mV. Здатність клітини спонтанно деполяризуватися називається спонтанною діастолічною де поля ризацією. Кардіоміоцити синусового вузла, спонтан но де поляризуючись, циклічно генерують біоелектричні імпуль си, які поширюються провідною системою серця. Під час збудження клітини проникність її мембрани для окремих йонів змінюється, при цьому реєструється крива трансмембранного потенціалу дії. Розрізняють кілька фаз трансмембранного потенціалу дії:
Фаза 0. Це фаза деполяризації клітини. Початок збудження характеризується активацією швидких натрієвих каналів сарколеми, Na+ надходить у середину клітини. Відбувається швидка деполяризація мембрани (10 мс). Електричний заряд її змінюється з -90 до +20 мВ. Період від 0 до +20 мВ має назву овершут – період дуже швидкої деполяризації.
Фаза 1. Це фаза ранньої швидкої реполяризації (відновлення передсердної полярності мембрани), пов’язана із швидким надходженням йонів Сl– усередину клітини. Заряд мембрани падає до 0 мВ і нижче.
Фаза 2. Характеризується відносно повільним процесом реполяризації. На кривій трансмембранного потенціалу дії реєструється плато. Постійний рівень потенціалу дії підтримується постійним повільним входженням Са2+ і частково Na+ в клітину. Фаза триває 200 мс, при цьому відбувається скорочення шлуночків і вигнання крові в судини.
Трансмембранний потенціал
Фази потенціалу дії кардіоміоцитів – пейсмекерів (водіїв ритму серця): а – загальна схема; б – із врахуванням спонтанної діастолічної деполяризації; 0 – фаза деполяризації; 1 – фаза ранньої швидкої реполяризації; 2 – плато – фаза ранньої повільної реполяризації; 3 – фаза кінцевої швидкої реполяризації; 4 – фаза спонтанної діастолічної деполяризації
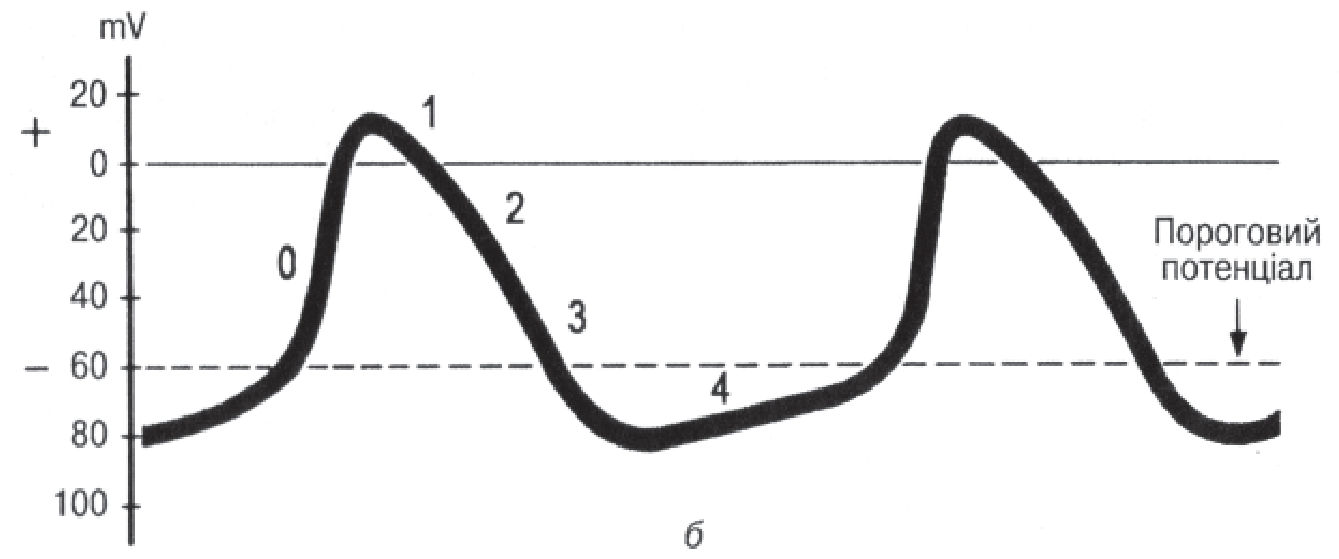
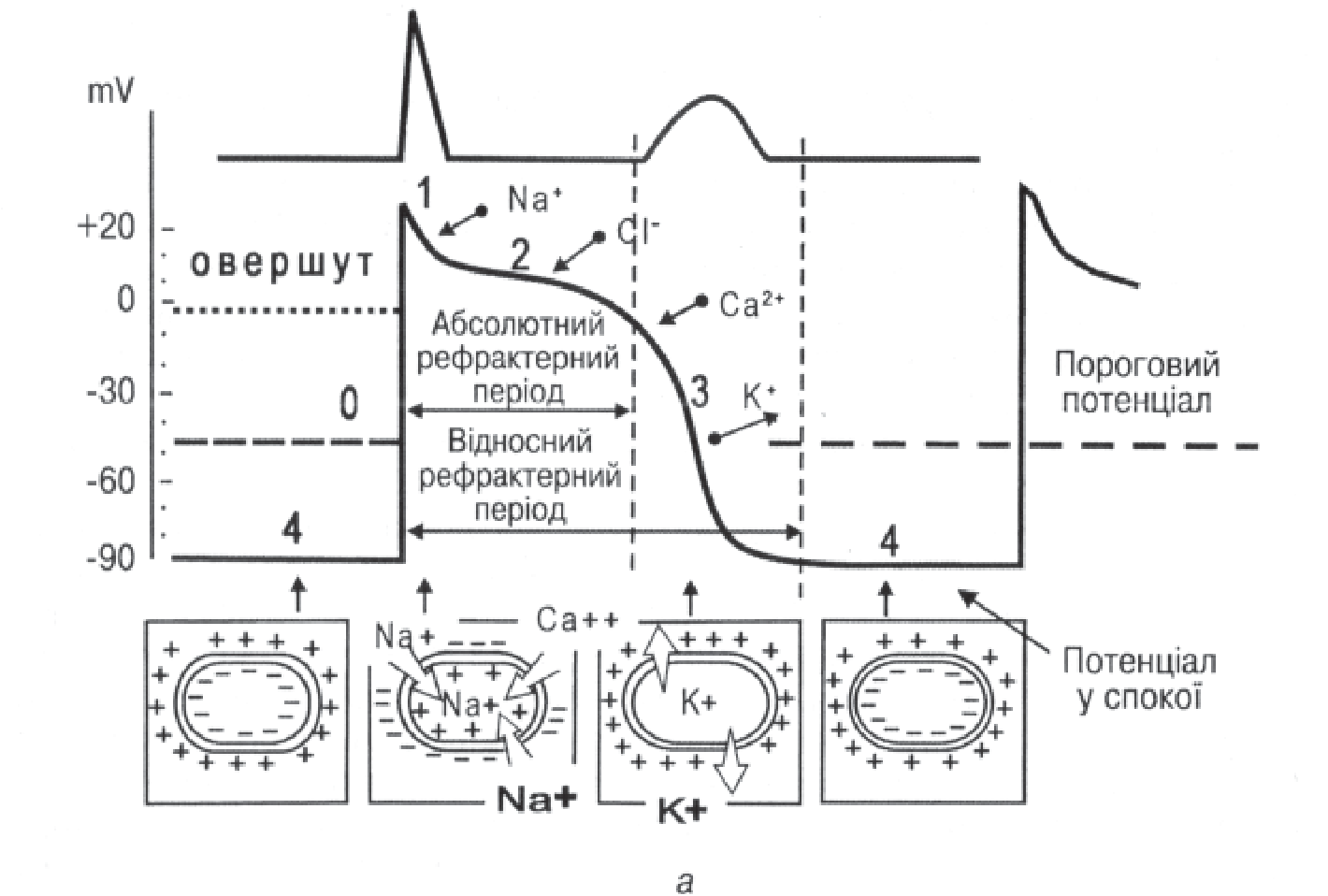
Фаза 3. Це прикінцева швидка реполяризація міоцитів. Відбувається переміщення К+ в позаклітинну рідину, що повністю відновлює попередню полярність мембрани.
Фаза 4. Це період діастоли. Рівень потенціалу дії наближується до -80 … -90 мВ. У клітинах водія ритму протягом цієї фази потенціал спокою зменшується, що зумовлено виходом з клітини К+. Це і є фаза спонтанної діастолічної деполяризації. Крива знижується до початкового рівня, після досягнення якого знову різко зростає проникність мембрани для Na+, і серцевий цикл повторюється.
Ця динаміка різниці потенціалів представлена у схемі (рис. №1).
Найпоширенішим і достатньо інформативним дослідженням ритму серця є традиційна ЕКГ в стані спокою. Деякі аритмії і блокади можна діагностувати під час проби з ДФН. Дуже важливими є дані холтерівського моніторування, коли протягом доби визначається ЧСС і за допомогою якого можна кількісно і якісно охарактеризувати екстрасистолію, тахікардії в стані спокою і під час фізичного навантаження, під впливом лікування.
КЛАСИФІКАЦІЯ ПОРУШЕНЬ СЕРЦЕВОГО РИТМУ І ПРОВІДНОСТІ (VІ НАЦІОНАЛЬНИЙ КОНГРЕС КАРДІОЛОГІВ УКРАЇНИ, 2000 рік)
І. Порушення утворення імпульсу.
- Синусова тахікардія (більше ніж 90 комплексів за 1 хв.).
- Синусова брадикардія (менше ніж 60 комплексів за 1 хв.).
- Синусова аритмія.
- Зупинка (відмова) синусового вузла.
- Міграція надшлуночкового водія ритму.
- Екстрасистолія (синонім – передчасна деполяризація):
- передсердна (артеріальна);
- передсердно-шлуночкова (атріо-вентрикулярна);
- шлуночкова:
- поодинока (до 30 за 1 год.);
- часта (30 і більше за 1 год.);
- алоритмія (бі-, три-, квадригемінія);
- поліморфна;
- парна;
- рання (R на Т).
7. Тахікардії:
надшлуночкові:
- синопередсердна (синоатріальна);
- передсердна (атріальна);
- передсердно-шлуночкова (атріовентрикулярна);
з додатковими шляхами проведення: ортодромна; антидромна;
шлуночкові:
- нестійка (від 3 шлуночкових комплексів до 30 с);
- стійка (більше ніж 30с);
- постійно-зворотна;
мономорфна;
поліморфна.
8. Фібриляція і тріпотіння передсердь:
- пароксизмальна (ритм відновлюється самостійно в межах 48 год.);
- персистуюча (для відновлення синусового ритму необхідне втручання);
- постійна (коли синусовий ритм відновити неможливо або недоцільно);
- брадисистолічна (частота шлуночкових скорочень менше ніж 60 за 1хв);
- тахісистолічна (частота шлуночкових скорочень більше ніж 90 за 1 хв.).
9. Фібриляція і тріпотіння шлуночків.
ІІ. Порушення проведення імпульсу.
- Синоаурикулярні блокади.
- Атріовентрикулярна блокади (І–ІІІ ступенів).
- Внутрішньошлуночкові блокади (постійні, минаючі):
однопучкові:
- блокада правої ніжки пучка Гіса;
- блокада передньоверхнього розгалуження лівої ніжки пучка Гіса;
- блокада задньонижнього розгалуження лівої ніжки пучка Гіса;
двопучкові:
- блокада лівої ніжки пучка Гіса;
- блокада правої ніжки пучка Гіса та передньоверхнього розгалуження лівої ніжки пучка Гіса (блокада Бейлі);
- блокада правої ніжки пучка Гіса та задньонижнього розгалуження лівої ніжки пучка Гіса (блокада Вільсона).
ІІІ. Комбіновані порушення утворення і проведення імпульсу.
Парасистолія:
- передсердна;
- атріовентрикулярного з’єднання;
- шлуночкова.
ІV. Захворювання, синдроми і феномени.
Синдроми та ЕКГ-феномени передчасного збудження шлуночків:
- синдром Вольфа-Паркінсона-Вайта;
- синдром скорочення інтервалу Р-R (Лауна-ГанонгаЛівайна або Кларк-Леві-Крітеско);
- синдром ранньої реполяризації шлуночків;
- синдром подовженого інтервалу Q-Т:
- природжений (Романо-Уорда);
- набутий.
- синдром слабкості синусового вузла;
- синдром Морганьї-Адамса-Стокса;
- синдром Фредеріка.
Раптова серцева смерть (аритмічна) – смерть, що настала протягом 1 год. після появи перших симптомів захворювання або суттєвого погіршення стану хворого на тлі стабільного хронічного перебігу захворювання:
- з відновленням серцевої діяльності;
- незворотна.
Зупинка серця (смерть, що настала більше ніж через 1 год. після появи чи посилення симптомів захворювання):
- з відновленням серцевої діяльності;
- незворотна.
Механізми смерті:
- фібриляція шлуночків;
- асистолія;
- електромеханічна дисоціація (вказується за можливості).
V. Аритмії при нормальній або порушеній функції кардіостимуляторів різного типу.
Етіологія аритмій
- Захворювання серцево-судинної системи: ІХС (хронічні форми), інфаркт міокарда, нестабільна стенокардія, міокардити, кардіоміопатії, вади серця, пролапс мітрального клапана.
- Нервово-рефлекторні дії (при холециститі, виразковій хворобі шлунка та 12-палої кишки, діафрагмальній килі, деформуючому остеохондрозі), порушення гуморальної регуляції, електролітного балансу (гіпокаліємія, гіперкаліємія, гіпомагніємія, гіперкальціємія), кислотно-лужної рівноваги, ендокринні порушення.
- Фізичні, хімічні впливи: куріння, алкоголь, травма, гіпоксія, гіпо- та гіпертермія, медикаментозні засоби (серцеві глікозиди, антиаритмічні засоби, діуретики, симпатоміметики тощо).
- Ідіопатичні аритмії.
Патогенетичні механізми деяких аритмій
В основі всіх аритмій лежить порушення утворення або проведення імпульсу, або одночасне порушення функцій провідної системи.
Такі аритмії, як синусова тахі- і брадикардія пов’язані відповідно з посиленням та пригніченням автоматизму клітин синусового вузла. В походженні екстрасистолії та па роксизмальних порушень ритму виділяють такі механізми: посилення автоматизму ектопічних вогнищ, повторний вхід збудження (re-entry) та круговий рух імпульсу, тригерна (наведена) активність спеціалізованих та скоротливих клітин.
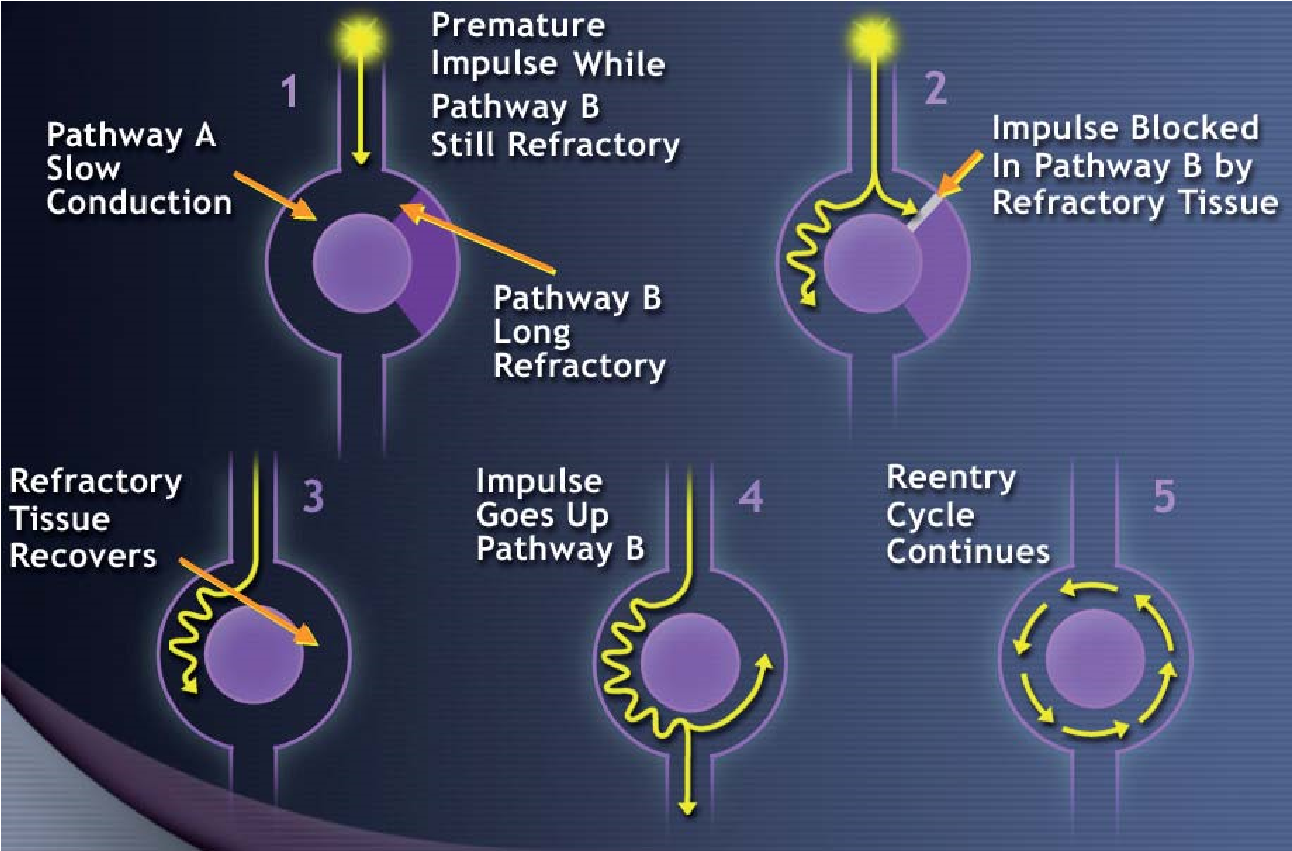
Механізм повторного входу збудження (re-entry) полягає у повторному або багатократному збудженні ділянки міокарда одним і тим же імпульсом, що здійснює круговий рух. Для реалізації цього механізму необхідні два шляхи проведення, причому по одному із них проходження імпульсу порушене внаслідок місцевої однонаправленої блокади. Ділянка міокарда, до якої черговий імпульс своєчасно не дійшов, збуджується обхідним шляхом із певним запізненням і стає джерелом позачергового збудження. Воно розповсюджується на сусідні ділянки міокарда.
Клініка
Порушення ритму серця можуть бути повністю безсимптомними або приводити до появи різних клінічних симптомів. До основних клінічних симптомів, безпосередньо пов’язаних із порушенням ритму серця, відносяться відчуття серцебиття або перебоїв у роботі серця.
Відчуття перебоїв у роботі серця зазвичай пов’язані з екстрасистолією – передчасним скороченням серця. Перебої в роботі серця хворі описують як несподівані поштовхи в грудній клітці, відчуття короткочасної зупинки чи завмирання серця (нерідко в сполученні з легким головокружінням чи потемнінням в очах). Дехто з хворих відчуває «перевернення серця», раптову необхідність глибоко вдихнути.
Причиною серцебиття в більшості випадків є синусова тахікардія при фізичному навантаженні або хвилюванні, страху, напливі тривожних думок.
Відчуття повністю нерегулярного (неритмічного) серцебиття характерне для нападів пароксизмального миготіння передсердь.
Аритмія може супроводжуватися виникненням стенокардії, задухи, набряку легень, різкої слабкості, головокружіння, перед непритомного стану, епізодів втрати свідомості й навіть кардіогенного шоку.
Як правило, причиною втрати свідомості є тахіаритмії або брадиаритмії.
Основною причиною раптової смерті також є аритмії (частіше за все шлуночкова тахікардія, що переходить у фібриляцію шлуночків).
Екстрасистолія
Екстрасистола – це передчасне збудження серця або його відділів під впливом патологічних імпульсів.
Екстрасистола проявляється передчасним скороченням із подальшою паузою. Вона називається постекстрасистолічним інтервалом або компенсаторною паузою. Якщо сума екстрасистолічного і постекстрасистолічного інтервалів дорівнює сумі двох серцевих циклів, то компенсаторна пауза вважається повною. Якщо сума інтервалів коротша, то пауза вважається неповною.
В деяких випадках компенсаторна пауза після екстрасистоли відсутня, тоді екстрасистоли називають інтерпольованими.
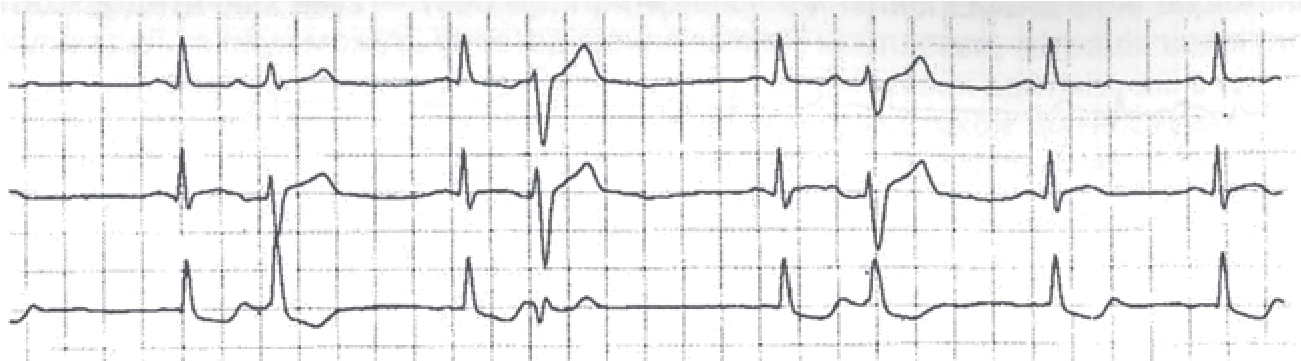

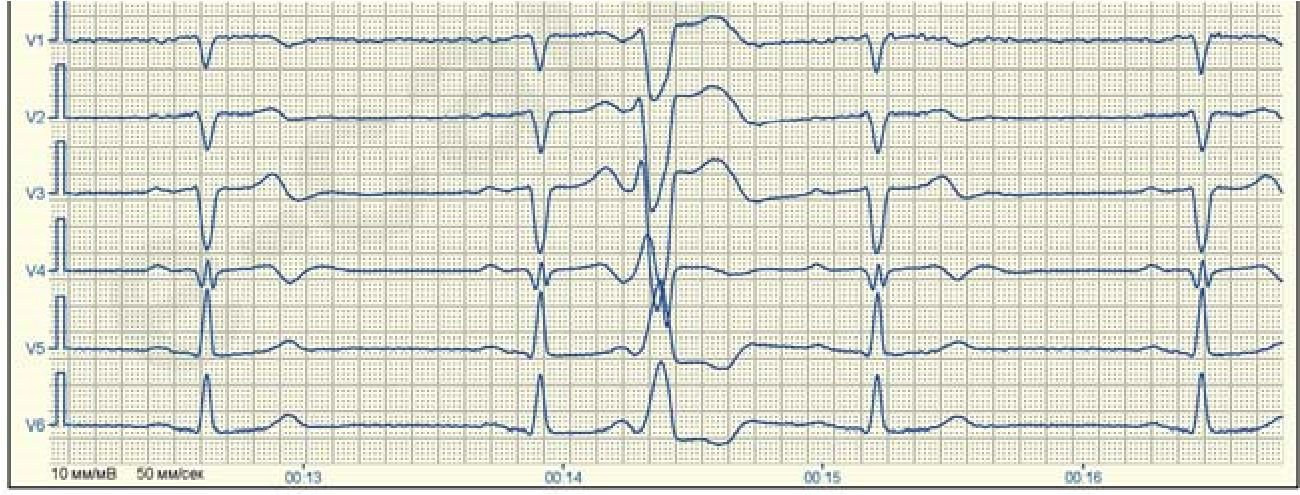
Екстрасистоли можуть бути поодинокими та груповими. Екстрасистолія, що чергується з комплексами у правильній послідовності, називається алоритмічною. Екстрасистоли, які йдуть за кожним черговим комплексом, визначаються як бігемінія, за кожним другим – тригемінія, за кожним третім – квадригемінія і т.д.
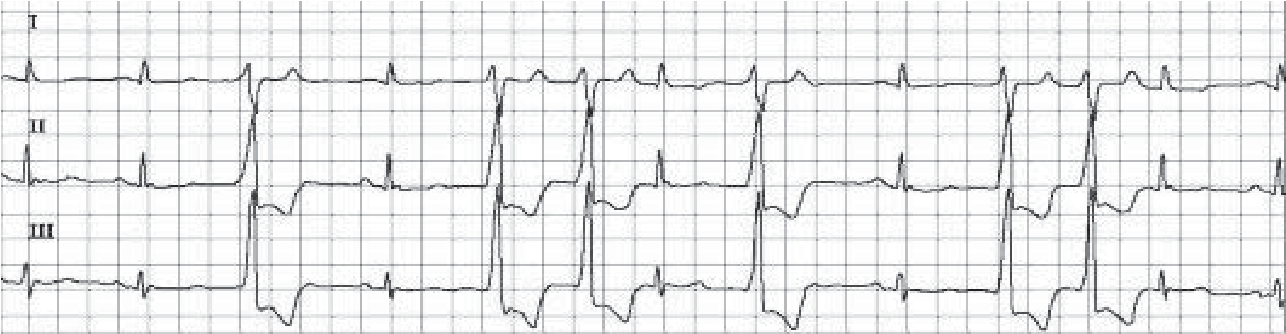
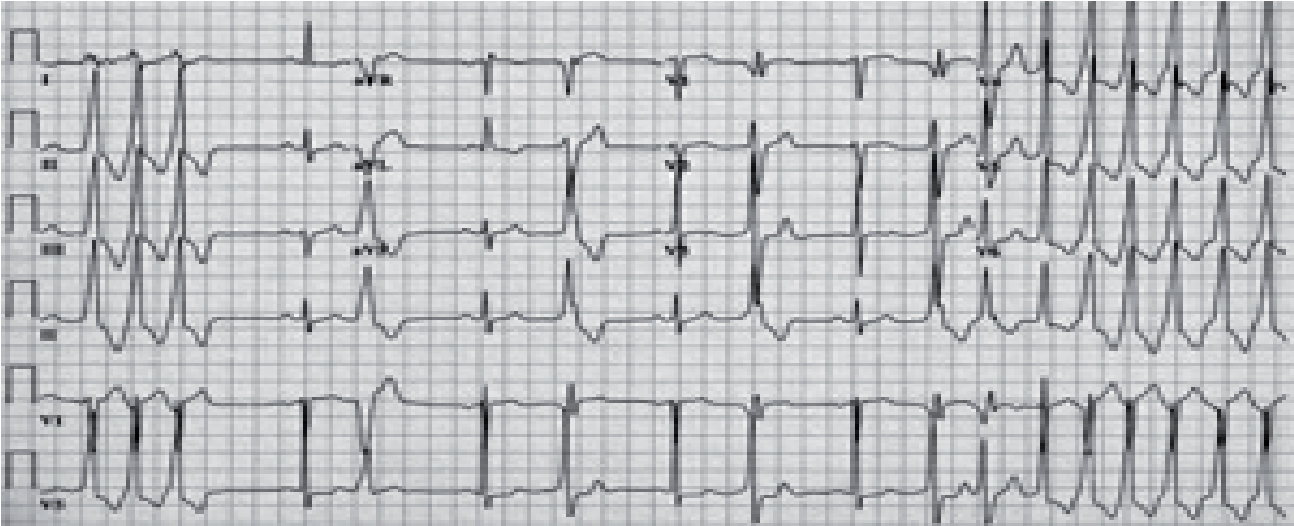
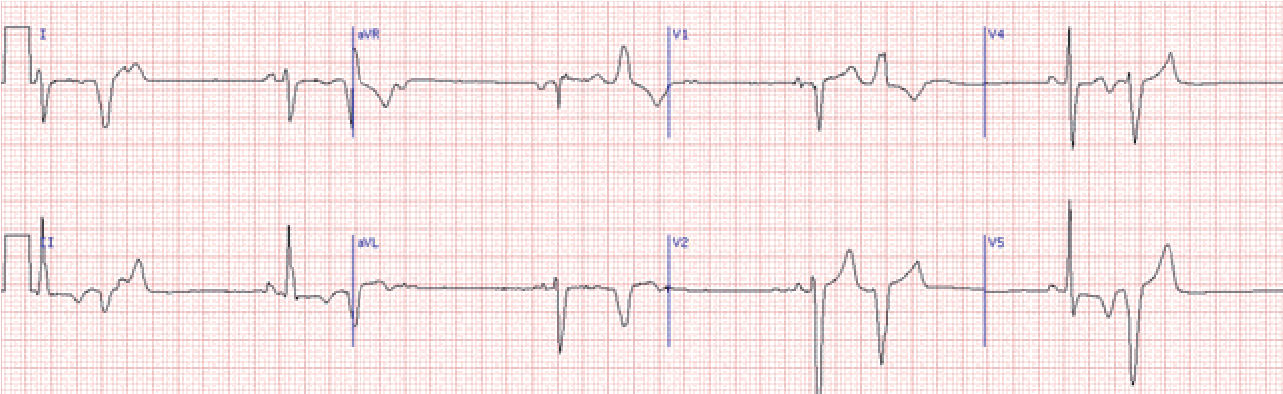
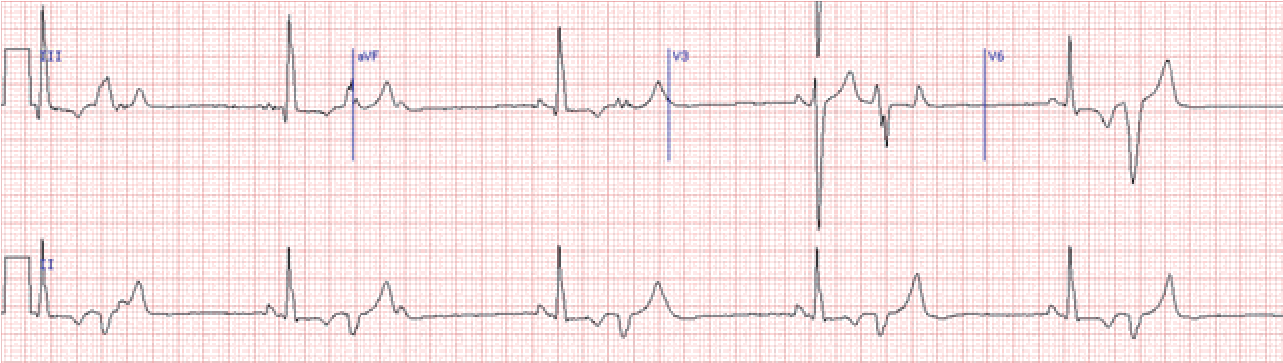
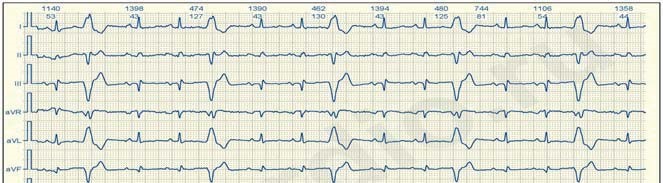
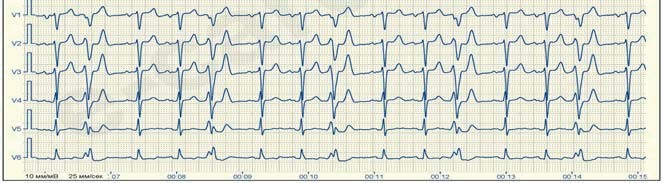
Велике практичне значення має розподіл екстрасистол за часом їх виникнення. При ранніх екстрасистолах екстра систо ліч ний комплекс нашаровується на зубець Т попереднього ком плексу, при середніх він стоїть від зубця Т, виникає в першій по ловині діастоли, при пізніх – виникає в другій половині діастоли.
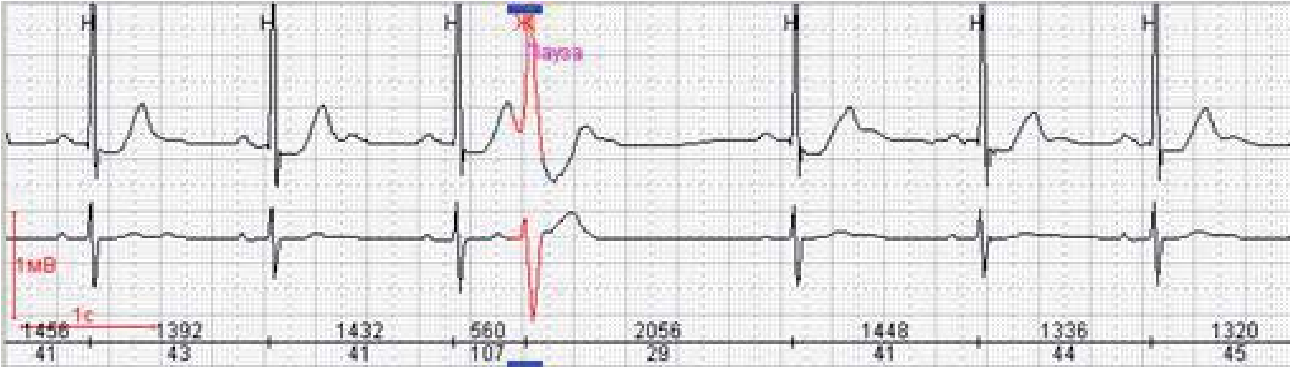
Рання екстрасистола
Ранні екстрасистоли, як правило, неефективні в гемодинамічному відношенні, ще більш важливо те, що вони можуть викликати загрозливі порушення ритму – миготіння та тріпотіння передсердь, фібриляцію шлуночків.
Екстрасистоли можуть бути моно- або політопними. При монотопних екстрасистолах екстрасистолічний інтервал однаковий, а при політопних – різний. Політопні екстрасистоли прогностично більш неблагоприємні, оскільки зазвичай свідчать про більш значне дифузне ураження міокарда.
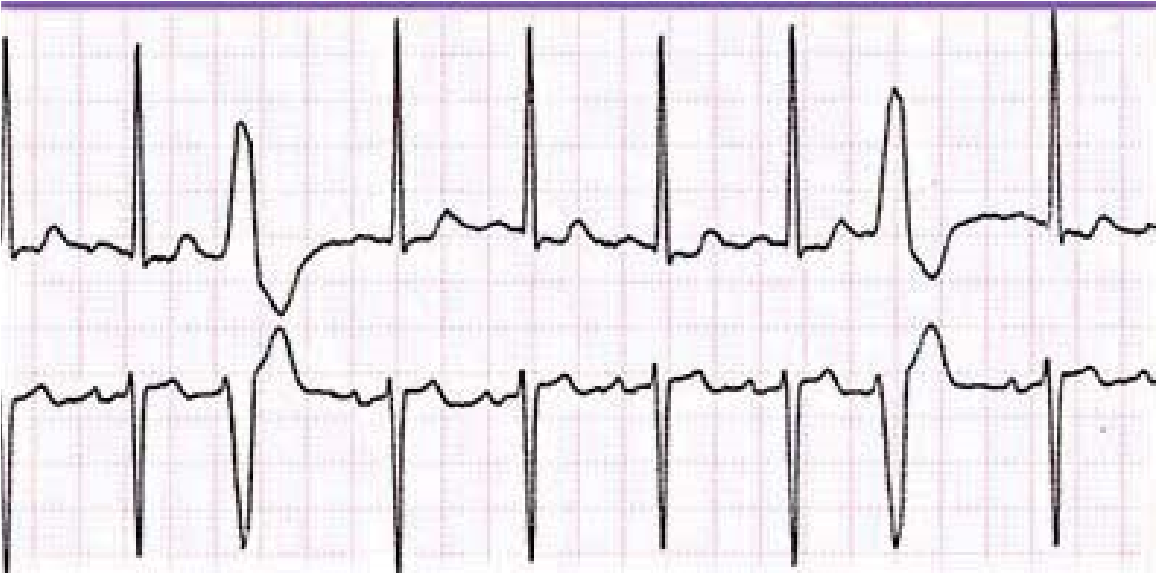
Монотопні екстрасистоли
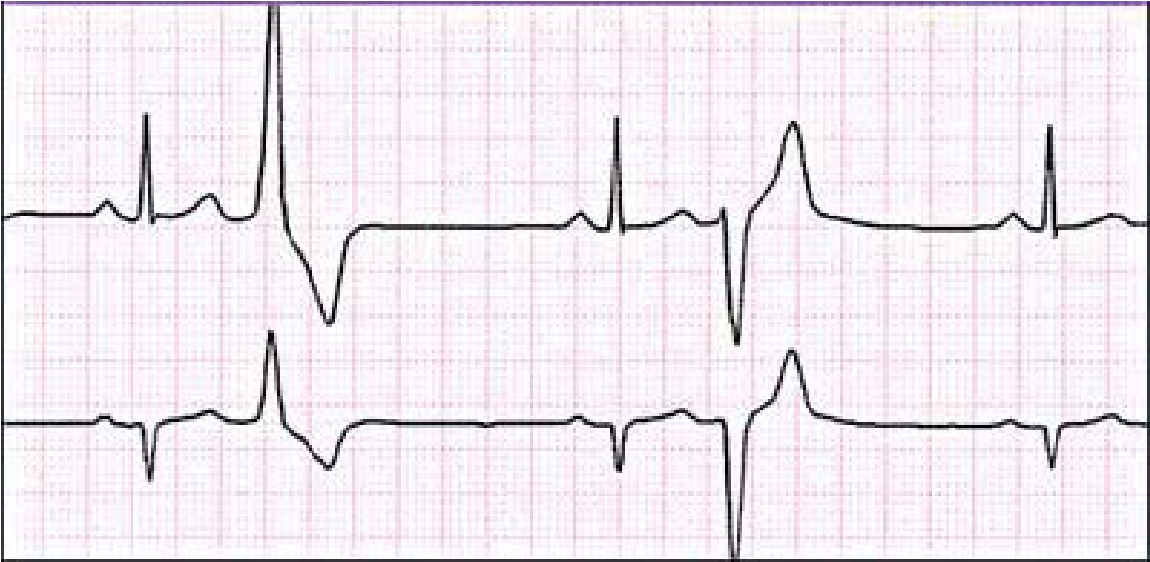
Політопні екстрасистоли
За локалізацією вогнища, з якого виникають передчасні імпульси, розрізняють екстрасистоли передсерді, вузлові, шлуночкові.
Передсердна екстрасистолія
Основна ознака – передчасний зубець Р, що за формою відрізняється від синусового. Форма шлуночкового комплексу не змінена. Компенсаторна пауза, як правило, неповна.
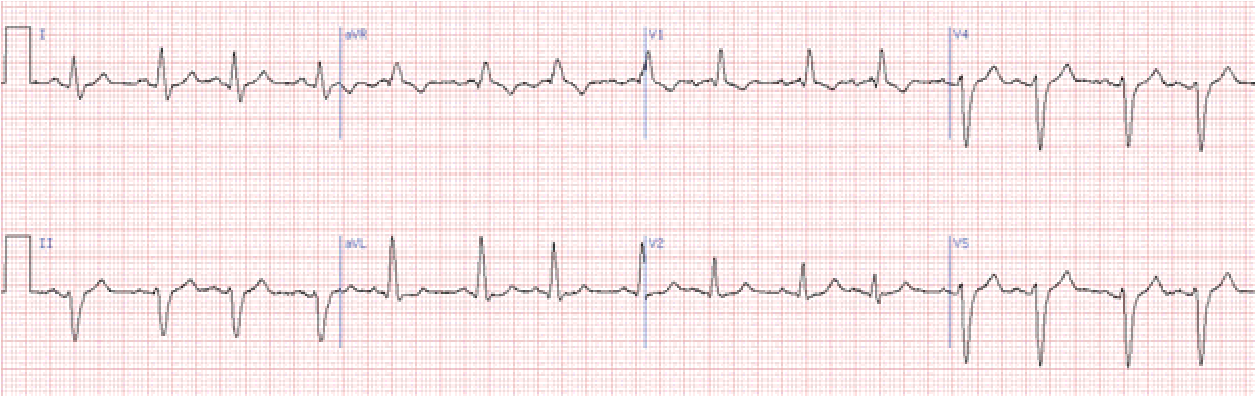
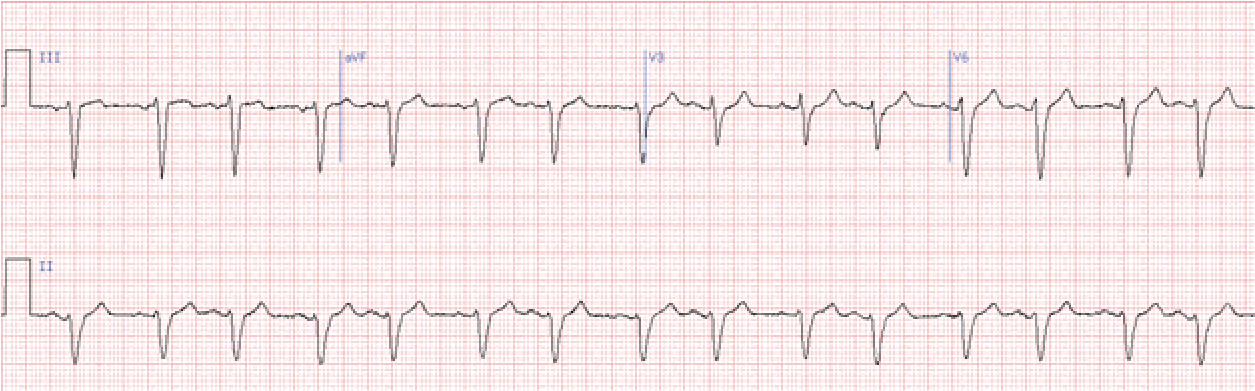
Передсердна екстрасистолія
Іноді шлуночкові комплекси змінені внаслідок функціональних порушень внутрішлуночкової провідності (частіше за типом блокади правої ніжки пучка Гіса).
Іноді трапляються блоковані передсердні екстрасистоли (зубець Р є, QRST відсутній).
Передсердні екстрасистоли у хворих можуть вказувати на зміни міокарда передсердь. Часті, групові, політопні передсердні екстрасистоли можна вважати передвісниками передсердної тахікардії, тріпотіння та фібриляції передсердь.
А-B екстрасистолія
А-В екстрасистоли поділяються на: верхньовузлову, середньовузлову та нижньовузлову. Якщо такі екстрасистоли виходять із а-в з’єднання, то в даному випадку передує збудження передсердь. Але вони можуть виходити і з нижніх відділів передсердь. Їх називають суправентрикулярними.
Якщо в екстрасистолічних комплексах зубці Р не виявляються (нашаровуються на QRS), то мова йде про а-в екстрасистоли з одночасним збудженням передсердь і шлуночків. Якщо зубці Р виявляються після зубців R екстрасистоли і вони (-) у відведеннях ІІ, ІІІ, аVF, то говорять про а-в екстрасистоли з наступним збудженням передсердь.
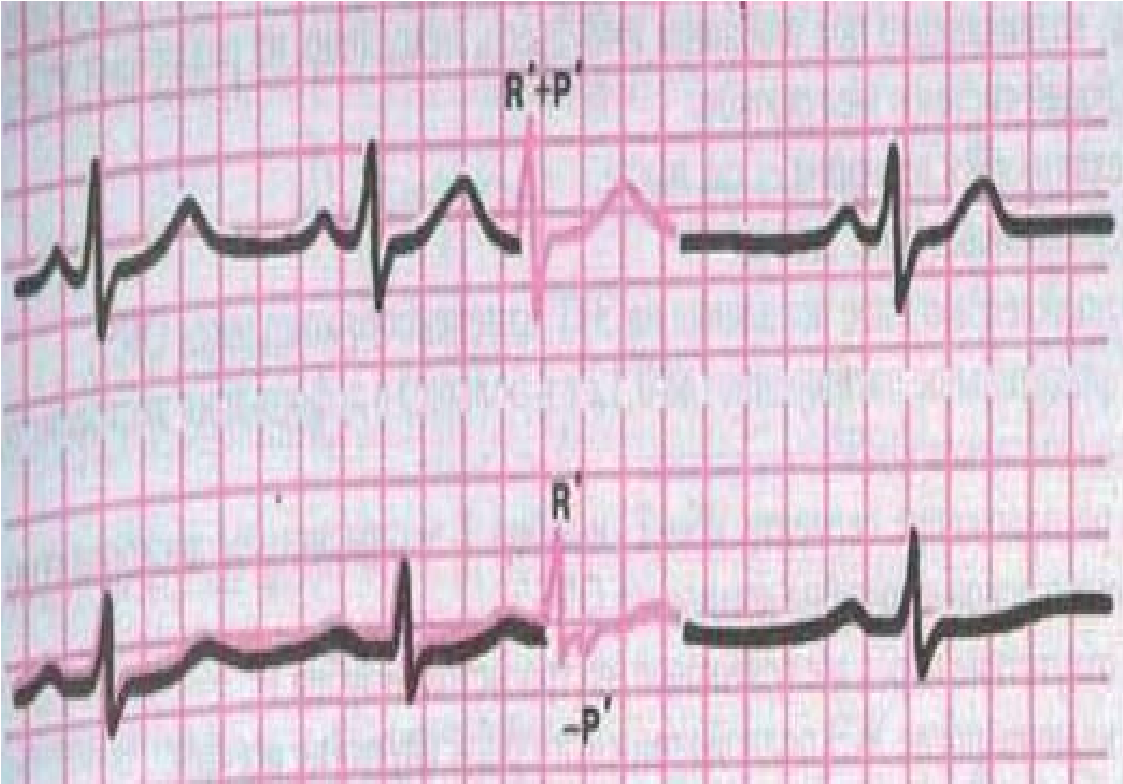
Компенсаторна пауза після а-в екстрасистол буває як повною, так і неповною.
Це найбільш рідкісний різновид екстрасистолії.
Шлуночкова екстрасистолія
Шлуночковою називають екстрасистолію, при якій вогнище локалізується в розгалуженнях пучка Гіса.
Відсутній зубець Р. Комплекс QRS деформований, >0,12 с. ST і Т розташовані дискордантно щодо головного зубця комплексу QRS. Компенсаторна пауза, як правило, повна.
Локалізацію ектопічного вогнища визначають за формою шлуночкового комплексу в різних відведеннях ЕКГ, причому головну роль грають грудні відведення.
У правошлуночкових екстрасистолах форма шлуночкового комплексу нагадує картину блокади лівої ніжки пучка Гіса.
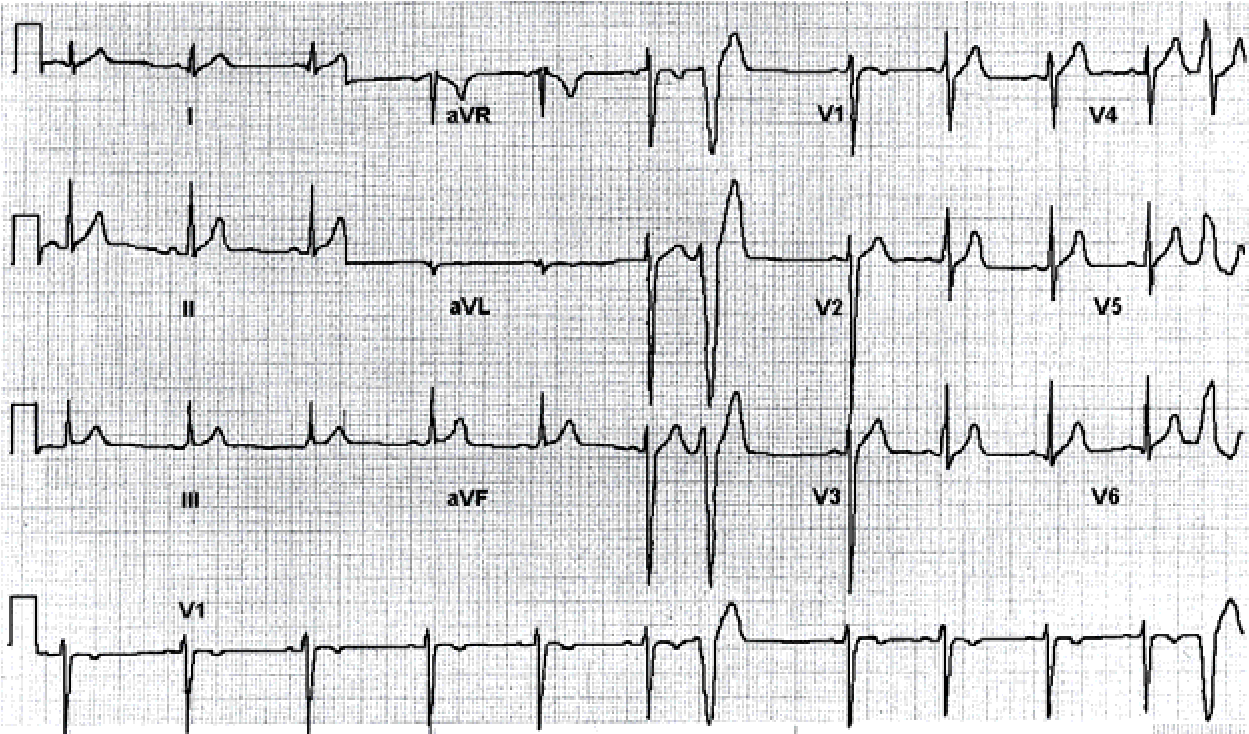
Лівошлуночкові екстрасистоли мають форму шлуночкового комплексу, як при блокаді правої ніжки.
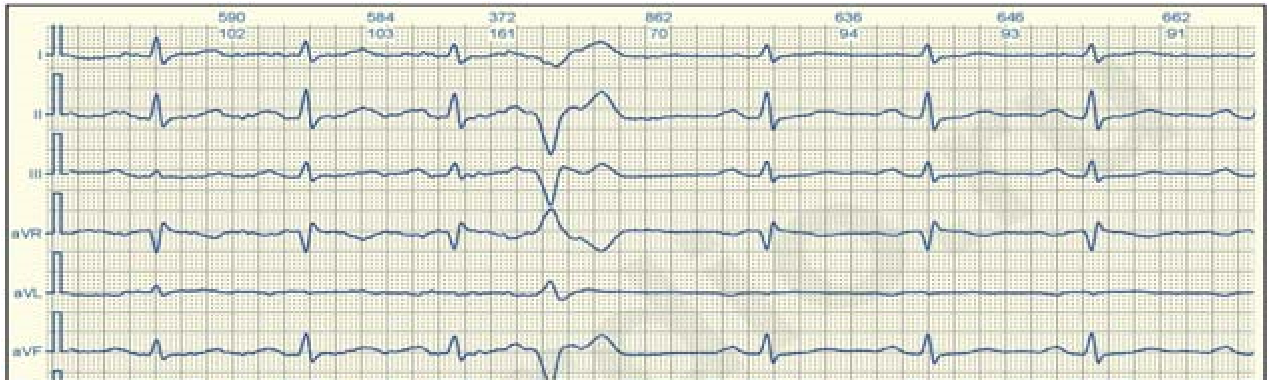
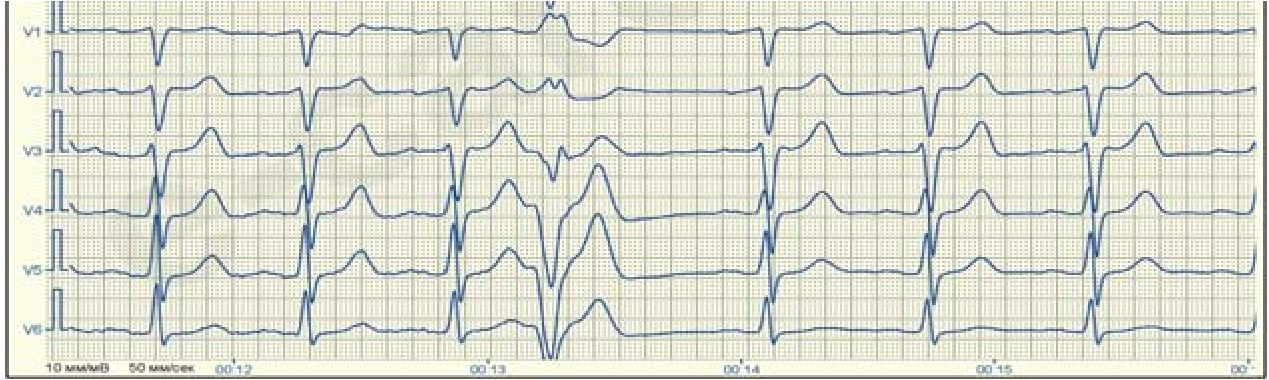
При базальних екстрасистолах комплекси QRS розширені, направлені вгору в усіх грудних відведеннях.
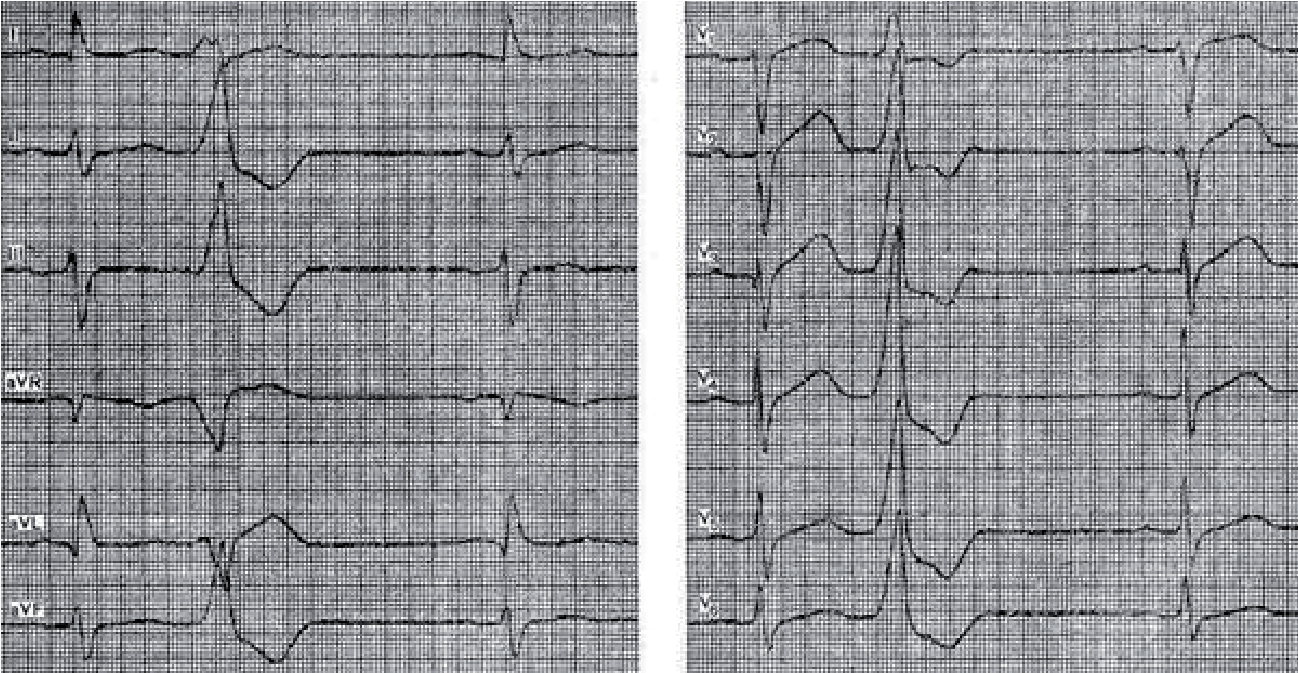
Апікальні (верхівкові) екстрасистоли характеризуються зубцями S, що переважають в усіх грудних відведеннях.
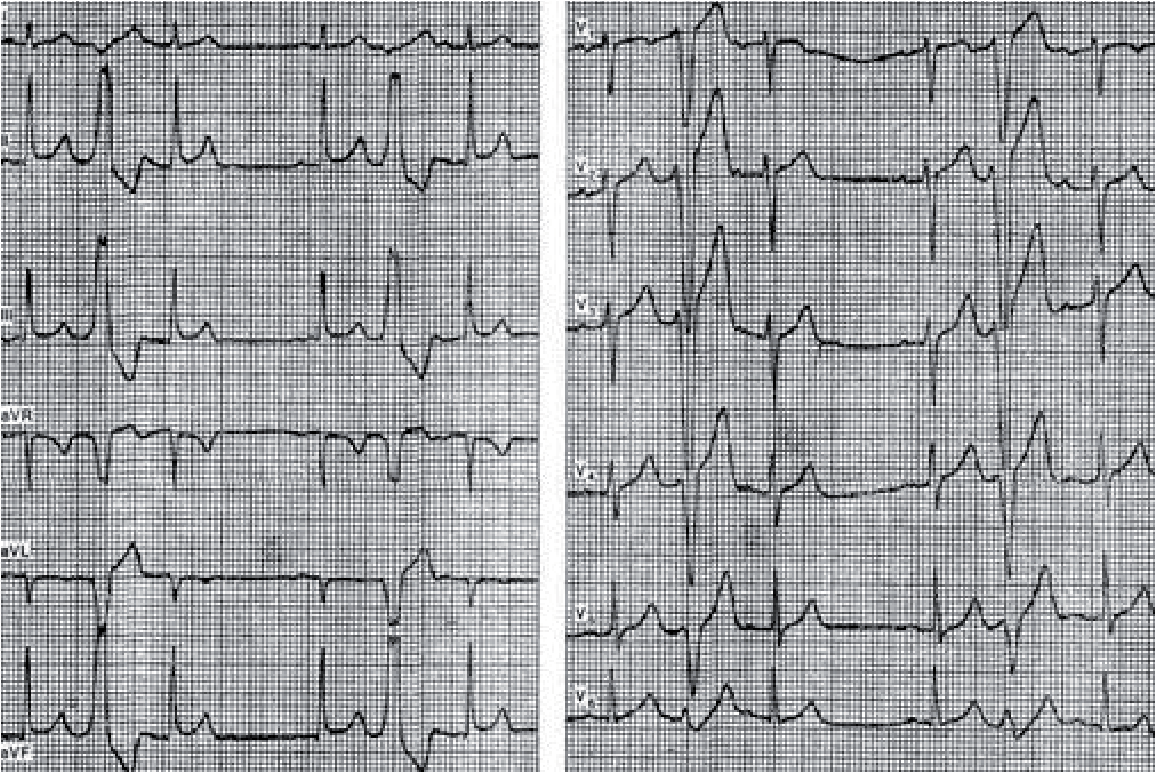
В. Lown (1977) класифікував шлуночкову екстрасистолію залежно від частоти виникнення, вогнищ аритмогенезу і прогнозу щодо виникнення тахікардії:
І клас – рідкі монотопні, до 5 за 1 хв. або 30 за 1 год.
ІІ клас – часті монотопні, >5 за 1 хв. або >30 за 1 год.
ІІІ клас – політопні екстрасистоли
ІVа клас – парні екстрасистоли (два скорочення поспіль – дуплети)
ІVв клас – три (і більше) екстрасистоли поспіль (короткі пароксизми)
V клас – «ранні» екстрасистоли (R на Т)
Пароксизмальна тахікардія
Це напади раптового різкого збільшення частоти серцевого ритму.
Ознаки: 1) висока частота ритму (зазвичай 160–250 в хв.),
2) правильний ритм, 3) гетеротопність. Ці ознаки неабсолютні. Так, іноді ЧСС може бути 130–150 на хв. У деяких випадках спостерігається дещо неправильний ритм.
Важливо, що напади пароксизмальної тахікардії (на відміну від синусової) раптово починаються та раптово закінчуються.
Напади можуть бути дуже тривалими (декілька днів, тижнів, місяців), дуже короткими (з 5 та більше комплексами).
Також як екстрасистолію, пароксизмальну тахікардію поділяють на суправентрикулярну та шлуночкову.
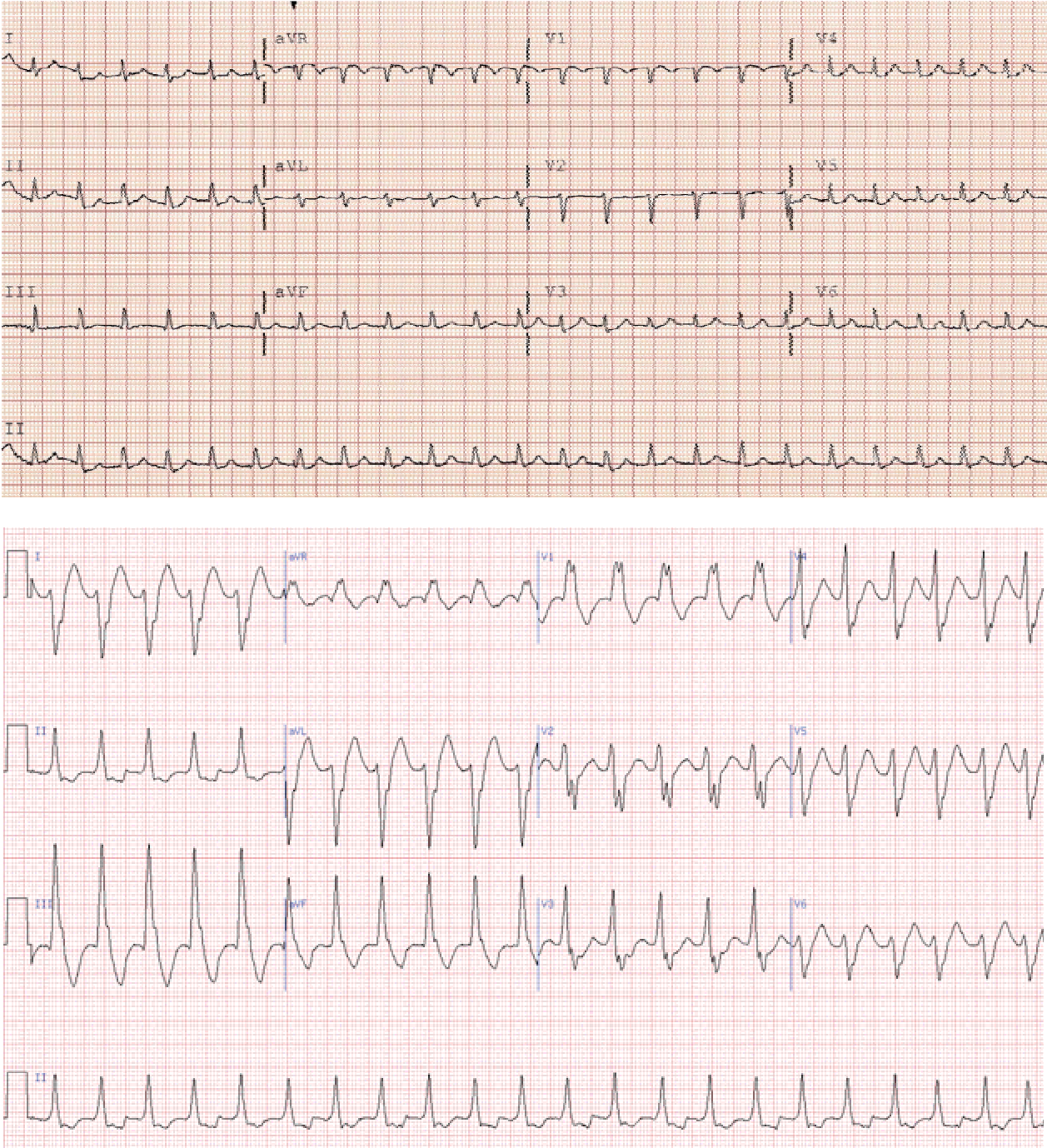
При суправентрикулярній тахікардії в більшості випадків немає деформації шлуночкових комплексів.
Надшлуночкова тахікардія має декілька різновидів. Зокрема, виділяють передсердну та а-в тахікардію.
Передсердна пароксизмальна тахікардія. Основна діагностична ознака – наявність зубців Р, пов’язаних із наступними шлуночковими комплексами. Вони мають змінену форму в порівнянні з синусовими Р. Інтервал РQ скорочений чи подовжений.
А-в пароксизмальна тахікардія. Різновиди відповідають а-в екстрасистоліям. Практично а-в пароксизмальну тахікардію з певністю можна діагностувати лише в тих випадках, коли на ЕКГ виявляються зубці Р, розташовані за комплексами QRS (-) у відведеннях ІІ, ІІІ, аVF.
А-в пароксизмальна тахікардія клінічно відрізняється від передсердної більшою стійкістю, більшою резистентністю до вагусних впливів та медикаментозних засобів.
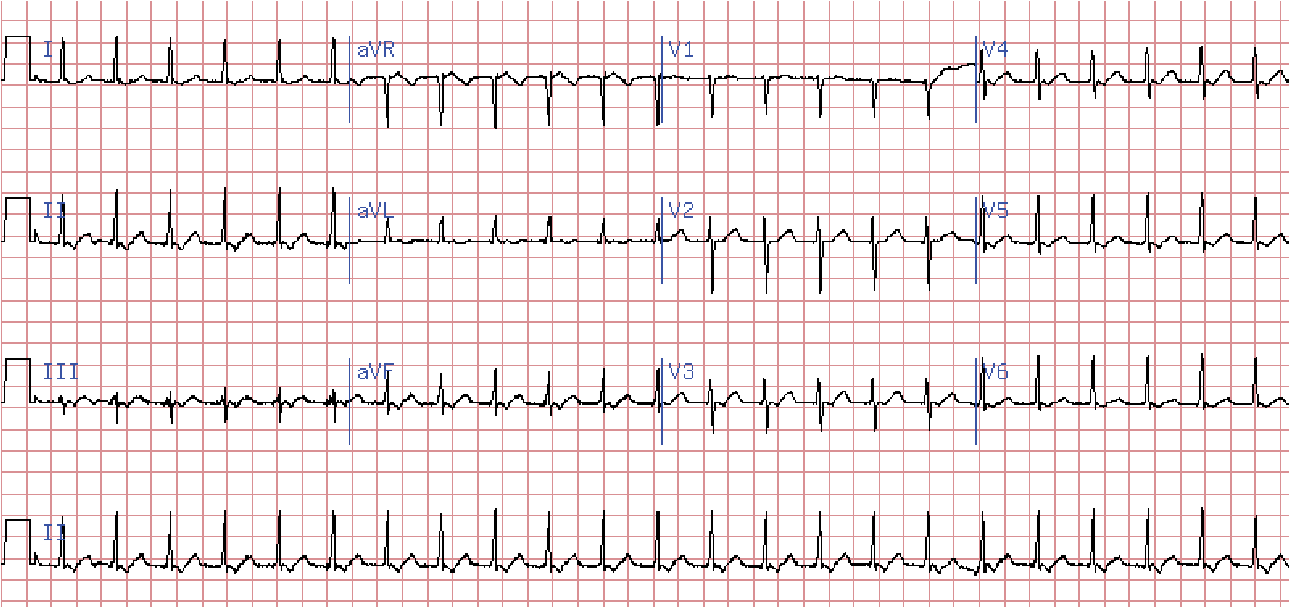
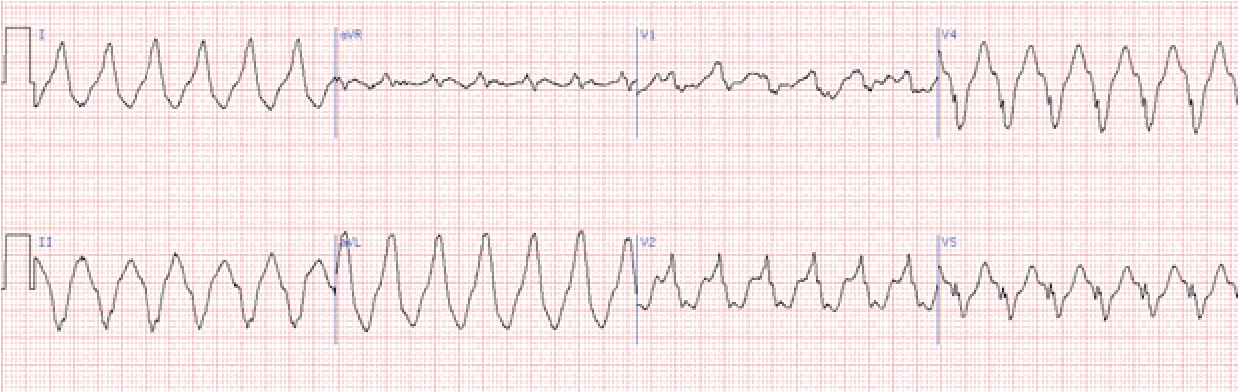
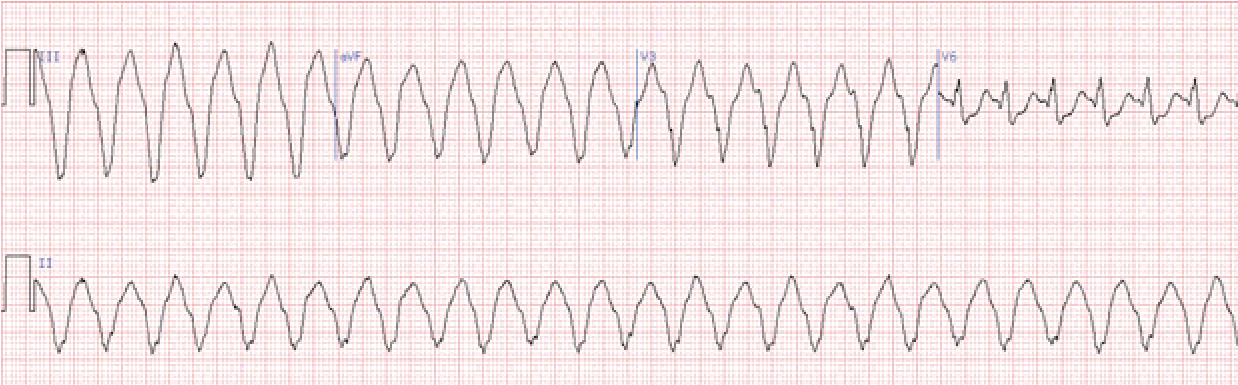
Ознаки: частота ритму 160–220, але може коливатись від 130 до 270 на хв. QRS деформовані, поширені (>0,12 с), SТ та Т дискор дантні основному зубцю (як при шлуночковій екстрасистолії).
Можуть реєструватися не пов’язані із шлуночковими комплексами зубці Р. Автономні зубці Р – не обов’язкова ознака шлуночкової тахікардії.
Певну допомогу в діагностиці шлуночкової тахікардії може створити виявлення у хворого в міжнападовому періоді шлуночкових екстрасистол, що мають аналогічну форму на ЕКГ (виникають із того ж ектопічного вогнища).
Локалізацію ектопічного вогнища при шлуночковій тахікардії визначають на підставі тих же ознак, що при шлуночковій екстрасистолії (по грудних відведеннях ЕКГ).
Шлуночкова тахікардія в більшості випадків трапляється при органічних захворюваннях серця. В деяких випадках дана аритмія може трансформуватися в тріпотіння та фібриляцію шлуночків, що нерідко спостерігається в гострій стадії інфаркту міокарда. Внаслідок цього шлуночкова тахікардія потребує активної терапії.
Миготлива аритмія трапляється в двох варіантах: тріпотіння передсердь та миготіння передсердь.
Тріпотіння передсердь характеризується ритмічною діяль ністю передсердь у дуже частому ритмі: від 250 до 370 на хв.
Діагностують на основі ритмічних пилкоподібних передсердних хвиль F на ЕКГ. Ці хвилі в одному і тому ж відведенні мають постійну форму. В типових випадках хвилі широкі, між ними немає ізоелектричного інтервалу. Звичайно хвилі краще видно у відведеннях ІІ, ІІІ, аVF і V1-2.
Шлуночкові комплекси можуть виникати ритмічно, слідуючи за кожною дугою, третьою, четвертою та так далі передсердною хвилею. В таких випадках говорять про правильну форму тріпотіння передсердь 2:1, 3:1 і т.д.
Форму тріпотіння передсердь з нерегулярним ритмом шлу ночків називають неправильною. Клінічно цю форму арит мії звичайно важко відрізнити від миготіння передсердь.
Існують пароксизмальна, персистуюча, та стійка, або постійна форма тріпотіння передсердь.
Тріпотіння передсердь зустрічається значно рідше, ніж інша форма миготливої аритмії – фібриляція передсердь. Ці форми можуть переходити одна в другу.
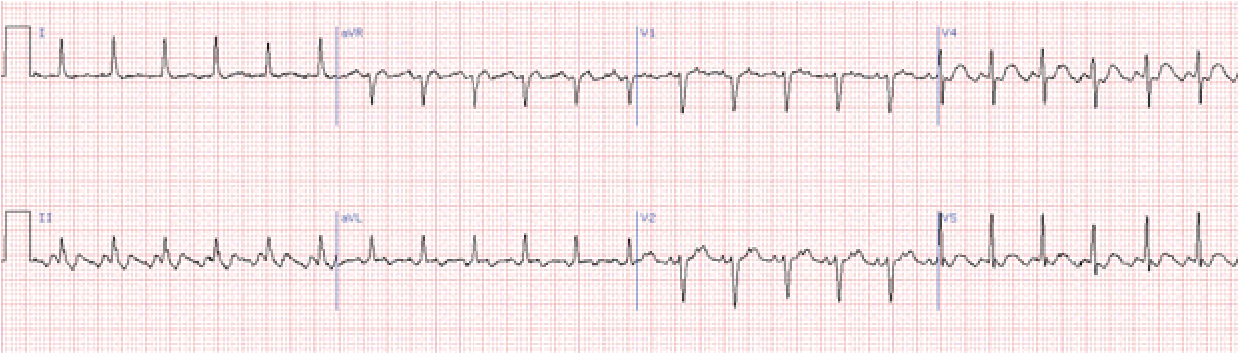
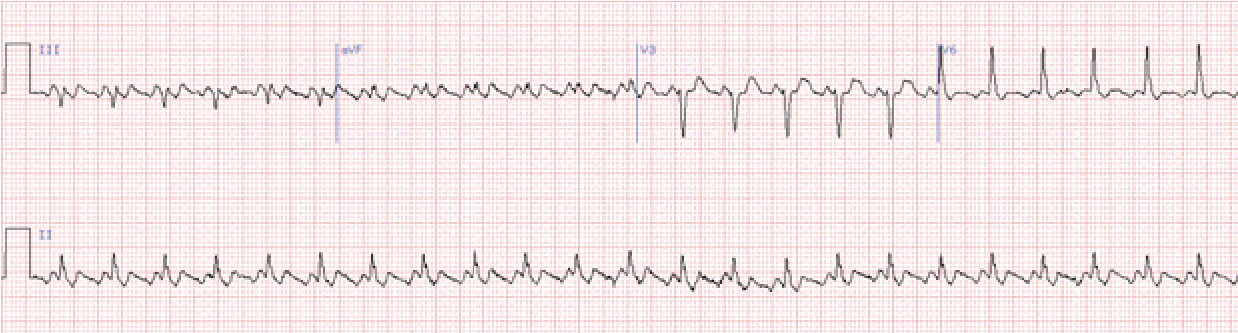
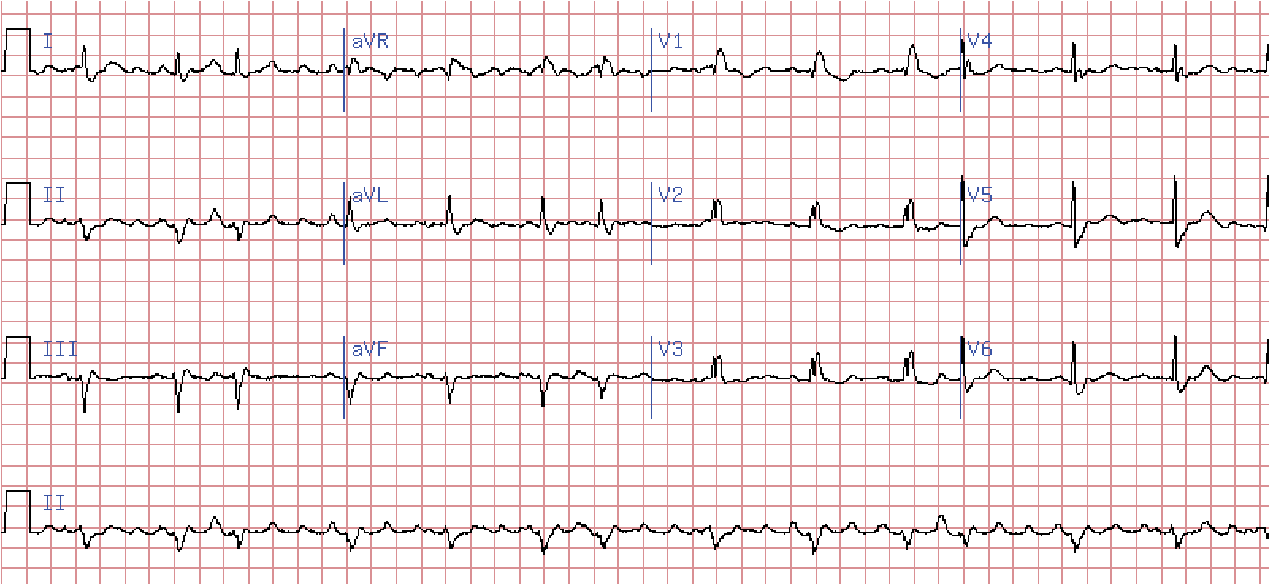
Миготіння (фібриляція) передсердь – це дуже часте, хаотичне збудження та скорочення окремих груп волокон міокарда передсердь. Частота імпульсів, що виникають у передсердях може коливатися від 370 до 700 на 1 хв. Більша частина цих імпульсів не доходить до шлуночків, затримуючись в а-в вузлі, і лише невелика частина досягає шлуночків, викликаючи їх неритмічне збудження. На ЕКГ відсутні зубці р, замість них виявляються безладні хвилі f, що мають різну форму і виникають з різною частотою. Ці хвилі зазвичай краще видно у відведеннях ІІ, ІІІ, а VF і V1, а в деяких випадках вони ледве помітні. В залежності від амплітуди хвиль f розрізняють крупно- та дрібнохвильову фібриляцію передсердь. Інтервали R-R мають різну тривалість.
Миготливу аритмію з шлуночковим ритмом 60–90 на хвилину називають нормосистолічною, менше 60 на 1 хв. – брадісистолічною, >90 на хв. – тахісистолічною.
Миготіння передсердь може бути пароксизмальним, персистуючим та стійким.
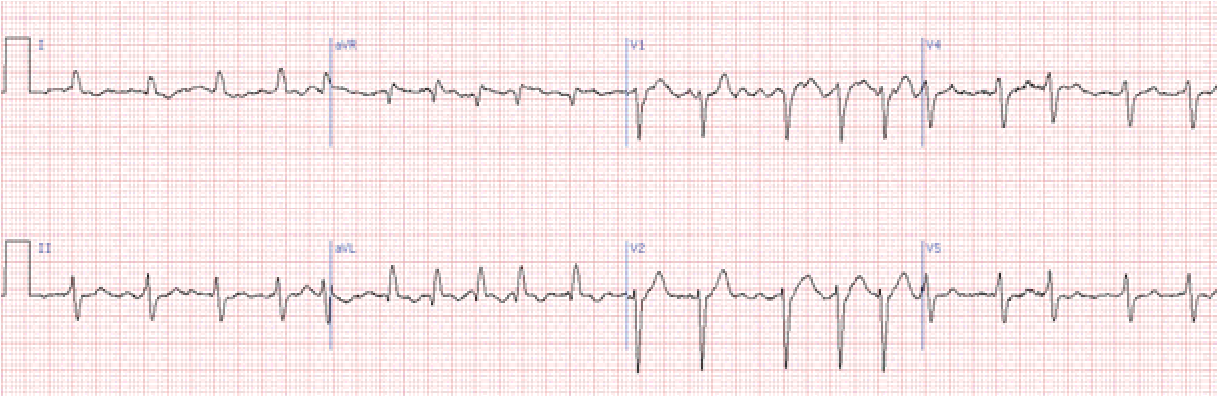

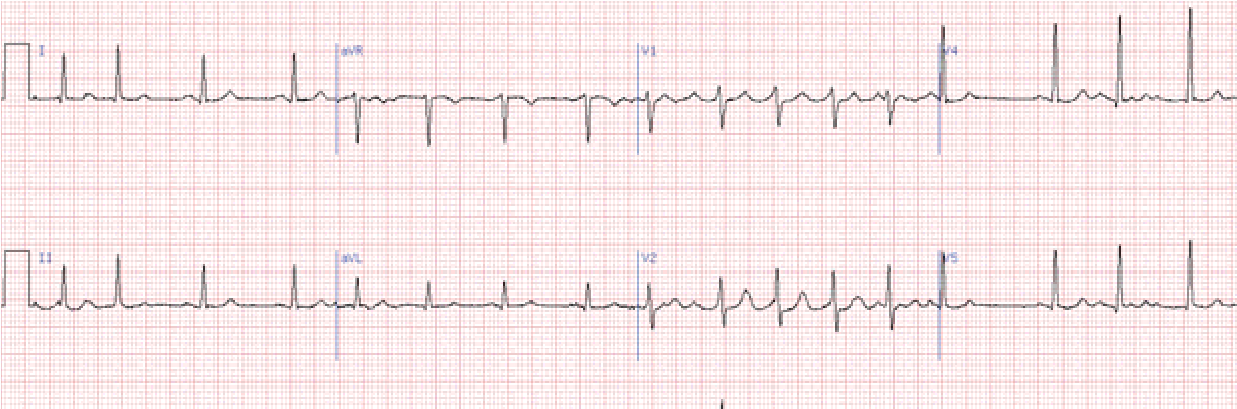
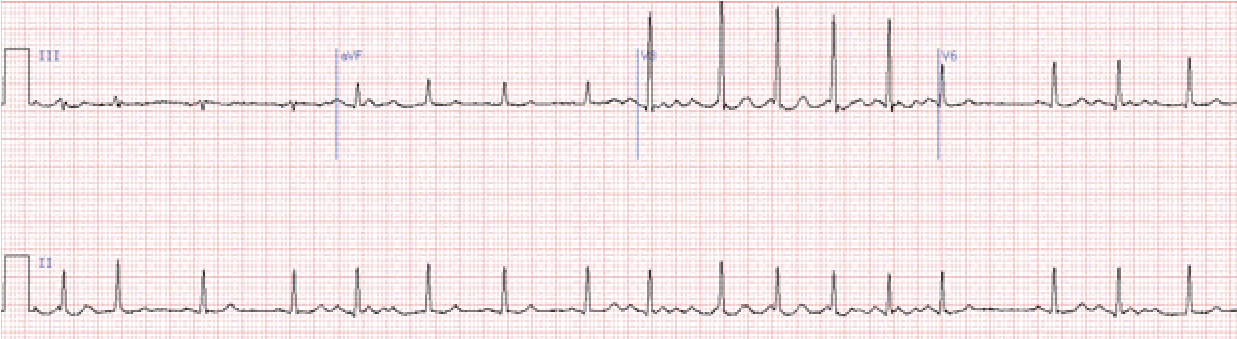
Сполучення миготіння передсердь та повної а-в блокади – це синдром Фредеріка.
Тріпотіння і фібриляція шлуночків
Тріпотіння і фібриляція шлуночків відносяться до аритмій, що викликають припинення ефективної гемодинаміки, тобто зупинку кровообігу. Ці порушення ритму є найбільш частою причиною раптової смерті кардіологічних хворих (аритмічна смерть).
Тріпотіння шлуночків – дуже часта, ритмічна, але неефективна діяльність міокарда шлуночків. На ЕКГ виявляється пилкоподібна крива з регулярними, ритмічними, однаковими за формою і амплітудою хвилями, де неможливо розрізни ти елементи шлуночкового комплексу і відсутні ізоелектрич ні інтервали (нагадує синусоїдальну криву).
Частота шлуночкового ритму при цьому 200–300 на хв.
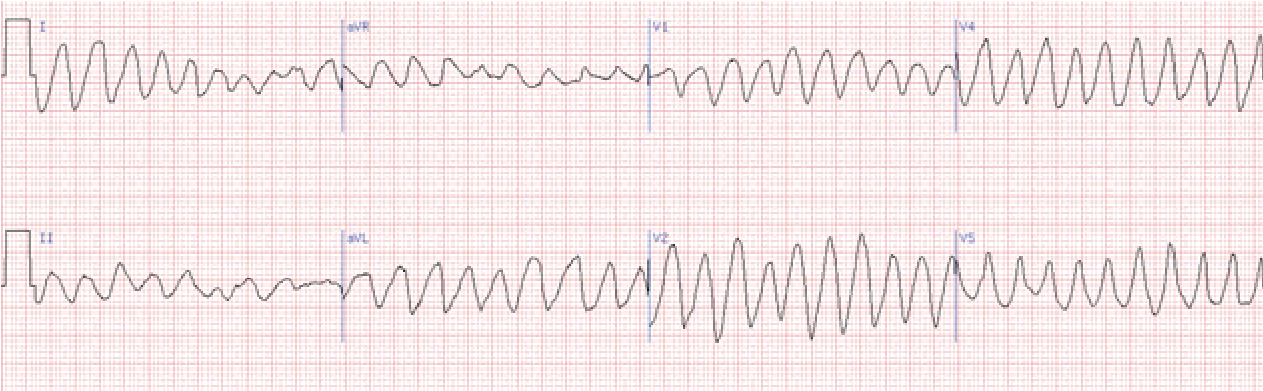
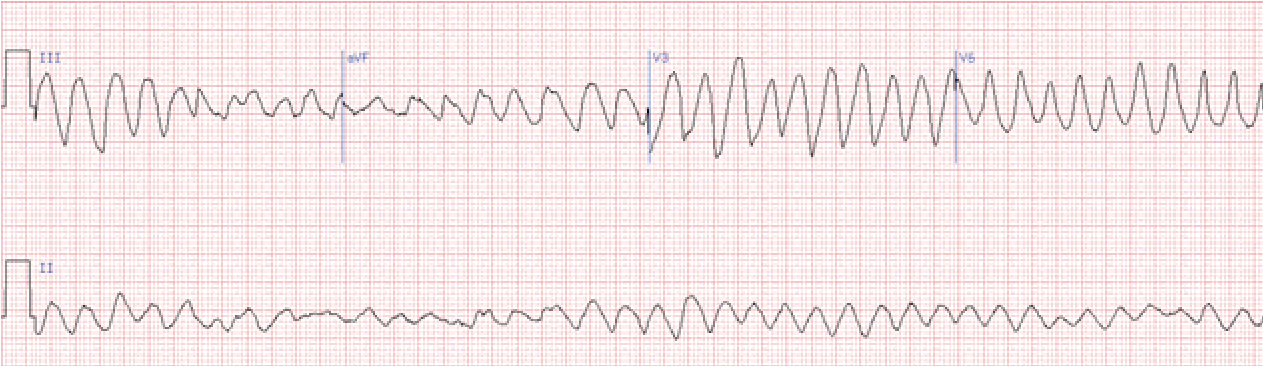
Фібриляція шлуночків – хаотичні, нерегулярні некоординовані скорочення волокон міокарда шлуночків. На ЕКГ реєструються часті (від 200 до 500 на хв.), нерегулярні хвилі різної форми і амплітуди. Розрізняють крупно- та дрібно хвильову фібриляцію. При крупно хвильовій фібриляції амплітуда хвиль перевищує 0,5 мВ, при дрібнохвильовій – не досягає цієї величини.
Блокади серця
Порушення провідності, або блокади серця – це сповільнення або повне припинення проведення імпульсу по якійсь ділянці провідної системи. В залежності від локалізації розрізняють: синоаурикулярну, внутріпередсердну, а-в та внутрішлуночкові блокади.
Синоаурикулярна (синоатріальна) блокада – порушення проведення імпульсу від синусового вузла до передсердь.
Розрізняють ІІІ ступені.
Частіше виникає СА блокада ІІ ст., коли частина синусових імпульсів не досягає передсердь. Діагностують на основі випадіння частини серцевих циклів на ЕКГ.
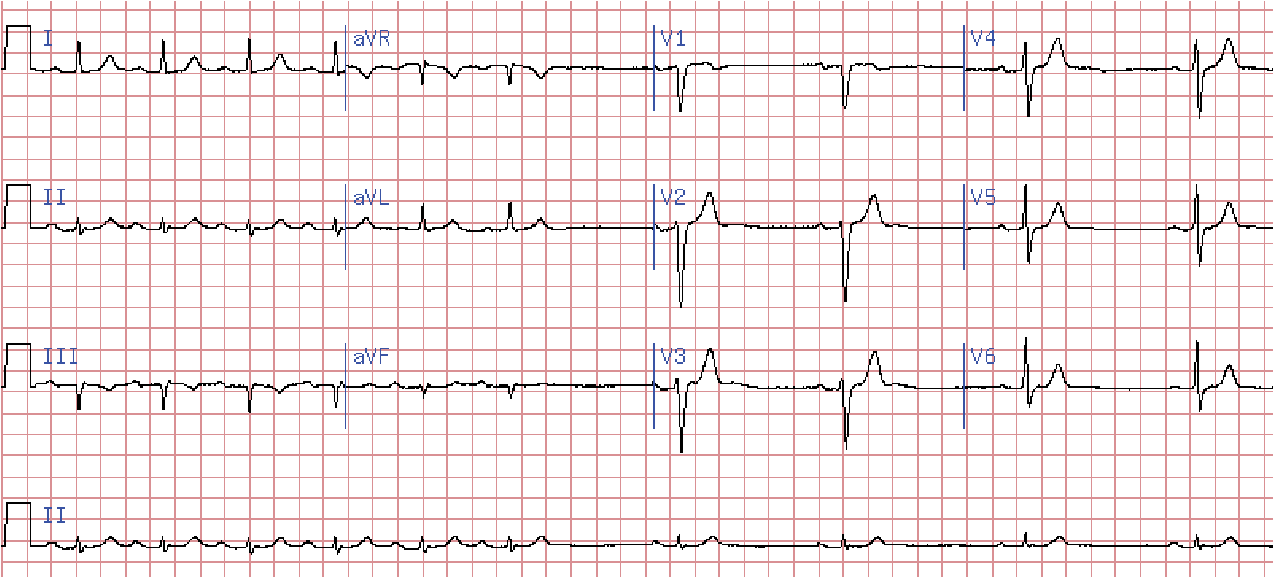
СА блокада ІІ ст. трапляється в двох варіантах (тип І і ІІ).
СА блокада ІІ ст. типу І (з періодами Венкебаха).
Можна вказати такі ЕКГ- критерії «класичного» типу І:
- інтервал R-R, що включає в себе блокований комплекс, коротший за подвоєний попередній інтервал;
- інтервал R-R, що настає за довгою паузою, довше ніж інтервал, що передує їй;
- перед довгими паузами відбувається поступове скорочення інтервалу R-R.
СА блокада ІІ ст. типу ІІ без періодів Венкебаха визначається за довгими паузами, в яких відсутні зубці Р та пов’язані з ними комплекси QRST. Якщо відбувається випадіння одного передсердно-шлуночкового комплексу, то подовжений інтервал R-R дорівнює подвоєному основному інтервалу R-R (як брадикардія). Але на відміну від брадикардії рQ не відповідає ЧСС.
Внутрішньопередсердною блокадою називається порушення проведення збудження по передсердних провідних шляхах. При неповній міжпередсердній блокаді І ст. спостерігається розширення зубця Р (>0,12с) та/або його розщеплення (двогорбий зубець Р).
Міжпередсердна блокада І ст. є частою електрокардіографічною знахідкою.
Атріовентрикулярна (а-в) блокада
А-в, або передсердно-шлуночковою блокадою називається розлад проведення збудження від передсердь до шлуночків.
Розрізняють а-в блокаду І, ІІ та ІІІ ст.
А-в блокада І ст. – сповільнення передсердно-шлу ночкової провідності з подовженням інтервалу РQ >0,2 с.
А-в блокада ІІ ст. При даному порушенні провідності деякі імпульси не проводяться від передсердь до шлуночків, що проявляється випадінням частини шлуночкових комплексів на ЕКГ.
Розрізняють 3 типи а-в блокади ІІ ст.
І тип, тип Венкебаха, або Мобітц-1 характеризується поступовим подовженням інтервалу рQ з наступним випадінням шлуночкового комплексу. Це явище називається періодами Венкебаха-Самойлова. Від комплексу до комплексу відбувається подовження інтервалу рQ, яке закінчується блокуванням останнього в періодиці зубця Р. Тривалість інтервалів R-R прогресуюче зменшується в міру наближення до довгої паузи (випадіння одного шлуночкового комплексу). Перед довгою паузою розташований найкоротший інтервал R-R. Довга пауза менша за подвоєний найкоротший інтервал R-R.
Якщо періодика відновлюється, то перший після довгої паузи інтервал рQ знову стає найкоротшим і далі все повторюється.

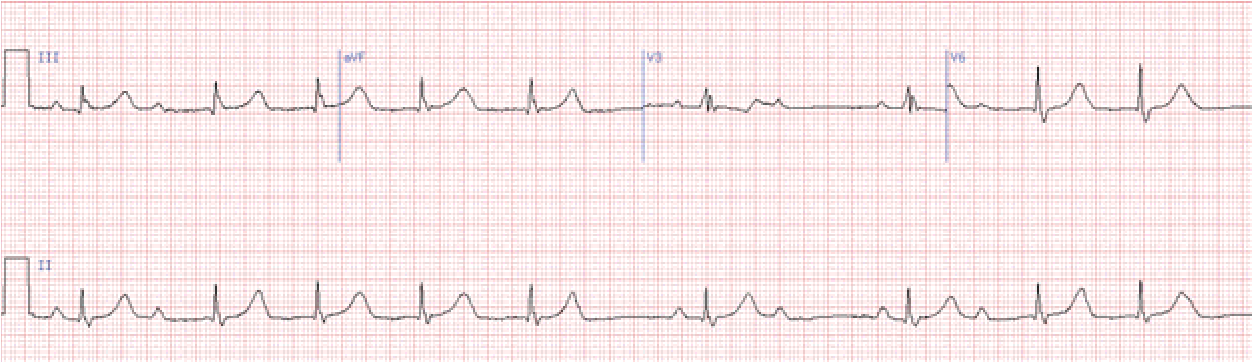
Вона характеризується випадінням шлуночкових комплексів на ЕКГ без попереднього поступового подовження інтервалу рQ, який залишається постійним.
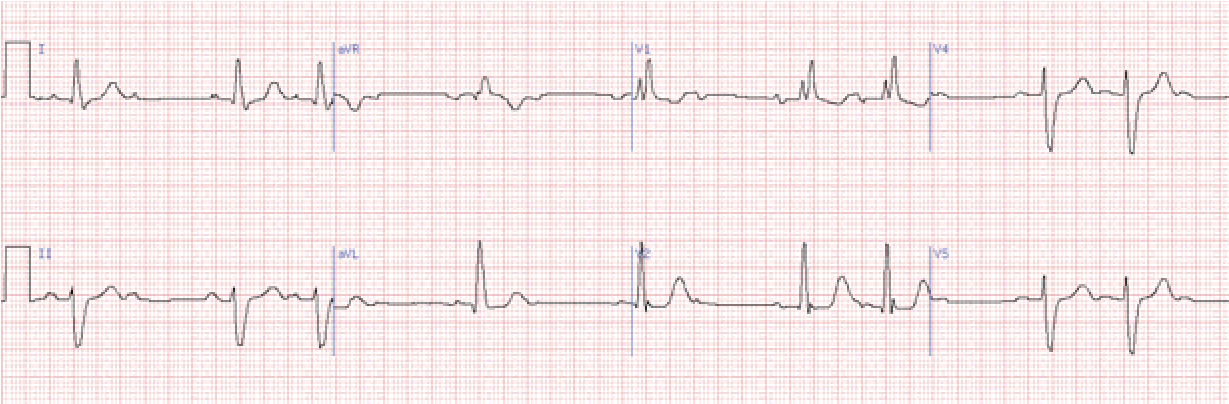
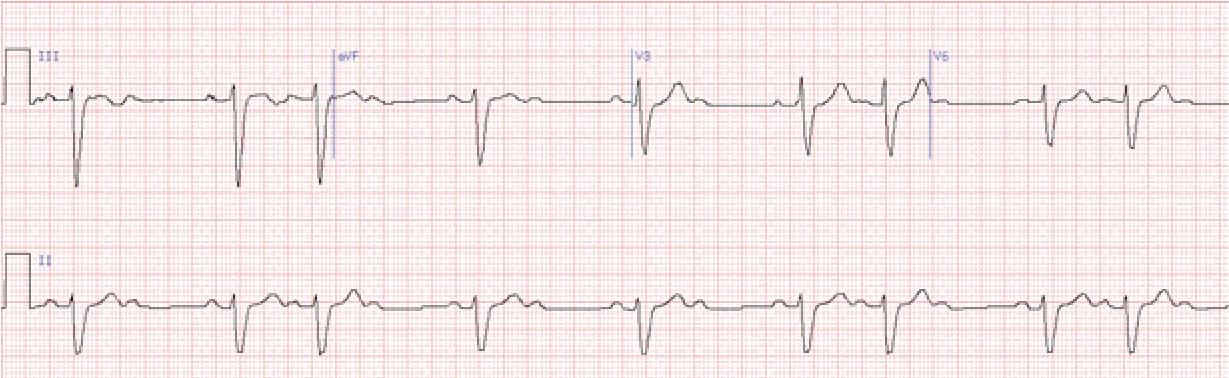
Характеризується випадінням двох та більше поспіль шлуночкових комплексів на ЕКГ. Дане порушення називають блокадою високого ступеня, а також такою, що далеко зайшла, або прогресуюча блокада, багаторазова, субтотальна.






При повній а-в блокаді імпульси з передсердь зовсім не проводяться до шлуночків, внаслідок чого передсердя і шлуночки функціонують незалежно один від одного. На ЕКГ виявляються зубці р, не пов’язані з шлуночковими комплексами. Шлуночки збуджуються у повільному ритмі.
Повна а-в блокада може бути пов’язана з ураженням проксимальних та дистальних відділів провідної системи. При проксимальній блокаді водій ритму шлуночків знаходиться в а-в з’єднанні, комплекси QRS не поширені, частота ритму шлуночків близько 50 на хв.
Повна а-в блокада дистального типу характеризується розширенням комплексу QRS>0,12 сек. та його деформацією, а також вираженою брадикардією, оскільки ідіовентрикулярні джерела ритму мають низький автоматизм.




Розрізнять повні та неповні, а також стійкі та такі, що переходять (минущі) блокади гілок пучка Гіса.
Блокада правої ніжки пучка Гіса
У відведеннях V1-2 комплекси QRS мають М-подібну форму: rSR, RSR, rsR, RsR, або широкі та розщеплені зубці R.
У лівих грудних відведеннях виявляються широкі зубці S, що відбивають деполяризацію правого шлуночка.
Якщо ширина комплексу QRS не перевищує 0,12 с, то мова йде про неповну блокаду.
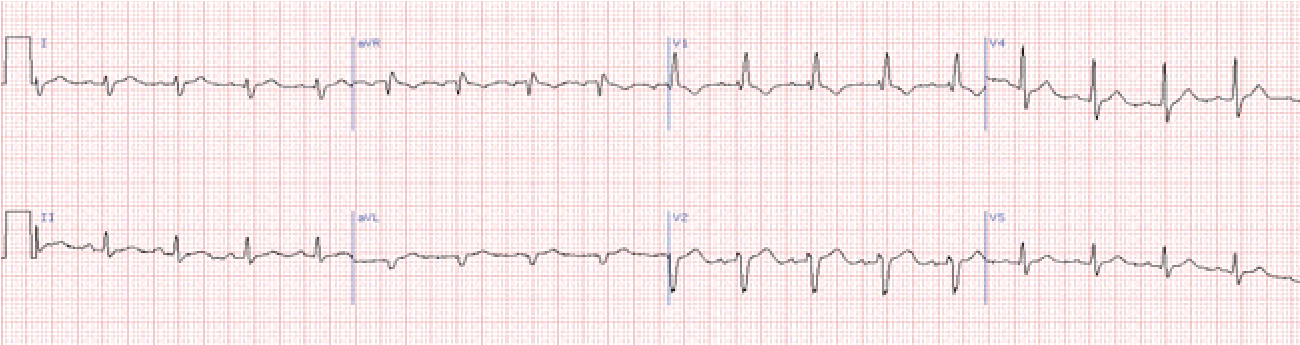
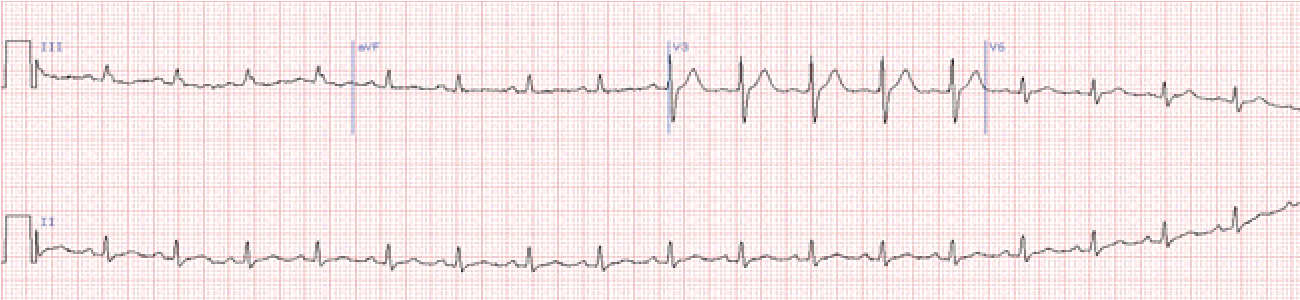
Розширення комплексу >0,12 с вказує на повну блокаду.
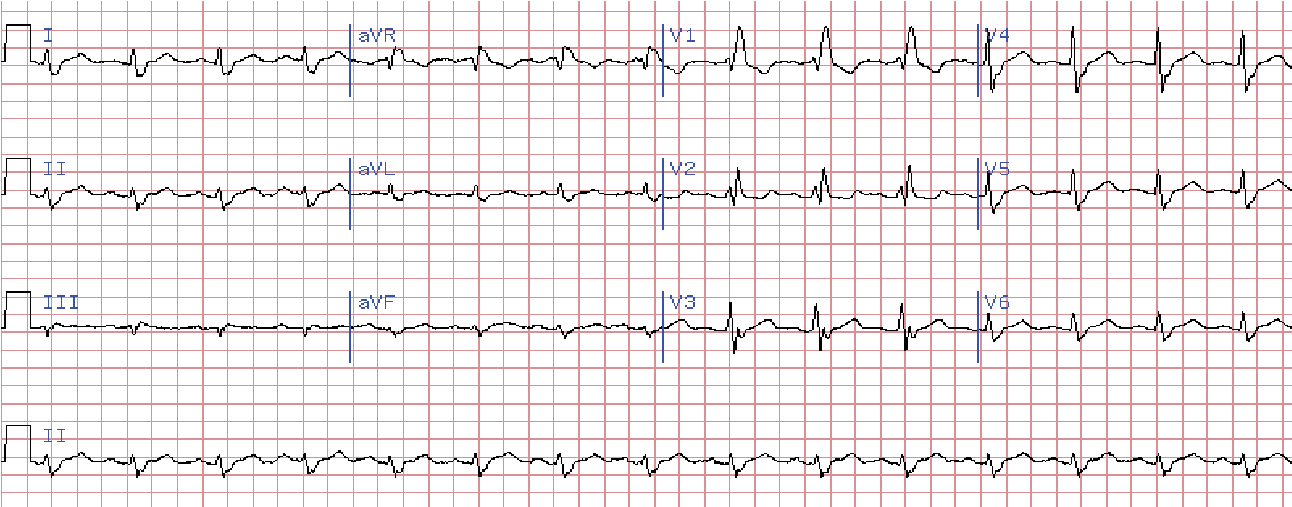
Сегмент ST та зубець Т розташовані дискордантно основному зубцю комплексу QRS. У V1 – від’ємний зубець Т та депресія сегмента ST дискордантно зубцю R, що в даному відведенні є основним.
Форма комплексів QRS у відведеннях від кінцівок залежить від положення електричної осі серця, наявності гіпертрофії шлуночків та від провідності по лівих гілках пучка Гіса.
Часто глибокі S у І, ІІ, ІІІ, aVL, aVF.
У відведенні аVR реєструється пізній високий та широкий зубець R, в ІІІ – комплекс QRS частіше має форму rSr.
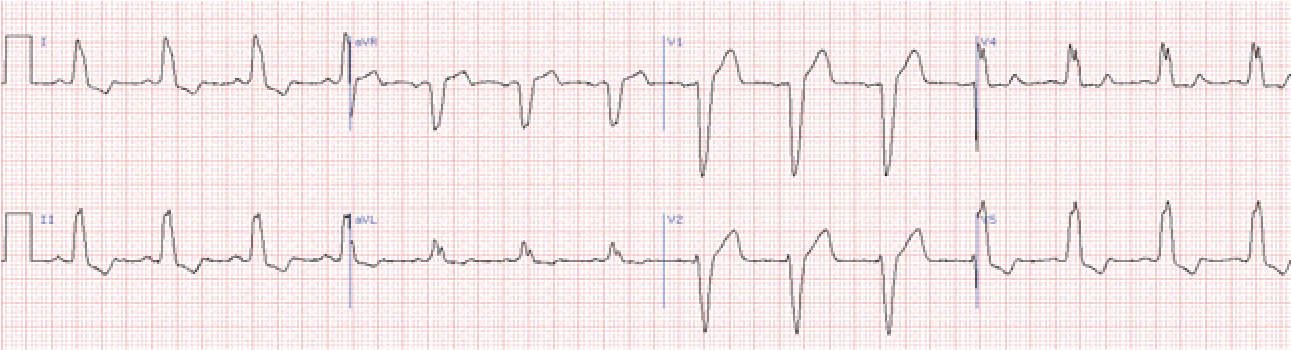
Блокада лівої ніжки пучка Гіса
У відведеннях V1-2 реєструється широкий S або rS.
У відведеннях V5-6 – широкий та розщеплений зубець R, відсутній зубець q.
Дискордантне щодо ведучого зубця комплексу положення сегмента ST та зубця Т (у V5-6 – вниз).
Електрична вісь серця частіше розташована горизонтально або відхилена вліво.
Ширина комплексу QRS збільшена.
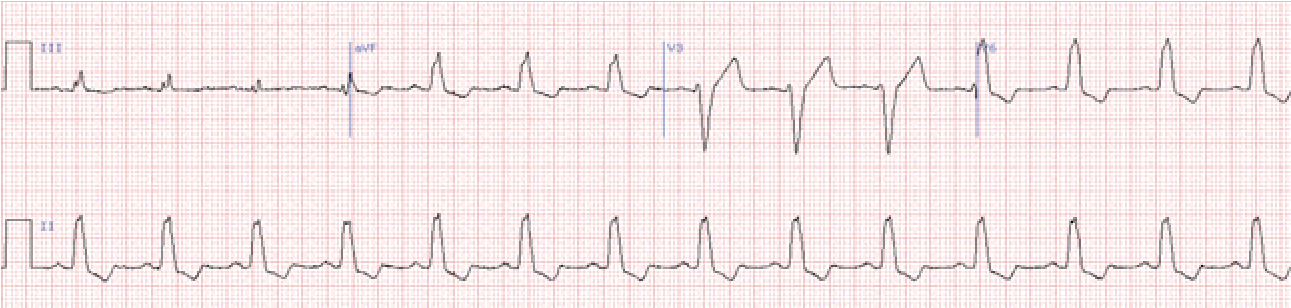
Блокада лівої передньої гілки (передньо-верхній геміблок)
Комплекс QRS суттєво не розширений.
Основною діагностичною ознакою є значне відхилення електричної вісі серця вліво. – при цьому перевищує – 300.
Зубець RаVLRІ.
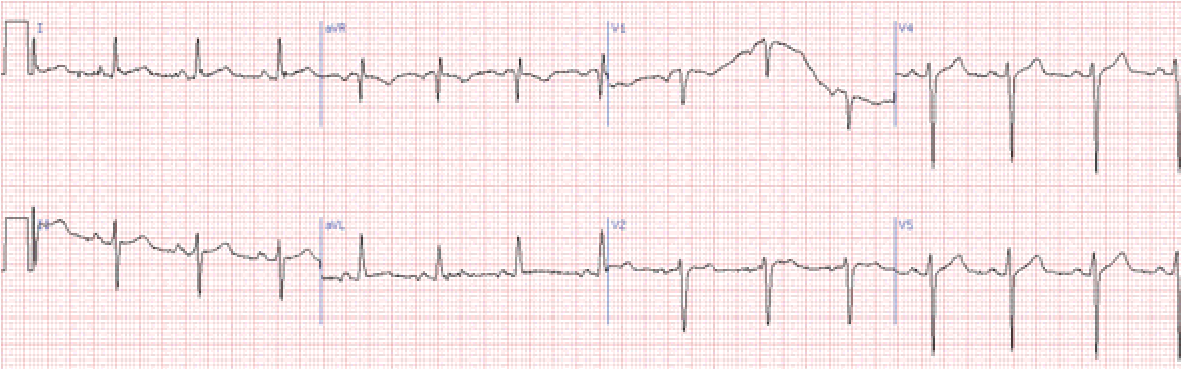
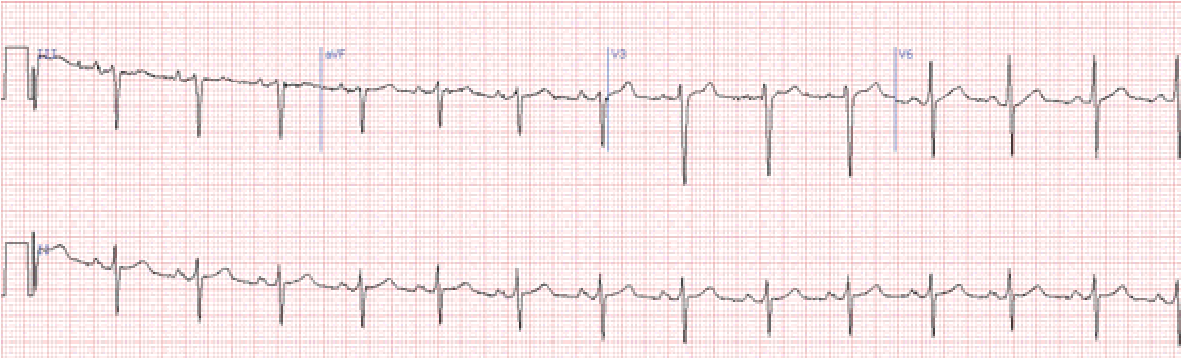
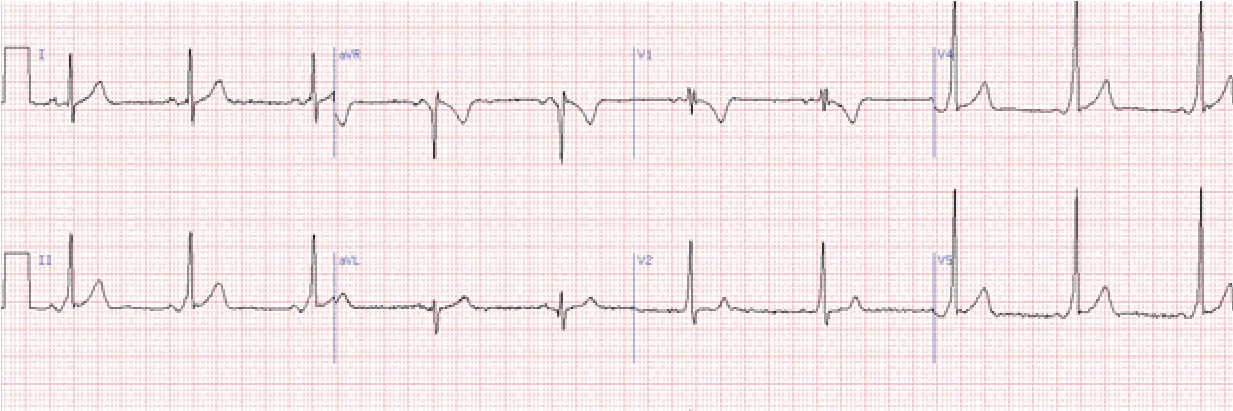
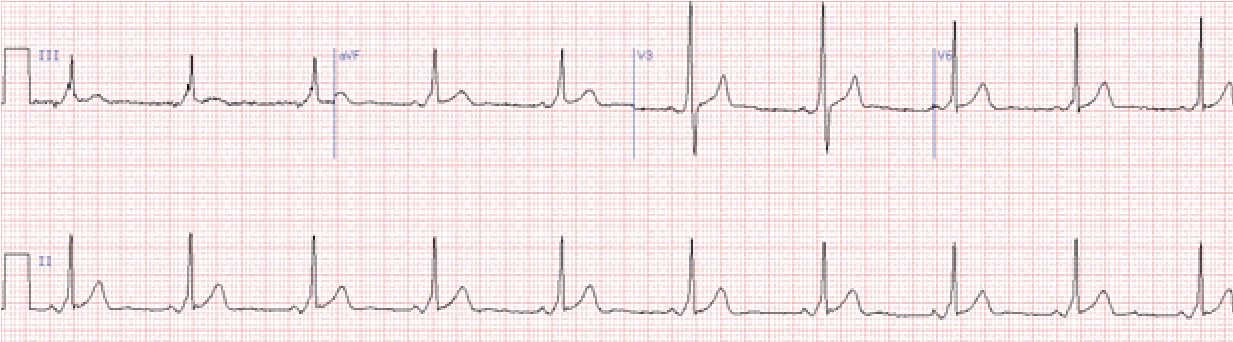
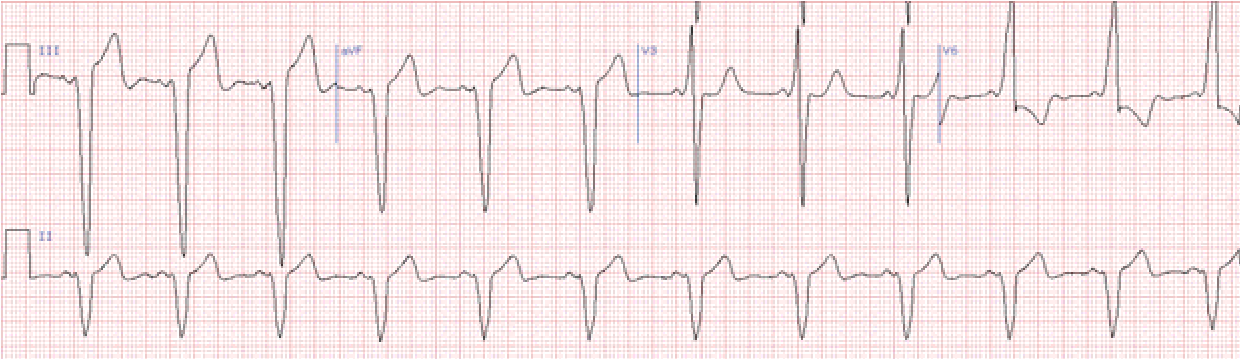
Блокада лівої задньої гілки (задньо-нижній геміблок)
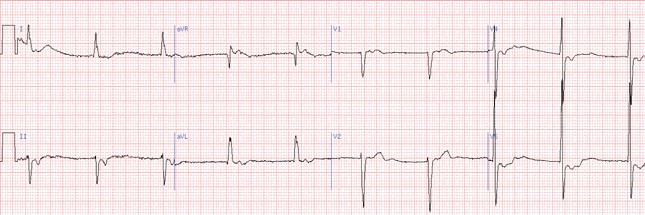
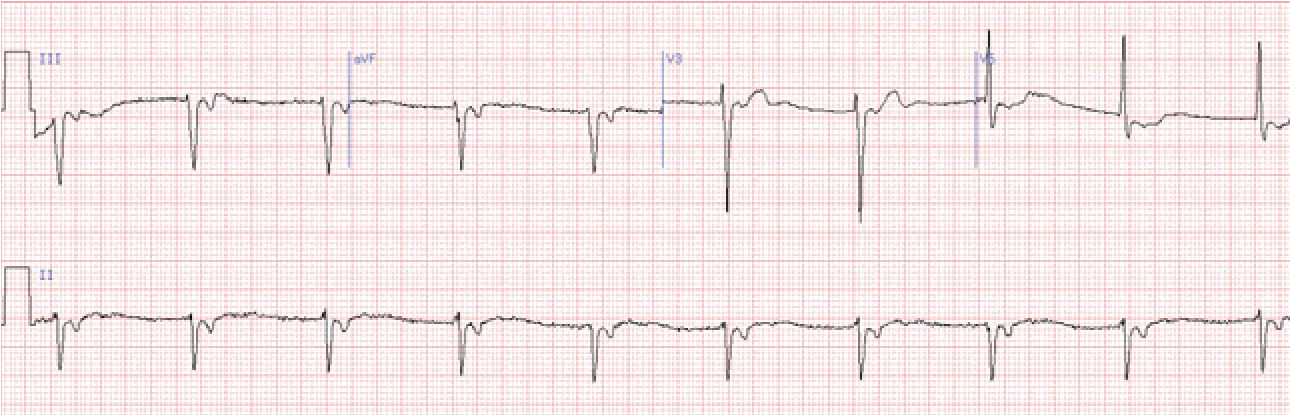
Характерне відхилення електричної осі серця вправо, у відведеннях ІІ, ІІІ, аVF основний зубець R, a у І, aVL – S. Ці ознаки неспецифічні й бувають при гіпертрофії правого шлуночка або при гострому легеневому серці, тому дане порушення провідності можна діагностувати лише виключивши вказані стани.





Класифікація антиаритмічних препаратів
І Блокатори швидких натрієвих каналів
ІА – хінидин, новокаїнамід, гілуритмал дизопірамід
ІВ – лідокаїн, тримекаїн, мексилетин, дифенін
ІС – етацизин, етмозин, пропафенон (рітмонорм), флекаїнід, алапінін
ІІ – β – адреноблокатори
ІІІ – ті, що збільшують потенціал дії та сповільнюють реполяризацію, блокатори калієвих каналів – аміодарон (кордарон), бретілій, соталол
ІV – блокатори повільних кальцієвих каналів – верапаміл, дилтіазем
Деякі автори виділяють ще 2 групи:
- – специфічні брадикардитичні препарати (алінідин)
- – препарати, що стимулюють пуринергічні рецептори міокардіоцитів (аденозин, АТФ)
Пропафенон (ритмонорм) має якості ІС підкласу та одночасно є β-адреноблокатором та антагоністом кальцієвих каналів.
Лікування екстрасистолії
Лікування екстрасистолії залежить від її клінічного і прогностичного значення. При лікуванні екстрасистолії слід мати на увазі:
а) наявність або відсутність структурного захворювання серця, ступінь ризику життєво небезпечних шлуночкових аритмій;
б) суб’єктивну переносимість аритмії.
Показаннями для призначення антиаритмічних препаратів при екстрасистолічній аритмії є:
- значне збільшення кількості екстрасистол на фоні прогресуючого перебігу захворювання;
- часті, політопні, парні, групові та ранні «R» на «Т» шлуночкові екстрасистоли, які є загрозливими щодо переходу в пароксизмальну шлуночкову тахікардію і фібриляцію шлуночків;
- алоритмія (бі-, три-, квадригемінія), короткі пробіжки передсердної тахікардії, які супроводжуються СН;
- екстрасистолічна аритмія, яка виникає при захворюваннях, що сприяють розвитку аритмогенних ефектів (пролабування мітрального клапана, синдром подовженого інтервалу Q-Т тощо);
- виникнення або збільшення частоти екстрасистол під час нападів стенокардії або гострого інфаркту міокарда;
- шлуночкові екстрасистоли після припинення нападу шлуночкової тахікардії і фібриляції шлуночків;
- екстрасистоли, які виникають на фоні аномальних шляхів проведення (синдромів WPW та СLС).
Хворі з «доброякісною» екстрасистолією спеціальної анти аритмічної терапії не потребують. При екстрасистолії в осіб молодого віку без структурного ураження серця антиаритмічні препарати зазвичай не призначаються. При суб’єктивній непереносимості екстрасистолії показані седативні засоби, транквілізатори або антидепресанти. Хворі з захворюваннями внутрішніх органів і екстрасистолією потребують адекватного лікування основного захворювання та призначення психотропних засобів. При вегетативній дисфункції показані β-адреноблокатори або М-холінолітики (атропін тощо).
Для лікування клінічно вираженої надшлуночкової екстрасистолії препаратами вибору є антагоністи кальцію (верапаміл, дилтіазем), а препаратами резерву – β-адрено блокатори. За відсутності ефекту цих препаратів переходять до призначення препаратів І класу або комбінації антиаритмічних препаратів із різними механізмами дії.
Хворі з прогностично несприятливими аритміями, рефрактерними до антиаритмічної терапії, з вираженими порушеннями гемодинаміки, коронарного кровотоку або в поєднанні з пароксизмами шлуночкової тахікардії і фібриляції шлуночків потребують хірургічного лікування (деструкція ектопічного вогнища, імплантація протитахікардитичних пристроїв або використання інших підходів).
Лікування суправентрикулярної пароксизмальної тахікардії
Рефлекторні методи купірування базуються на подразненні блукаючого нерва, підвищенні його тонусу.
Проба Вальсальви – затримка дихання з натуженням на висоті вдиху.
Проба Чермака – Геринга – масаж ділянки коритидного синуса.
Проба Ашнера – Данні – тиск великими пальцями на очні яблука нижче надбрівних дуг.
Відтворення рвотного рефлексу.
«Рефлекс пірнання» – занурення обличчя в холодну воду з затримкою дихання.
Проба з надуванням повітряної кулі.
Фармакотерапія
Препаратами вибору є верапаміл та АТФ.
Верапаміл вводиться внутрішньовенно струменево 2 мл 2,5% розчину (5 мг) за 5 хв. або 4 мл (10 мг) за 10 хв. у нерозчиненому вигляді. При відсутності ефекту повторюють введення в тій же дозі.
АТФ вводиться в/в струменево без розчинення 1–2 мл 1% розчин протягом 5–10 сек. При відсутності ефекту введення можна повторити в тій же дозі.
Пропафенон (рітмонорм) 2 мг/кг (150 мг) в/в за 10 хв., далі в/в крапельно – 2 години.
Аміодарон (кордарон) вводиться в/в струменево 6 мл 5% розчину протягом 2–3 хв., потім в/в крапельно 6 мл в 250 мл 5% розчину глюкози протягом 1–2 годин.
Обзидан – 5 мл 0,1% розчину розводять у 10 мл ізотонічного розчину NаСІ.
Ефективність протиаритмічних препаратів збільшується на фоні введення препаратів К+ або поляризуючої суміші.
Електрична кардіоверсія робиться при неефективності медикаментозної антиаритмічної терапії.
Показання:
- розвиток гострої лівошлуночкової недостатності
- аритмічний колапс
- гостра коронарна недостатність (розвиток під час нападу пароксизмальної тахікардії
- нестабільної стенокардії або інфаркту міокарда).
Черезстравохідна електрокардіостимуляція Показання:
- порушення гемодинаміки
- неефективність антиаритмічних препаратів або наявність протипоказань до них;
- суправентрикулярна пароксизмальна тахікардія, що обумовлена застосуванням антиаритмічних засобів (тобто їх аритмогенним ефектом).
Імплантація постійного антитахікардіального електрокардіостимулятора проводиться хворим з тяжкими формами суправентрикулярної пароксизмальної тахікардії, рецидивними і рефрактерними до медикаментозної антиаритмічної терапії.
Хірургічне лікування
Покази:
- Частота скорочень шлуночків більше 200 за хв. під час тахікардії.
- Порушення гемодинаміки під час тахікардії.
- Молодий вік хворого.
- Вагітність.
- Наявність у одного хворого додаткового шляху проведення та миготливої аритмії.
- Неефективність медикаментозної терапії або непереносимість.
- Інвалідизація хворих.
Хірургічне лікування полягає у видаленні ділянки розташування аритмогенного вогнища, його ізоляції або модифікації.
Профілактика
Дози: верапаміл-ретард 240 мг на добу, пропафенон – 10 мг/кг/добу в 3 прийоми через кожні 8,
годин соталол – 3–5 мг/кг/добу в 2 прийоми, кордарон – по 200 мг на добу 5 днів поспіль, 2 дні перерви обзідан – 240 мг на добу
Шлуночкова тахікардія
Пароксизм шлуночкової тахікардії з вираженою гемодинамічною нестабільністю
Показана екстрена електрична кардіоверсія або шлуночкова кардіостимуляція.
Гемодинамічно незначуща шлуночкова тахікардія
Робиться прекардіальний удар, вирішується питання про в/в ведення препаратів.
- Новокаїнамід – 10 мл 10% розчину розводять у 10 мл фізіологічного розчину і вводять в/в струменево під контролем АТ. Препарат ефективний у 70% випадків шлуночкової тахікардії;
- Аміодарон. Препарат призначають як при збереженій, так і при зниженій фракції викиду лівого шлуночка в дозі 300–450 мг в/в струменево або в/в крапельно протягом 1 години. Потім 15 мг/кг в/в повільно наступні 23 години;
- Лідокаїн призначається для купірування шлуночкової тахікардії при гострому інфаркті міокарда та нестабільній стенокардії. 80–120 мг (4–6 мл 2% розчину), 0,5 мл (10 мг) на кожні 10 кг ваги в/в струменево в 10 мл ізотонічного розчину NaCl протягом 1,5 хв із наступним в/в крапельним введенням 2 мг/кг.
Підтримуюча антиаритмічна терапія при шлуночковій тахікардії:
- аміодарон
- антиаритмічні препарати І класу при некоронарогенних шлуночкових тахікардіях
- верапаміл
- β-адреноблокатори
Електрична кардіоверсія
Покази:
- неефективність медикаментозної антиаритмічної терапії;
- тяжкі клінічні прояви з самого початку нападу пароксизмальної тахікардії (гостра лівошлуночкова недостатність, колапс, гостра коронарна недостатність).
Електрокардіостимуляція (ендокардіальна, черезстравохідна) показана при неефективності медикаментозної антиаритмічної терапії і електричної кардіоверсії.
Хірургічне лікування
Установка кардіовертера-дефібрилятора.
Радіочастотна абляція.
Аневризмектомія.
Останній метод – пересадка серця.
Лікування миготливої аритмії Купірування пароксизма
Електрична кардіоверсія, якщо напад супроводжується вираженими гемодинамічними порушеннями з розвитком обмороку, колапсу, серцевої астми, набряку легень, стенокардії.
Якщо пароксизм фібриляції передсердь (ФП) триває до 48 годин, то його можна купірувати без повноцінної антикоагулянтної підготовки, проте виправдане введення або нефракціонованого гепарину 4000–5000 Од в/в, або низькомолекулярних гепаринів (надропарину кальція 0,6 або еноксипарину натрія 0,4 п/ш).
Якщо пароксизм ФП триває більше 48 годин, перед відновленням ритму необхідно провести повноцінну антикоагулянтну терапію (варфарин).
Перше в житті хворого в/в введення антиаритмічного препарату проводять під контролем моніторування ЕКГ. Якщо відома ефективність якогось препарату, перевагу надають йому.
При ФП тривалістю не більше 7 днів рекомендовані: пропафенон аміодарон (доказана ефективність) або новокаїнамід, хінідін (менш ефективні).
При ФП тривалістю більше 7 днів рекомендовані: аміодарон (доведена ефективність), менш ефективні новокаїнамід, пропафенон, хінідін.
Не можна використовувати для купірування пароксизмальної форми ФП серцеві глікозиди та соталол.
Кардіоверсія пропафеноном
Пропафенон вводиться 2 мг/кг (150 мг) в/в за 10 хв., далі в/в крапельно – 2 години (75 мг).
Кардіоверсія аміодароном
Аміодарон вводиться 5 мг/кг (300 мг) в 250 мл 5% розчину глюкози впродовж 1 години, далі 15 мг/кг (900 мг) в 500 мл 5% розчину глюкози впродовж наступних 23 годин.
Кардіоверсія новокаїнамідом
Новокаїнамід вводиться в/в струменево 10 мл 10% розчину в 10 мл ізотонічного розчину NaCl повільно впродовж 8–10 хв. під постійним контролем АТ, ЧСС та ЕКГ. Хінідін 0,2 – по 1 т. один раз у 6–8 год. (не >0,6 за добу).
Профілактика:
- хінідін 0,2 1 т. 2–3 рази на добу;
- пропафенон 0,15 по 1т. 3–4 рази на добу;
- соталол 0,08–0,32 (на 2 або 3 прийоми);
- аміодарон 1 т. на день.
При неефективності антиаритмічних препаратів, при збереженні частих, погано переносимих пароксизмів ФП необхідно розглянути питання про проведення радіочастотної абляції.
При відсутності ефекту від радіочастотної катетерної абляції показано призначення терапії, що уріжає ритм (дігоксин з β-адреноблокатором) для зменшення тахісистолії під час пароксизму в сполученні з антикоагулянтами) аспірином.
Існують дві принципові стратегії в лікуванні персистуючої та постійної форми ФП:
- стратегія контролю ритму: відновлення синусового ритму з наступною профілактикою рецидивів;
- стратегія контролю ЧСС: збереження ФП з до сягненням адекватного уріження ЧСС та постійною повноцінною антикоагулянтною терапією.
При рецидивуючій персистуючій формі ФП з успіхом можна використовувати обидві стратегії лікування.
Відновлення синусового ритму слід прагнути, якщо можна розраховувати на безпечність кардіоверсії та достатньо тривале утримання синусового ритму. Додатковою підставою вибирати тактику контролю ритму є молодий та середній вік хворих, погана переносимість аритмії, перша спроба усунення аритмії.
Вибір тактики контролю ЧСС виправданий у осіб старше 65 років, що мають фактори ризику інсульту або транзиторну ішемічну атаку в анамнезі, інші епізоди тромбоемболії в анамнезі, не кориговані клапанні вади серця (або термін < 6 міс. з моменту проведення хірургічної корекції вади серця), виражені структурні зміни міокарда лівого шлуночка (фракція викиду < 40%, кардіомегалія, постінфарктний кардіосклероз, хронічна аневризма), виражене збільшення розмірів лівого передсердя (>5,5–6 см), тромб у лівому передсерді за даними черезстравохідної ЕхоКГ, активний ревматизм, міокардит, тиреотоксикоз, ожиріння важкого ступеня, наявність в анамнезі синдрому слабкості синусового вузла, давність ФП більше 3 років, невеликий термін (менше 6 міс.) збереження синусового ритму після попереднього усунення ФП.
Вибрана тактика контролю ритму. Перед проведенням кардіоверсії необхідно провести 3–4-тижневу повноцінну антикоагулянтну підготовку (варфарин до досягнення МНС 2,0–3,0).
Після відновлення ритму варфарин призначають упродовж 4 тижнів (мінімум).
Підготовка включає призначення антиаритмічного препарату (аміодарон 0,6–0,8 на добу за 2 тижні до кардіоверсії).
При персистуючій формі ФП перевагу має електрична кардіоверсія.
Її ефективність складає 90–96%.
Підготовка до кардіоверсії може включати призначення панангіна (6–8 т. на добу) за 7–10 днів до електричної кардіоверсії, препарати, що уріжають ЧСС – β-адреноблокатори або верапаміл (відміняють за добу до кардіоверсії), дігоксин (відміняють за 3–4 доби).
Контроль ЧСС при хронічній формі ФП.
- дігоксин 0,125–0,25 на добу;
- верапаміл SR 120 мг х 2 рази або 240 мг на добу;
- ділтіазем SR 120 мг х 2 рази або 240 мг;
- β – блокатори.
Додатково:
- соталол 40–160 мг на добу;
- аміодарон 100–300 мг на добу.
Найбільш оптимальним є комбіноване призначення серцевих глікозидів із β-блокаторами або антагоністами Са.
Нефармакологічне лікування ФП
- хірургічна абляція;
- катетерна абляція;
- передсердне стимулювання;
- внутрішні передсердні дефібрилятори.
Лікування тріпотіння передсердь
Основний метод – радіочастотна катетерна абляція кава-трикуспідального перешийку (істмуса). Ефективність метода складає 90–95%.
Інші особливості лікування тріпотіння передсердь (ТП) такі:
- для купірування ТП на будь-якому етапі можна використати черезстравохідну стимуляцію серця (особливо при непереносимості / неефективності антиаритмічних препаратів). При пароксизмі ТП приблизно в 2/3 випадків відновлюється синусовий ритм, в 1/3 ТП трансформується у ФП;
- при використанні електроімпульсної терапії для купірування ТП використовують розряд меншої потужності (100–200 Дж);
- при використанні антиаритмічних препаратів І класу є небезпека до уріження частоти хвиль тріпотіння з переходом до проведення 1:1;
- незважаючи на менший ризик тромбоемболічних ускладнень, показання до призначення антикоагулянтів аналогічні таким при ФП;
- при проведенні уріжаючої ритм терапії хворим із постійною формою ТП слід домагатися трансформації тріпотінням у фібриляцію передсердь, яка легше піддається уріженню (дігоксин цьому сприяє, аміодарон, соталол навпаки запобігають). Можливе проведення черезстравохідної стимуляції серця з метою трансформації у ФП (при відповідній підготовці на випадок відновлення синусового ритму).
Лікування порушень функції провідності
Тактика і методи лікування порушень провідності (блокад серця) визначаються основним захворюванням, рівнем і ступінем порушення провідності, вираженістю клінічних проявів.
Якщо блокада не супроводжується вираженими клінічними проявами, то вона не потребує спеціального лікування. Провідність може відновитись при упішному лікуванні основного захворювання (міокардиту, ревматизму, інфаркту міокарда, порушень електролітного балансу), відміні антиаритмічних засобів, що викликають порушення провідності.
Лікування СА блокади
Невідкладні лікувальні заходи проводяться у хворих СА блокадою ІІ–ІІІ ст. у тих випадках, коли вона супроводжується вираженою брадикардією, порушеннями гемодинаміки, повторними епізодами втрати свідомості, синдромом Морганьї-Адамса-Стокса. В цих випадках найбільш ефективним методом є електрична кардіостимуляція.
Хворим із нападами асистолії, з клінікою синдрому Морганьї -Адамса-Стокса, що гостро розвинувся внаслідок СА блокади, показано застосування тимчасової електрокардіостимуляції.
Може бути використана також черезстравохідна електрокардіостимуляція.
При синдромі Морганьї-Адамса-Стокса, що часто повторюється, необхідна імплантація постійного кардіостимулятора.
При неможливості проведення електрокардіостимуляції назначаються лікарські засоби, що полегшують проведення імпульсу від синусового вузла до передсердь (холінолітики, стимулятори β-адренорецепторів), які збільшують частоту ритму серця.
- атропін – 0,5–1 мл 0,1% розчину п/ш 2–3 рази на день або по 10 крапель 3 рази на день внутрішньо, при необхідності можна ввести в/в;
- настій екстракту беладони – по 20 крапель 3 рази на день, белоїд – по 1–2 др. 3 рази на день (у неважких випадках);
- ефедрин – по 0,025 2–3 рази на день або по 1 мл 5% розчину п/ш 2–3 рази на день;
- ізадрин – по 1 т. (0,005) під язик 3 рази на день;
- алупент – 0,5–1 мл 0,05% розчину в/м (у важких випадках в/в) 2–3 рази на день, внутрішньо 0,02 (1 т.) 3 рази на день;
Слід пам’ятати, що застосування β-стимуляторів інколи може призвести до виникнення ектопічних аритмій (у цьому випадку необхідно зменшити дозу або відмітити препарат).
Лікування а-в блокад
Лікування а-в блокади І ст.
Як правило, проводиться лише лікування основного захворювання.
При а-в блокаді І ст. із блокадою ніжки пучка Гіса, що розвинулася у хворих на гострий інфаркт міокарда, показана профілактична ендокардіальна електрокардіостимуляція (трифасцикулярна блокада може перейти в повну а-в блокаду).
Лікування а-в блокади ІІ ст.
При а-в блокаді ІІ ст., тип І або Мобітц І (з періодами Самойлова-Венкебаха), коли випадіння рідкі, спеціального лікування не треба. Необхідно спостереження.
При а-в блокаді ІІ ст., тип ІІ і особливо ІІІ при рідкому ритмі проводиться таке ж лікування, як при повній а-в блокаді.
Лікування а-в блокади ІІІ ст.
При а-в блокаді ІІІ ст., що гостро розвинулася, хворого необхідно госпіталізувати, визначити вид лікування, з’ясувати, чи потрібно застосовувати тимчасову електрокардіостимуляцію.
При ЧСС>40 на хв., при відсутності загрозливих симптомів, доброму самопочутті хворого специфічного лікування не проводять.
Показання до тимчасової електрокардіостимуляції:
- Напади Морганьї-Адамса-Стокса.
- Рідкий ритм шлуночків (<40 на хв.).
- Недостатність кровообігу, що розвивається.
- Повна а-в блокада у хворого на гострий інфаркт міокарда передньої стінки.
- Необхідність введення препаратів, що сповільнюють а-в провідність.
- Несправність постійного кардіостимулятора.
При неможливості проведення електрокардіостимуляції призназначають препарати, що прискорюють ритм шлуночків (холінолітики, β-адреностимулятори).
При блокаді, що розвинулась гостро внаслідок міокардиту, інфаркту міокарда доцільно призначити лікування преднізолоном у дозі 60–120 мг в/в із наступним переходом на прийом внутрішньо 60 мг на добу з поступовим зниженням дози.
При хронічній а-в блокаді ІІІ ст. проводиться медикаментозне лікування або постійна електрокардіостимуляція.
Показання до постійної електрокардіостимуляції:
- Рідкий шлуночковий ритм (<40 на хв.).
- Напади Морганьї-Адамса-Стокса або головокружіння.
- Розвиток хронічної недостатності кровообігу.
- Розвиток артеріальної гіпертензії.
Лікування синдрому Морганьї-Адамса-Стокса
Синдром Морганьї-Адамса-Стокса – періоди асистолії шлуночків, що приводять до гіпоксії головного мозку і втрати свідомості. Найбільш частими причинами синдрому є повна а-в блокада (особливо момент переходу неповної а-в блокади ІІ ст. в повну), синдром слабкості синусового вузла, шлуночкова тахікардія, тріпотіння і фібриляція шлуночків.
Невідкладна допомога при синдромі Морганьї-Адамса-Стокса
Перші етапи допомоги однакові для фібриляції і асистолії шлуночків:
- Удар кулаком у ділянку грудини.
- Зовнішній масаж серця.
- Штучна вентиляція легень.
- Електрична дефібриляція (вона купірує фібриляцію шлуночків, але може «запустити» серце і при асистолії).
Одночасно з початком і на фоні реанімаційних заходів налагоджується ЕКГ-дослідження.
- Екстрена електрокардіостимуляція при діагностиці асистолії шлуночків. Найбільш ефективна ендокардіальна кардіостимуляція, коли активний електрод вводиться через підключичну вену в правий шлуночок.
- При неможливості або затримці проведення кардіостимуляції проводять медикаментозну терапію: в/в вводять адреналіну гідрохлорид 0,5–1 мл 0,1% розчину в 5 мл ізотонічного розчину натрію хлориду. Алупент вводять в/в краплинно 1–2 мл 0,05% розчину в 200 мл ізотонічного розчину натрію хлориду. При повній а-в блокаді ефективний атропіна сульфат в/в 1 мл 0,1% розчину в 10 мл ізотонічного розчину NaCl.