Рефлюкс-езофагіт та стравохід Баррета
Патофізіологія
Патологічний рефлюкс шлункового вмісту розвивається, коли рефлюкс долає антирефлюксні бар’єри шлунково-стравохідного переходу. Первинним антирефлюксним механізмом є нижній стравохідний сфінктер (НСС), який скорочується, щоб підтримувати тиск вище шлункового. Анатомічне порушення шлунково-стравохідного з’єднання, яке зазвичай асоціюється з грижею стравохідного отвору діафрагми (рис. 4.1), робить свій внесок у патогенез рефлюксної хвороби, порушуючи функцію НСС. Грижа стравохідного отвору діафрагми особливо важлива у пацієнтів з тяжким езофагітом, пептичною стриктурою або стравоходом Барретта. Хронічний низький тиск у НСС є домінуючим механізмом у пацієнтів з ГЕРХ з вираженим рефлюксом, а порушення стравохідного кліренсу також може бути іншою патофізіологічною причиною, як і у пацієнтів зі склеродермією (рис. 4.2).
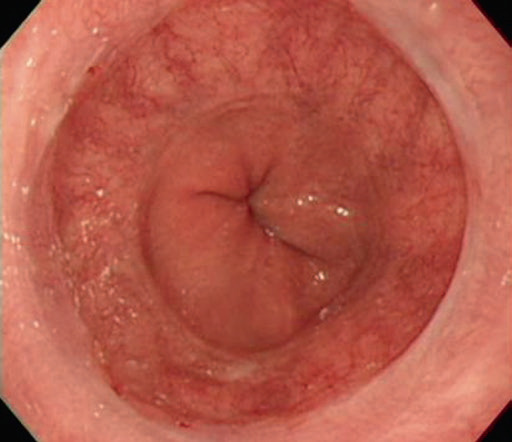

Рис. 4.1 Грижа стравохідного отвору діафрагми. Грижа стравохідного отвору діафрагми визначається як випинання частини шлунка через діафрагмально-стравохідний отвір. Тиск на нижній стравохідний сфінктер знижується через втрату черевного тиску та зміщення стравохідного отвору діафрагми.
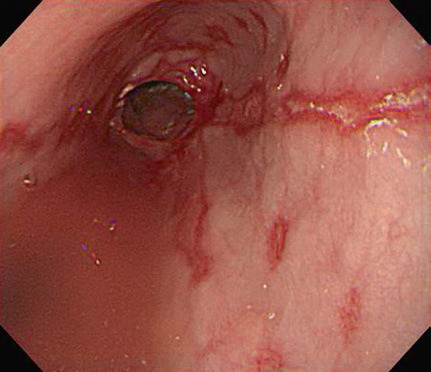
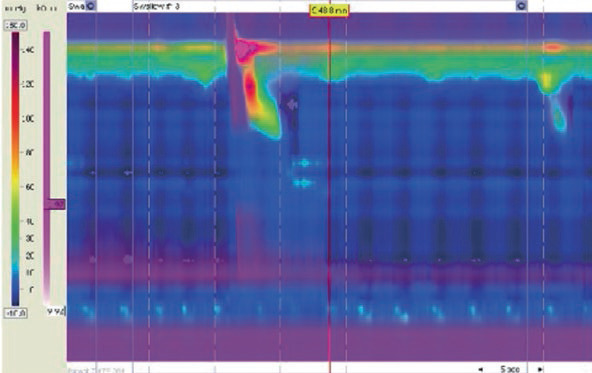
Рис. 4.2 Рефлюкс-езофагіт у пацієнтів зі склеродермією.
Клінічні характеристики
Печія та регургітація є типовими клінічними проявами ГЕРХ (табл. 4.1). Наявність “тривожних симптомів і ознак” – дисфагія, одінофагія, втрата ваги, постійна нудота та блювання, довга тривалість симптомів (>10 років) та відсутність відповіді на лікування – є підставою для проведення ендоскопічного обстеження.
| Типові | Нетипові |
|---|---|
| Печія | Блювота |
| Відрижка | Біль у грудях |
| Одинофагія | Хронічний кашель |
| Дисфагія | Охриплість голосу |
Показання до проведення ендоскопічного дослідження
Ендоскопія верхніх відділів травної системи дозволяє не тільки діагностувати рефлюкс-езофагіт, але й виявити будь-які ускладнення, такі як стриктури або стравохід Барретта. Пацієнти, які не реагують на відповідну антисекреторну медикаментозну терапію або мають інші клінічні ознаки, що вказують на ускладнену ГЕРХ, повинні бути обстежені за допомогою ендоскопії. Слід також розглянути інші методи діагностики, такі як амбулаторний рН-моніторинг, стравохідна манометрія або багатоканальна імпедансометрія. Ендоскопія також є тестом вибору у пацієнтів, які мають ризик розвитку стравоходу Барретта. Показання до ендоскопічного дослідження верхніх відділів стравоходу у пацієнтів з ГЕРХ наведені в таблиці 4.2.
Таблиця 4.2 Показання до ендоскопії у пацієнтів з ГЕРХ
- Симптоми рефлюксу, які є постійними або прогресуючими навіть після прийому антисекреторних препаратів
- Ненавмисна втрата ваги
- Дисфагія або одінофагія
- Анемія
- Підозра на позастравохідні прояви ГЕРХ
- Скринінг стравоходу Барретта
- Блювота
- Рецидивні симптоми після ендоскопічного або хірургічного антирефлюксного лікування
Діагностика та класифікація рефлюкс-езофагіту
Ендоскопічними ознаками рефлюкс-езофагіту є ерозії або виразки, що охоплюють ділянку від дистального відділу стравоходу до лінії Z зі смугастим характером поширення, які є результатом пошкодження слизової оболонки стравоходу та запалення під впливом кислоти (рис. 4.3). Наявність цих типових ендоскопічних знахідок дозволяє діагностувати ГЕРХ зі специфічністю 90-95%. Щонайменше 50% пацієнтів із симптомами рефлюксу мають нормальну ендоскопічну картину стравоходу, що називається неерозивною рефлюксною хворобою. Повторна ендоскопія не показана пацієнтам без стравоходу Барретта за відсутності нових симптомів. Однак ендоскопічне дослідження слід повторно проводити у пацієнтів з тяжким ерозивним езофагітом після антисекреторної терапії, щоб виключити наявність стравоходу Барретта.
Ступінь і тяжкість пошкодження слизової оболонки можна оцінити ендоскопічно. Лос-Анджелеська класифікація кількісно визначає довжину та окружність пошкоджень слизової оболонки при рефлюкс-езофагіті.
Існує кілька класифікацій для оцінки ендоскопічної тяжкості ерозивного рефлюкс-езофагіту та пов’язаних з ним ускладнень. Ці системи класифікації в основному використовуються в клінічних дослідженнях для вивчення ефективності медикаментозної терапії при лікуванні рефлюкс-езофагіту, а також корисні в клінічній практиці для документування тяжкості захворювання. Найчастіше використовується Лос-Анджелеська класифікація (табл. 4.3 і рис. 4.4), яка має добру внутрішньо- і міжспостережну узгодженість, а також високу кореляцію зі ступенем впливу кислоти стравоходу, визначеним за допомогою 24-годинного рН-моніторингу. Біопсію стравоходу слід проводити для виключення інших діагнозів, у тому числі інфекційної етіології та злоякісних новоутворень, за таких умов: пацієнти з ослабленим імунітетом, неправильна або глибока виразка, наявність масивного ураження або вузлуватості, неправильна або злоякісна стриктура.
| Ступінь | Характеристика |
|---|---|
| A | ≥1 розрив слизової оболонки довжиною не більше 5 мм без переходу на складки слизової оболонки |
| B | ≥1 розрив слизової оболонки довжиною більше 5 мм без переходу між складками слизової оболонки |
| C | ≥1 розрив слизової оболонки, який є безперервним між вершинами двох або більше складок слизової оболонки, але займає менше 75% окружності |
| D | ≥1 розрив слизової оболонки, який охоплює щонайменше 75% окружності стравоходу |
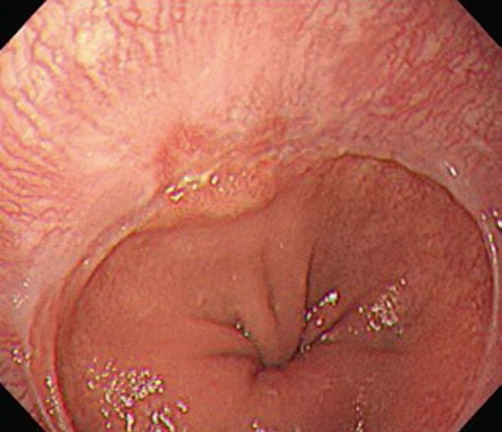
Рис. 4.3 Типова картина рефлюкс-езофагіту. Показана смугаста виразка з еритемою від Z-лінії
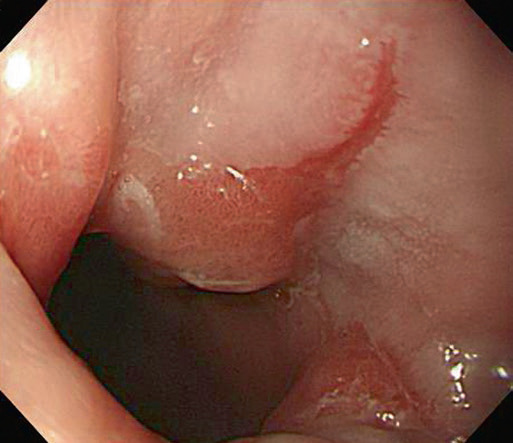
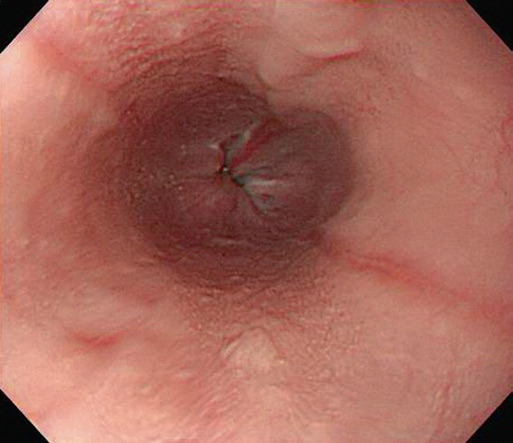
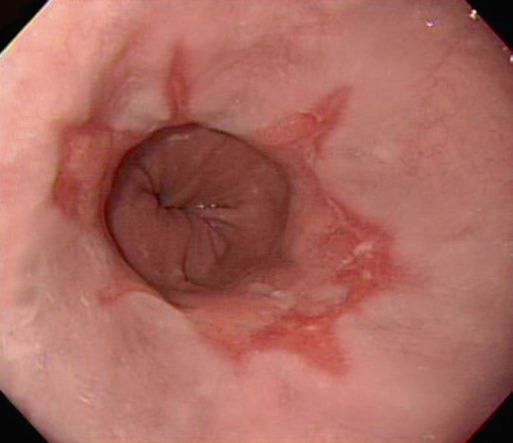
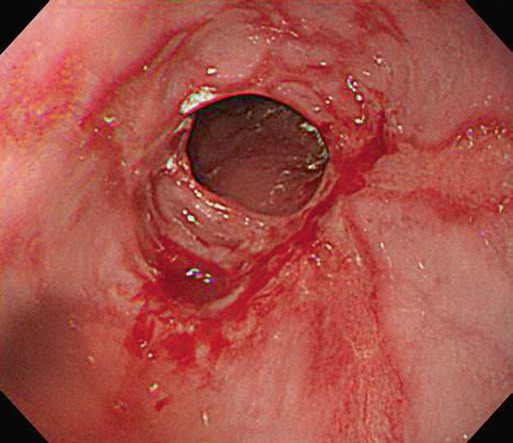
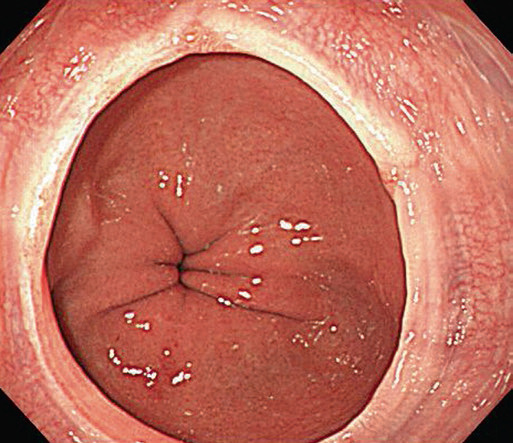
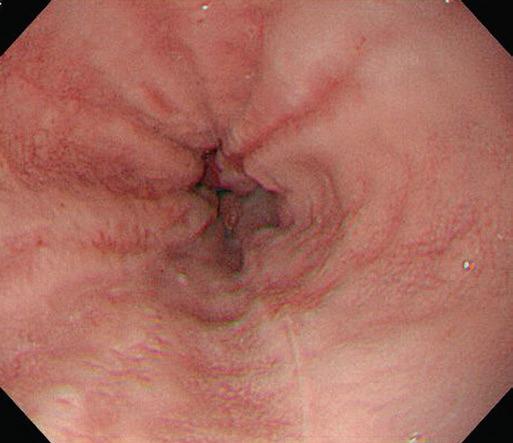
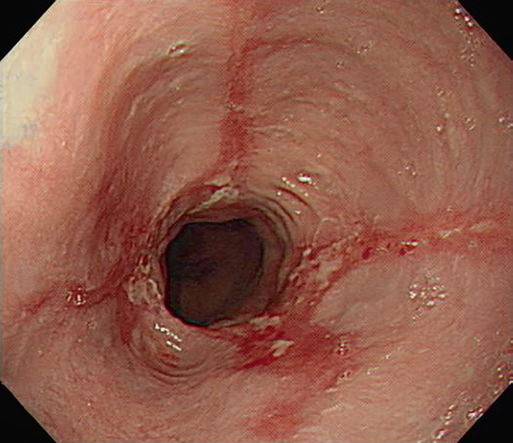
Рис. 4.4 Лос-Анджелеська класифікація рефлюкс-езофагіту. (a) Ступінь А, одиночна лінійна ерозія (<5 мм завдовжки) в дистальному відділі стравоходу, (b) Ступінь В, множинні лінійні ерозії та еритематозні смуги (>5 мм завдовжки), (c) Ступінь С, лінійні виразки стають циркулярними, (d) Ступінь D, тяжке захворювання з циркулярною глибокою виразкою в ділянці шлунково-стравохідного з’єднання над сфінктером стравоходу
Мінімальні зміни
Існує інша класифікація ГЕРХ, згідно з якою так звані мінімальні зміни слизової оболонки – набряк, рихлість та еритема, білувате помутніння, дрібнозернисті зміни, ексудат, рихлість слизової оболонки та невидимість судин – є ознаками неерозивного рефлюкс-езофагіту. Однак варіабельність цих результатів між спостерігачами є надто низькою. Для подолання низької узгодженості були розглянуті нові методи, такі як NBI (вузькосмугове зображення) та ендоскопія зі збільшенням. Система NBI покращує візуалізацію мікросудин і структури слизової оболонки. У поєднанні зі збільшенням у пацієнтів з НЕРБ можна спостерігати ендоскопічні аномалії. Патерн ворсинчастих/гребеневих ямок, підвищена васкуляризація, мікроерозія, збільшення кількості інтрапапілярних капілярних петель або звивистість можуть спостерігатися як ознаки НЕРХ (рис. 4.5).
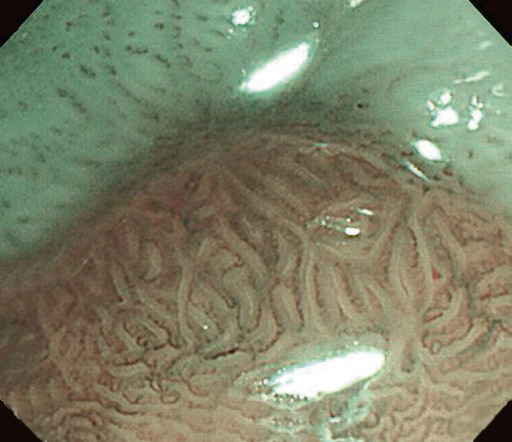
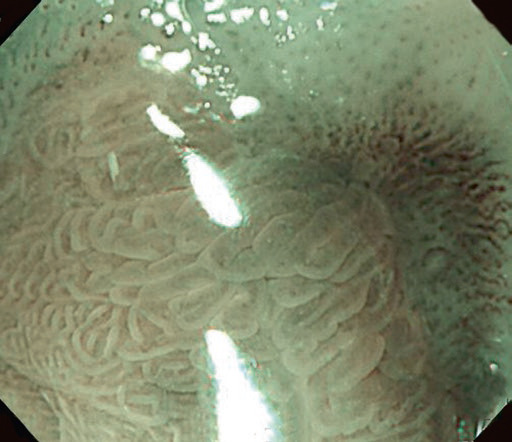
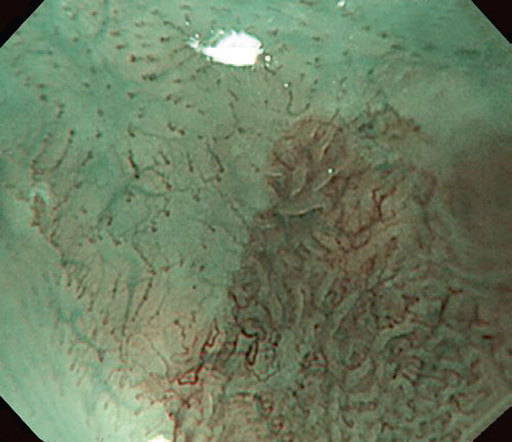

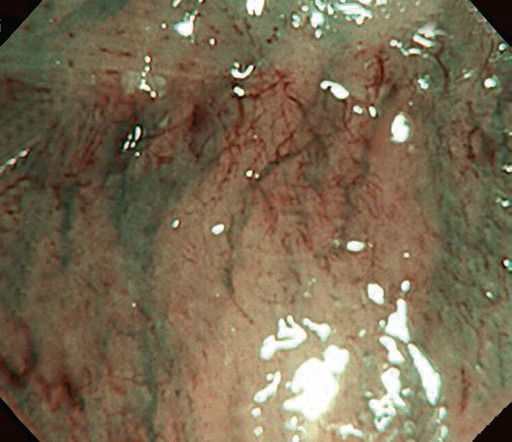
Рис. 4.5 Результати дослідження шлунково-стравохідного з’єднання за допомогою вузькосмугової системи візуалізації зі збільшенням у пацієнтів з неерозивною рефлюксною хворобою.
Лікування
Кислотознижуюче лікування
Інгібітори протонної помпи (ІПП) є основою як гострої, так і підтримуючої терапії ГЕРХ. ІПП помітно зменшують секрецію шлункового соку, пригнічуючи кінцевий загальний шлях насоса секреції кислоти (рис. 4.6).
Фундоплікація
Лапароскопічна фундоплікація є поширеною операцією для лікування рефлюкс-езофагіту. Правильно виконана фундоплікація повинна бути короткою, прямою, паралельною до діафрагми та у верхній частині шлунка (рис. 4.7).
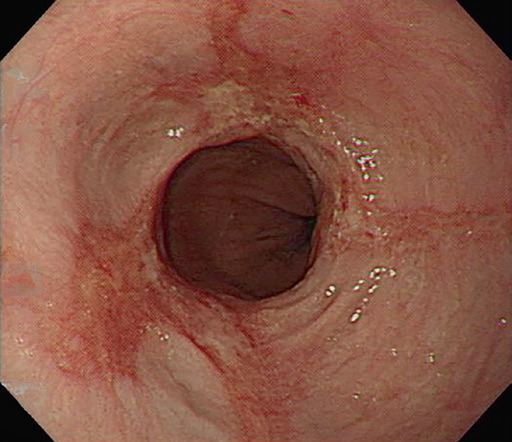
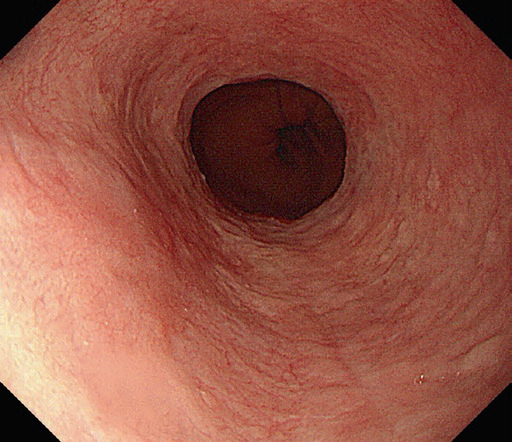
Рис. 4.6 Приклад вилікуваного рефлюкс-езофагіту після лікування інгібітором протонної помпи.
Сторожовий поліп (складка)
Сторожова складка або поліп – це поліпоїдна складка безпосередньо дистальніше стравохідно-шлункового переходу. Ендоскопічно сторожова складка зазвичай виявляється в ділянці вогнищевих тяжких ерозій або виразок. Біопсія складки виявляє нормальний стовпчастий епітелій з прихованим гострим і хронічним запаленням. Після агресивної антирефлюксної терапії складка зникає або значно зменшується в розмірах (рис. 4.8).

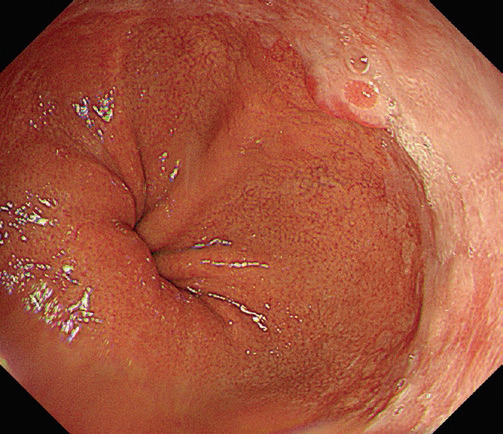
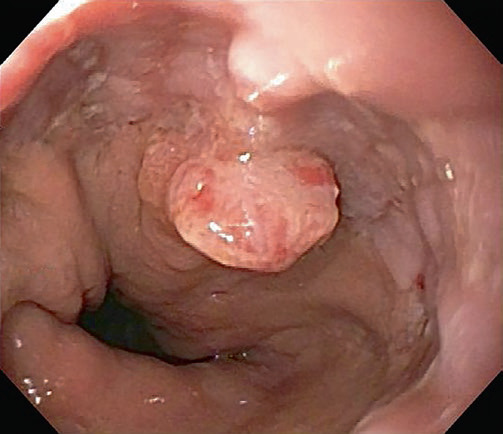
Рис. 4.8 Сторожові поліпи.
Пептичні стриктури
Пептичні стриктури розвиваються в ділянці стравохідно-шлункового переходу внаслідок тривалої ГЕРХ та запалення з фіброзом і рубцюванням. Більшість стриктур короткі, але деякі можуть простягатися на кілька сантиметрів у дистальному відділі стравоходу (рис. 4.9). Найбільш ранньою зміною зазвичай є потовщення лінії Z, за яким слідує концентричне звуження просвіту.
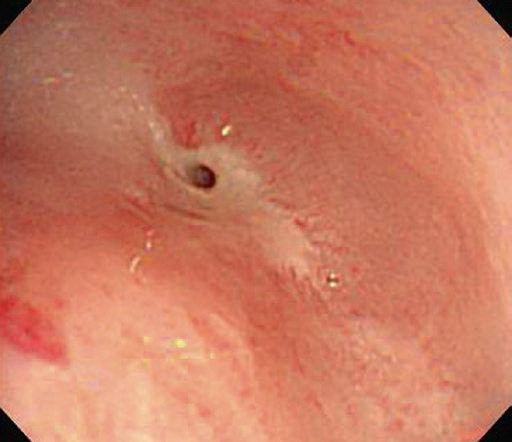
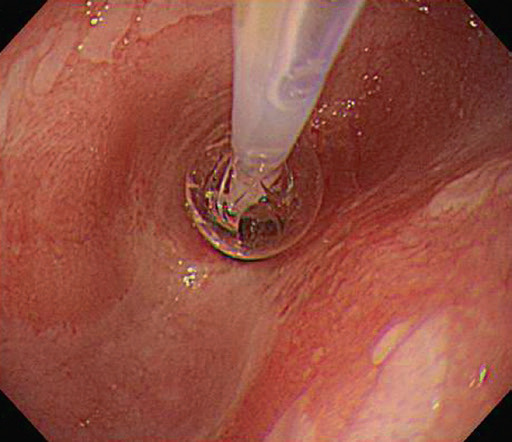
Рис. 4.9 Стриктура, асоційована з рефлюкс-езофагітом.
Стравохід Барретта
Стравохід Барретта – це стан, при якому плоский епітелій дистального відділу стравоходу заміщується стовпчастим епітелієм кишкового типу (“кишкова метаплазія”, рис. 4.10). Ця зміна відбувається, коли плоский епітелій стравоходу, пошкоджений хронічним рефлюксом, замінюється метапластичним стовпчастим епітелієм. Важливість цієї знахідки – а отже, необхідність її виявлення, підтвердження за допомогою біопсії та моніторингу прогресування – полягає в тому, що ризик утворення аденокарциноми в стравоході, вистеленому стовпчастим епітелієм, становить приблизно 10%.
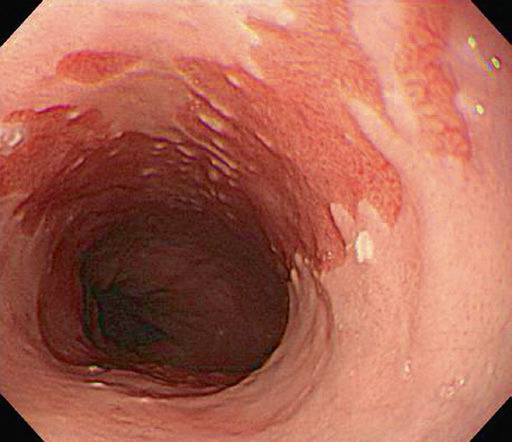
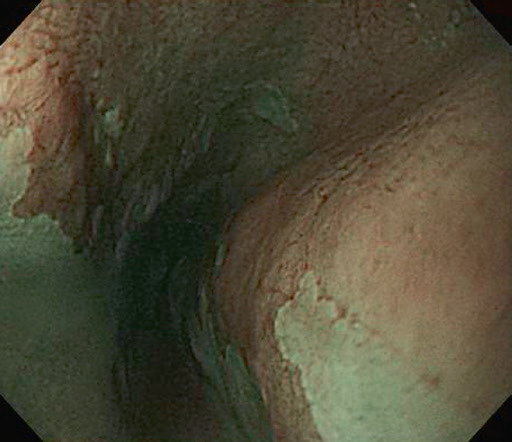
Рис. 4.10 Стравохід Барретта.
Ендоскопія є найточнішим інструментом для виявлення та діагностики стравоходу Барретта. Щоб ендоскопічно діагностувати наявність стравоходу Барретта, необхідно чітко ідентифікувати сквамоколонне з’єднання та шлунково-стравохідний перехід. Хоча проксимальне зміщення сквамоколонного з’єднання відносно шлунково-стравохідного з’єднання вказує на наявність БЕ, ендоскопічна поява слизової оболонки лососевого кольору або неправильної Z-лінії, окремо або в комбінації, не є достатньою для постановки діагнозу. Для гістологічного підтвердження стовпчастого епітелію завжди слід брати біопсію для гістологічного дослідження.
Пацієнтам зі стравоходом Барретта без ознак дисплазії при первинній ендоскопії слід провести повторну ендоскопію протягом наступного року. Якщо дисплазія не підтверджується, ці пацієнти вважаються такими, що мають низький ризик прогресування захворювання або розвитку раку. Тому інтервал додаткового спостереження рекомендовано проводити кожні 3 роки. Якщо підтверджується дисплазія високого ступеня, епітелій Барретта слід видалити. Останнім часом для лікування диспластичного стравоходу Барретта успішно застосовують альтернативні ендоскопічні методи лікування, такі як ендоскопічна резекція слизової оболонки, термічна коагуляція або фотодинамічна терапія.
Празька класифікація була розроблена для стандартизації класифікації стравоходу Барретта. У цій класифікації під час ендоскопічного дослідження вимірюється як максимальна довжина (М) стравоходу Барретта (включаючи язичок), так і довжина циркулярного сегмента Барретта (С). Ці показники можуть бути використані для спостереження за сегментом Барретта з плином часу. Ця система має високий ступінь загальної валідності для ендоскопічної оцінки візуалізованого сегмента стравоходу Барретта, якщо він має довжину >1 см (рис. 4.11).
Цікава вікторина
Жінка 54 років звернулася до нашої клініки зі скаргами на дисфагію, печію та біль за грудиною тривалістю 5 днів. Ці симптоми розвинулися раптово вранці за 5 днів до її візиту. Симптоми не зникали, що змусило пацієнтку звернутися за медичною допомогою. Після опитування вона пройшла скринінгові обстеження 3 місяці тому, які складалися з верхньої ендоскопії, сонографії органів черевної порожнини, кісткової денситометрії та рентгенографії грудної клітки. Ці обстеження не виявили жодних відхилень від норми, окрім остеопорозу, внаслідок чого пацієнтка регулярно приймала бісфосфонат. Через стійкість симптомів пацієнтці було проведено ендоскопію верхніх відділів шлунково-кишкового тракту, як показано на рис. 4.12. Який, на Вашу думку, найбільш вірогідний діагноз?
Відповідь. Медикаментозний езофагіт.
П’ять днів тому вона прийняла таблетку бісфосфонату перед сном, оскільки забула прийняти її вранці. На той час вона не відчувала жодних симптомів чи розпирання в загрудинній ділянці.
Ендоскопічне дослідження виявило непомітну виразку з кількома ерозивними ураженнями на відстані приблизно 25 см від різців. Лікування складалося з рідких антацидів та ранітидину. На четвертий день лікування симптоми повністю зникли.
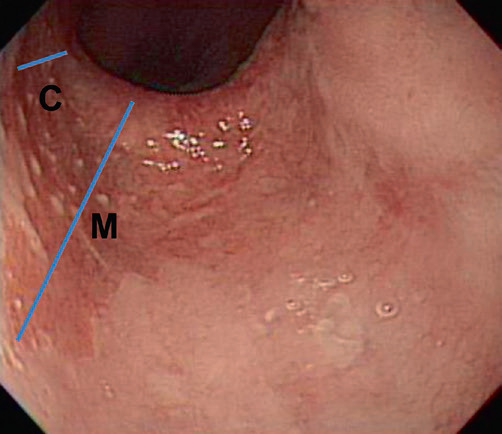
Рис. 4.11 Празька класифікація стравоходу Барретта. У цій класифікації під час ендоскопії вимірюють як максимальну довжину (М) (включаючи язичок) стравоходу Барретта, так і довжину циркулярного сегмента Барретта (С). Ці цифри потім можна використовувати для відстеження довжини сегмента Барретта з плином часу
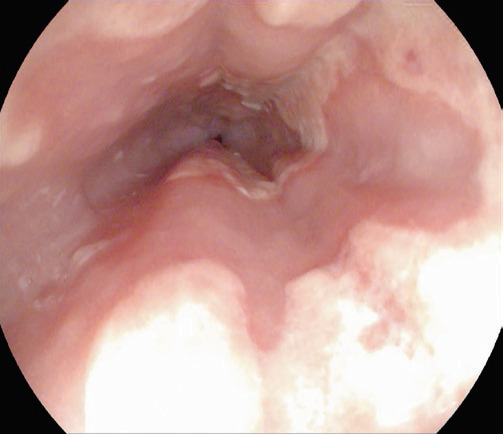
Рис. 4.12 Ендоскопічне дослідження виявило непомітну виразку з кількома ерозивними ураженнями на відстані приблизно 25 см від різців